Clear Sky Science · de
TREM1–NLRP3-getriebene Pyroptose bei sepsisassoziiertem akutem Nierenschaden (AKI) mit parallelen Autophagie-Veränderungen
Warum diese Nierengeschichte wichtig ist
Sepsis, eine lebensbedrohliche Reaktion auf eine Infektion, trifft häufig zuerst die Nieren und führt jährlich bei Millionen von Menschen zu akutem Nierenversagen. Sobald die Nieren versagen, steigt das Sterberisiko deutlich an, doch Ärzten fehlen noch präzise Frühsignale und gezielte Therapien. Diese Studie untersucht eine neu entdeckte Kettenreaktion in Nierenzellen während der Sepsis — eine Reaktion, die schützende Immunantworten in einen selbstzerstörerischen Sturm verwandeln kann — und fragt, ob das Unterbrechen dieser Kette sowohl frühere Warnhinweise liefern als auch die Nieren vor schweren Schäden schützen könnte.
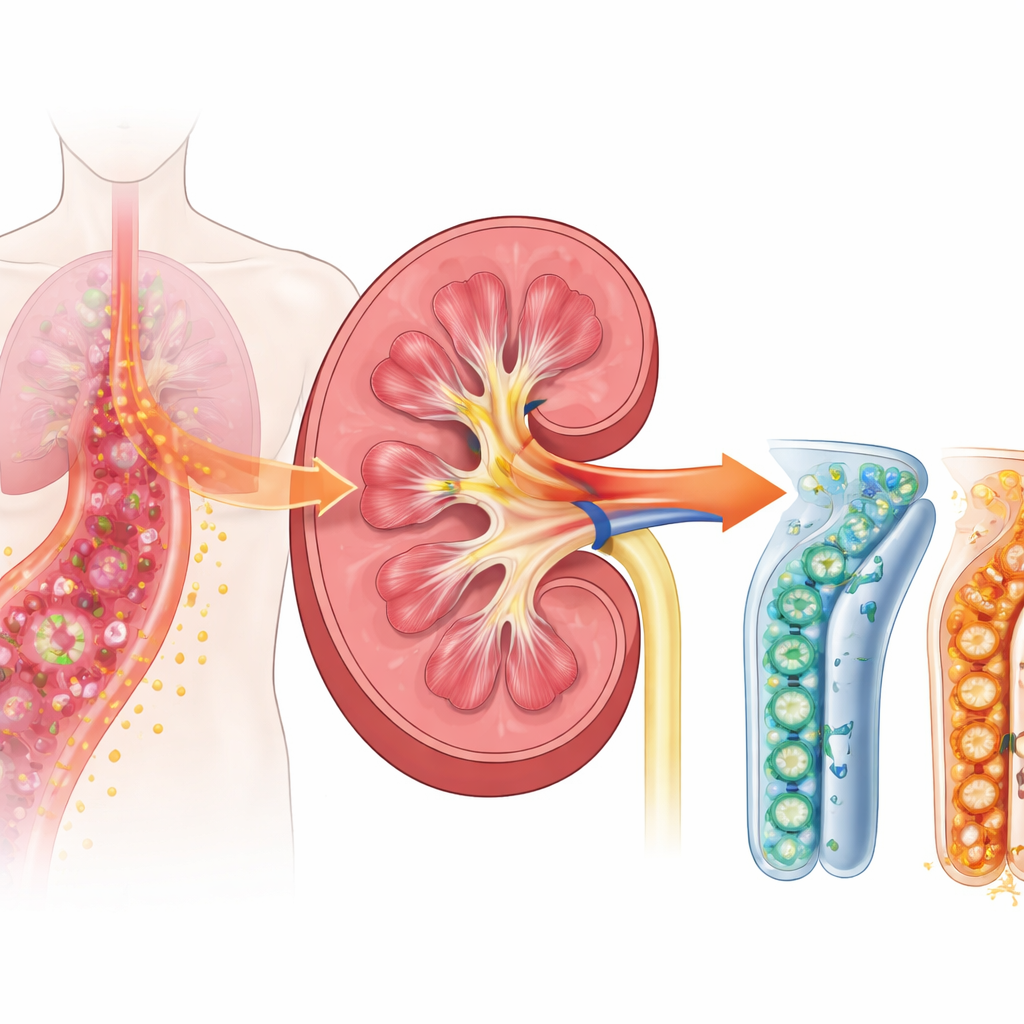
Eine gefährliche Kettenreaktion bei Sepsis
Wenn sich eine Sepsis entwickelt, fährt das Immunsystem hoch, um eindringende Mikroben zu bekämpfen. Die Nieren sind nicht nur Filter; ihre Tubuluszellen helfen auch dabei, Infektionen zu erkennen und darauf zu reagieren. Die Forscher konzentrierten sich auf einen Oberflächenrezeptor namens TREM-1, der auf Immunzellen sitzt und, wie neuere Arbeiten nahelegen, auch auf Nierentubuluszellen vorkommt. TREM-1 wirkt wie ein Lautstärkeregler für Entzündungen: Wird er hochgedreht, kann er die Alarmsignale, die Schwellung, Fieber und Gewebeschäden antreiben, stark verstärken. Frühere Patientenstudien zeigten, dass eine lösliche Form dieses Rezeptors, die ins Blut und den Urin abgegeben wird, früh in der Sepsis ansteigt und mit Nierenproblemen verknüpft ist, was darauf hindeutet, dass TREM-1 ein wichtiger Auslöser des Schadens sein könnte.
Vom Warnsignal zur Zellexplosion
In den Nierentubuluszellen untersuchte das Team, wie TREM-1 mit einer molekularen Maschine namens Inflammasom verbunden ist, die eine dramatische Form des Zelltods steuert, die manchmal als zellulare Explosion beschrieben wird. Bei Mäusen, die einem Standard-Sepsismodell unterzogen wurden, stellten die Autoren fest, dass Sepsis die TREM-1-Spiegel in den Nieren und im Blut stark erhöhte, begleitet von der Aktivierung eines um das Protein NLRP3 aufgebauten Inflammasoms. Sobald dieses Komplex eingeschaltet ist, aktiviert es Enzyme, die Löcher in Zellmembranen schlagen und starke entzündungsfördernde Moleküle freisetzen, wodurch die Zelle dabei zugrunde geht. Dieses feurige Todesprogramm, als Pyroptose bekannt, kann bei der Beseitigung von Infektionen helfen, aber wenn es unkontrolliert abläuft, kann es auch große Bereiche des empfindlichen Nierengewebes zerstören.
Den Lautstärkeregler herunterdrehen und den Weg testen
Um zu prüfen, wie entscheidend TREM-1 in dieser Kettenreaktion ist, verwendeten die Forscher Mäuse, bei denen das Trem1-Gen genetisch entfernt worden war. Im Vergleich zu normalen Mäusen, die demselben septischen Reiz ausgesetzt wurden, zeigten diese Knockout-Tiere weniger strukturelle Schäden in ihren Nierentubuli, niedrigere Blutspiegel von Abbauprodukten wie Kreatinin und Harnstoff und weniger zirkulierende Entzündungsmediatoren. Ihre Nieren wiesen außerdem reduzierte Zeichen von NLRP3-Inflammasom-Aktivität und pyroptotischem Zelltod auf. Als das Team NLRP3 direkt mit einem Wirkstoff blockierte, verbesserte sich die Nierenverletzung selbst bei normalen Mäusen, während eine künstliche Überaktivierung von NLRP3 die Schäden verschlimmerte, selbst wenn Trem1 fehlte. Zusammen ordnen diese Experimente TREM-1 klar stromaufwärts von NLRP3 in der Verletzungskaskade ein.
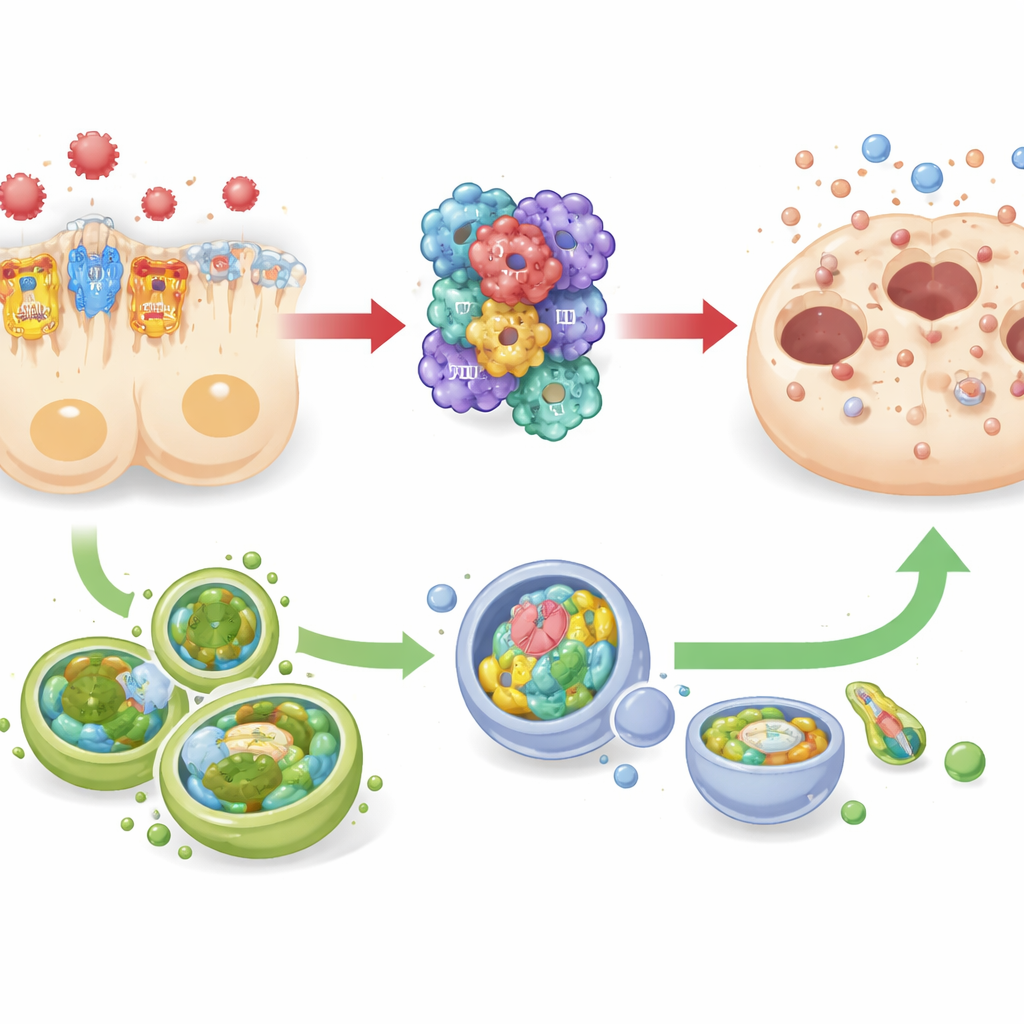
Ein Tauziehen mit der Zellaufräumcrew
Die Studie verfolgte außerdem Veränderungen der Autophagie — eines eingebauten Aufräum- und Recyclingsystems, das Zellen hilft, Stress zu überstehen, indem es beschädigte Komponenten entfernt. Sowohl bei septischen Mäusen als auch in menschlichen Nierentubuluszellen, die im Labor kultiviert wurden, ging eine Herunterregulierung von TREM-1 mit höheren Spiegeln von Autophagie-Markern einher, während stärkere TREM-1-Signale mit verringerter Autophagie korrelierten. Zur gleichen Zeit bewegten sich Inflammasom-Aktivität und Zelltodmarker in die entgegengesetzte Richtung. Dieses Muster deutet auf eine Druck-gegen-Zug-Beziehung hin: TREM-1 und NLRP3 wirken zusammen wie ein „Gaspedal“ für zerstörerische Entzündung, während die Autophagie eher wie eine „Bremse“ funktioniert, die diesem Antrieb entgegenwirken könnte. Da die Forscher jedoch Autophagie nicht direkt ein- oder ausschalteten, warnen sie, dass ihre schützende Rolle, obwohl stark vermutet, noch bewiesen werden muss.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit Sepsis haben die Ergebnisse zwei zentrale Implikationen. Erstens könnte die lösliche Form von TREM-1 im Blut oder Urin als frühes Warnzeichen dienen, das anzeigt, dass dieser schädliche Weg in den Nieren aktiv ist, noch bevor ein vollständiges Nierenversagen eintritt. Zweitens könnten Wirkstoffe, die TREM-1 oder das NLRP3-Inflammasom dämpfen, eines Tages die Nieren vor sepsisbedingten Schäden schützen — insbesondere bei Patientinnen und Patienten, deren Laborwerte eine starke Aktivierung dieses Wegs zeigen. Die Arbeit zeichnet das Bild eines sepsisassoziierten Nierenschadens als Kampf zwischen einem entzündlichen Beschleuniger und einem internen Aufräumsystem und identifiziert TREM-1 als vielversprechenden Ansatzpunkt, sowohl um Hochrisikopatienten zu erkennen als auch präzisere Therapien zu entwickeln.
Zitation: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Schlüsselwörter: sepsisassoziierter akuter Nierenschaden, TREM-1, NLRP3-Inflammasom, Pyroptose, Autophagie