Clear Sky Science · es
TREM1–NLRP3–mediado piroptosis en lesión renal aguda (LRA) asociada a sepsis con cambios paralelos en la autofagia
Por qué importa esta historia renal
La sepsis, una reacción potencialmente mortal a la infección, a menudo afecta primero a los riñones, provocando insuficiencia renal súbita en millones de personas cada año. Cuando los riñones fallan, el riesgo de muerte aumenta drásticamente, y aun así los médicos carecen de señales de alerta temprana precisas y de tratamientos dirigidos. Este estudio explora una cadena de reacciones recién descubierta dentro de las células renales durante la sepsis—una que puede convertir defensas inmunitarias protectoras en una tormenta autodestructiva—y plantea si interrumpir esta cadena podría tanto señalar el peligro antes como proteger los riñones de un daño severo.
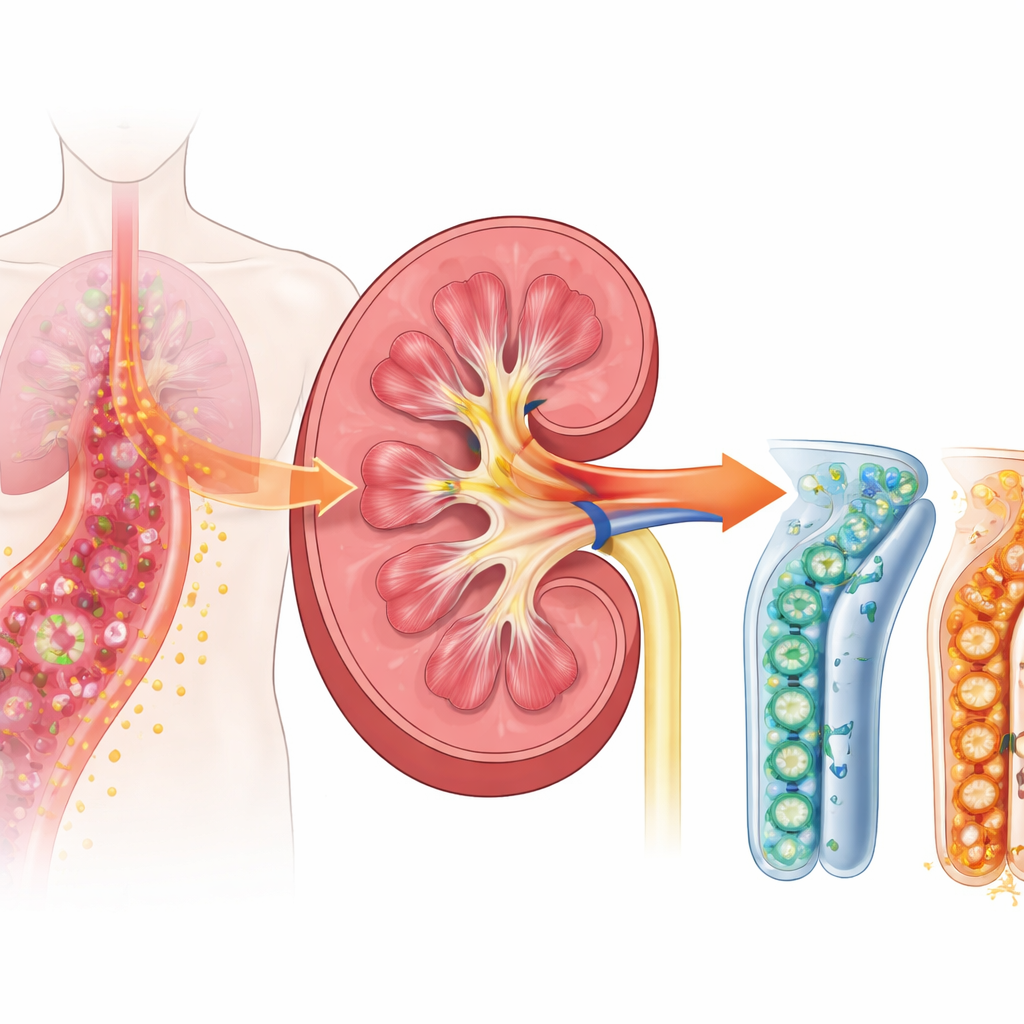
Una peligrosa reacción en cadena en la sepsis
Cuando se desarrolla la sepsis, el sistema inmunitario del cuerpo se dispara para combatir los microbios invasores. Los riñones no son solo filtros; sus células tubulares también ayudan a detectar y responder a la infección. Los investigadores se centraron en un receptor de superficie llamado TREM-1, que se encuentra en células inmunitarias y, según trabajos recientes, también en células del túbulo renal. TREM-1 actúa como un mando de volumen para la inflamación: una vez subido, puede amplificar enormemente las señales de alarma que provocan hinchazón, fiebre y lesión tisular. Estudios previos en pacientes mostraron que una forma soluble de este receptor, liberada en sangre y orina, aumenta de forma temprana en la sepsis y se asocia con problemas renales, lo que sugiere que TREM-1 puede ser un desencadenante aguas arriba importante del daño.
De señal de aviso a explosión celular
Dentro de las células del túbulo renal, el equipo examinó cómo TREM-1 se conecta con una máquina molecular llamada inflamasoma, que controla un tipo dramático de muerte celular a veces descrito como explosión celular. En ratones sometidos a un modelo estándar de sepsis, los autores encontraron que la sepsis aumentó marcadamente los niveles de TREM-1 en los riñones y en la sangre, junto con la activación de un inflamasoma centrado en una proteína llamada NLRP3. Una vez activado, este complejo pone en marcha enzimas que perforan las membranas celulares y liberan potentes moléculas inflamatorias, matando la célula en el proceso. Este programa de muerte ígneo, conocido como piroptosis, puede ayudar a eliminar la infección pero, cuando no se controla, también puede destruir grandes zonas de tejido renal frágil.
Bajar el mando de volumen y probar la vía
Para ver cuán crucial es TREM-1 en esta reacción en cadena, los investigadores usaron ratones modificados genéticamente que carecen del gen Trem1. En comparación con ratones normales sometidos al mismo insulto séptico, estos animales knockout presentaron menos daño estructural en sus túbulos renales, niveles sanguíneos más bajos de productos de desecho como creatinina y urea, y menos moléculas inflamatorias circulantes. Sus riñones también mostraron signos reducidos de actividad del inflamasoma NLRP3 y de muerte celular por piroptosis. Cuando el equipo bloqueó directamente NLRP3 con un fármaco, la lesión renal mejoró incluso en ratones normales, mientras que forzar la hiperactividad de NLRP3 empeoró el daño incluso cuando Trem1 estaba ausente. En conjunto, estos experimentos sitúan a TREM-1 claramente por encima de NLRP3 en la cascada de lesión.
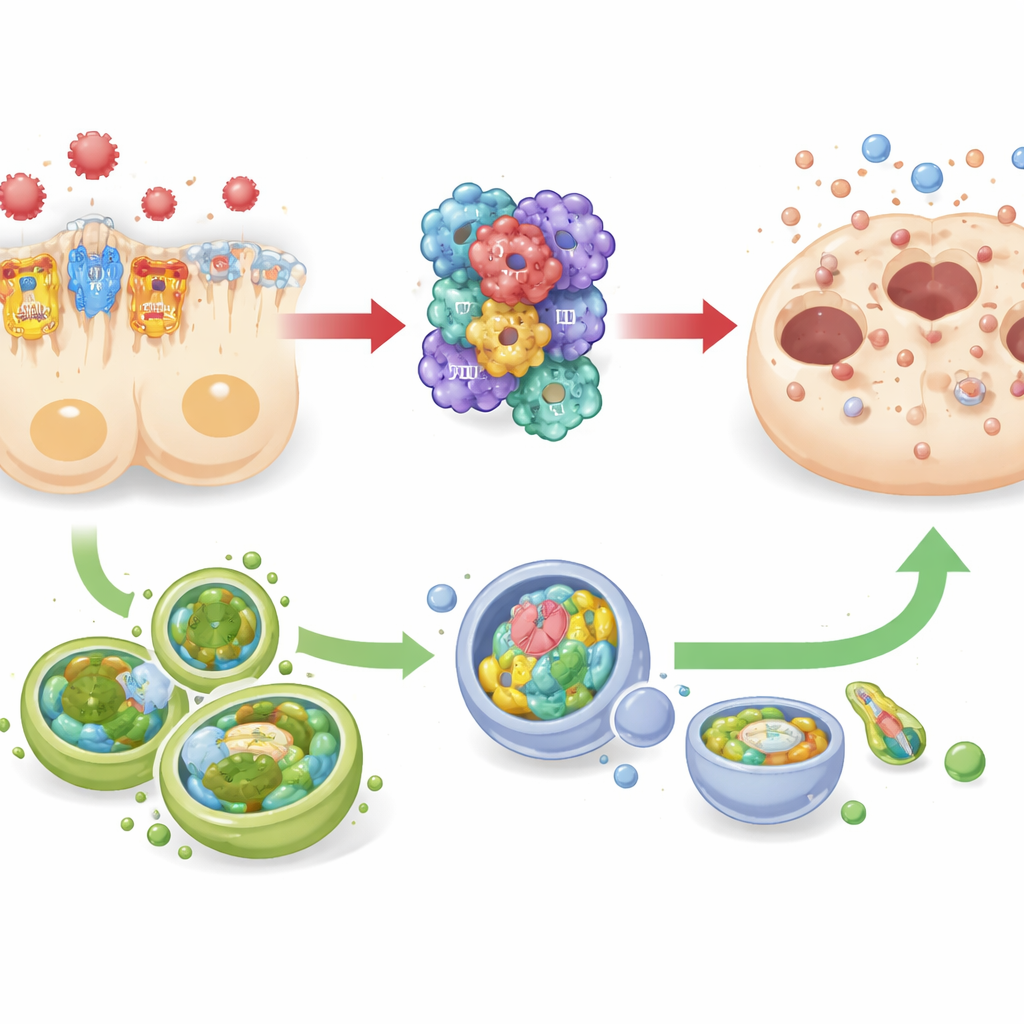
Una lucha con el servicio de limpieza celular
El estudio también siguió cambios en la autofagia—un sistema interno de limpieza y reciclaje que ayuda a las células a sobrevivir al estrés eliminando componentes dañados. Tanto en ratones sépticos como en células del túbulo renal humano cultivadas en el laboratorio, reducir TREM-1 se asoció con niveles más altos de marcadores relacionados con la autofagia, mientras que una señalización de TREM-1 más intensa coincidió con una autofagia reducida. Al mismo tiempo, la actividad del inflamasoma y los marcadores de muerte celular se movieron en la dirección opuesta. Este patrón sugiere una relación de empuje–tirón: TREM-1 y NLRP3 actúan juntos como un “acelerador” de la inflamación destructiva, y la autofagia se comporta más como un “freno” que podría contrarrestar dicha impulsión. Sin embargo, dado que los investigadores no activaron ni inhibieron directamente la autofagia, advierten que su papel protector, aunque muy sugerido, aún debe ser demostrado.
Qué podría significar esto para los pacientes
Para las personas con sepsis, los hallazgos tienen dos implicaciones clave. Primero, la forma soluble de TREM-1 en sangre u orina podría servir como un marcador de advertencia temprano que indique que esta vía dañina está activa en los riñones antes de que aparezca una insuficiencia manifiesta. Segundo, fármacos que atenúen TREM-1 o el inflamasoma NLRP3 podrían algún día proteger los riñones de la lesión relacionada con la sepsis, particularmente en pacientes cuyos análisis muestren una fuerte activación de esta vía. El trabajo dibuja una imagen de la lesión renal asociada a sepsis como una batalla entre un acelerador inflamatorio y un sistema interno de limpieza, e identifica a TREM-1 como un punto de apoyo prometedor tanto para detectar a pacientes de alto riesgo como para diseñar tratamientos más precisos.
Cita: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Palabras clave: lesión renal aguda asociada a sepsis, TREM-1, inflamasoma NLRP3, piroptosis, autofagia