Clear Sky Science · fr
Pyroptose induite par TREM1–NLRP3 dans l’insuffisance rénale aiguë associée à la septicémie (IRA) avec modifications parallèles de l’autophagie
Pourquoi cette histoire rénale est importante
La septicémie, une réaction potentiellement mortelle à une infection, touche souvent les reins en premier, entraînant une défaillance rénale aiguë chez des millions de personnes chaque année. Une fois les reins compromis, le risque de décès augmente fortement, et pourtant les médecins manquent encore de signaux d’alerte précoces précis et de traitements ciblés. Cette étude examine une chaîne de réactions nouvellement mise au jour à l’intérieur des cellules rénales pendant la septicémie — une chaîne qui peut transformer des défenses immunitaires protectrices en une tempête autodestructrice — et se demande si interrompre cette chaîne pourrait à la fois signaler le danger plus tôt et protéger les reins contre des lésions sévères.
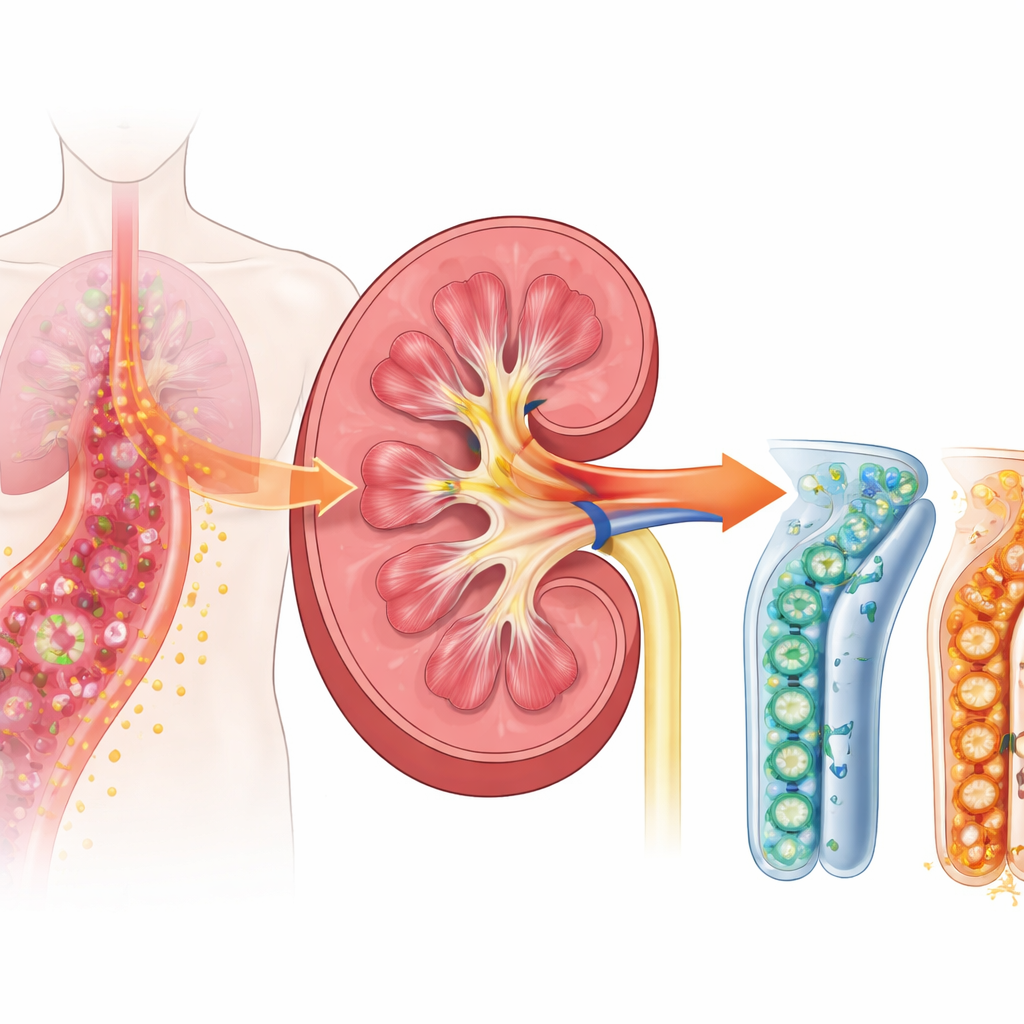
Une chaîne de réactions dangereuse dans la septicémie
Lorsque la septicémie se développe, le système immunitaire se met en surrégime pour combattre les microbes envahisseurs. Les reins ne sont pas de simples filtres ; leurs cellules tubulaires contribuent aussi à détecter et répondre à l’infection. Les chercheurs se sont concentrés sur un récepteur de surface appelé TREM-1, présent sur les cellules immunitaires et, selon des travaux récents, également sur les cellules tubulaires rénales. TREM-1 agit comme un bouton de volume pour l’inflammation : une fois monté, il peut fortement amplifier les signaux d’alarme qui provoquent gonflement, fièvre et lésions tissulaires. Des études antérieures chez l’homme ont montré qu’une forme soluble de ce récepteur, libérée dans le sang et l’urine, augmente précocement lors de la septicémie et est associée à des problèmes rénaux, suggérant que TREM-1 pourrait être un déclencheur en amont important des lésions.
Du signal d’alerte à l’explosion cellulaire
À l’intérieur des cellules tubulaires rénales, l’équipe a examiné comment TREM-1 se relie à une machine moléculaire appelée inflammasome, qui contrôle un type spectaculaire de mort cellulaire parfois décrit comme une explosion cellulaire. Chez des souris soumises à un modèle standard de septicémie, les auteurs ont constaté que la septicémie augmentait fortement les niveaux de TREM-1 dans les reins et dans la circulation sanguine, parallèlement à l’activation d’un inflammasome centré sur une protéine nommée NLRP3. Une fois activé, ce complexe met en jeu des enzymes qui perforent les membranes cellulaires et libèrent des molécules inflammatoires puissantes, entraînant la mort de la cellule. Ce programme de mort enflammatoire, connu sous le nom de pyroptose, peut aider à éliminer l’infection mais, s’il n’est pas contrôlé, peut aussi détruire de vastes zones de tissu rénal fragile.
Régler le bouton de volume et tester la voie
Pour évaluer l’importance de TREM-1 dans cette cascade, les chercheurs ont utilisé des souris génétiquement modifiées dépourvues du gène Trem1. Comparées aux souris normales soumises au même stimulus septicémique, ces animaux knockout présentaient moins de lésions structurelles dans leurs tubules rénaux, des taux sanguins plus faibles de déchets tels que la créatinine et l’urée, et moins de molécules inflammatoires en circulation. Leurs reins montraient également des signes réduits d’activité de l’inflammasome NLRP3 et de mort cellulaire par pyroptose. Lorsque l’équipe a bloqué directement NLRP3 avec un médicament, les lésions rénales se sont améliorées même chez des souris normales, tandis que forcer l’activation de NLRP3 a aggravé les lésions même en l’absence de Trem1. Ensemble, ces expériences placent clairement TREM-1 en amont de NLRP3 dans la cascade de lésions.
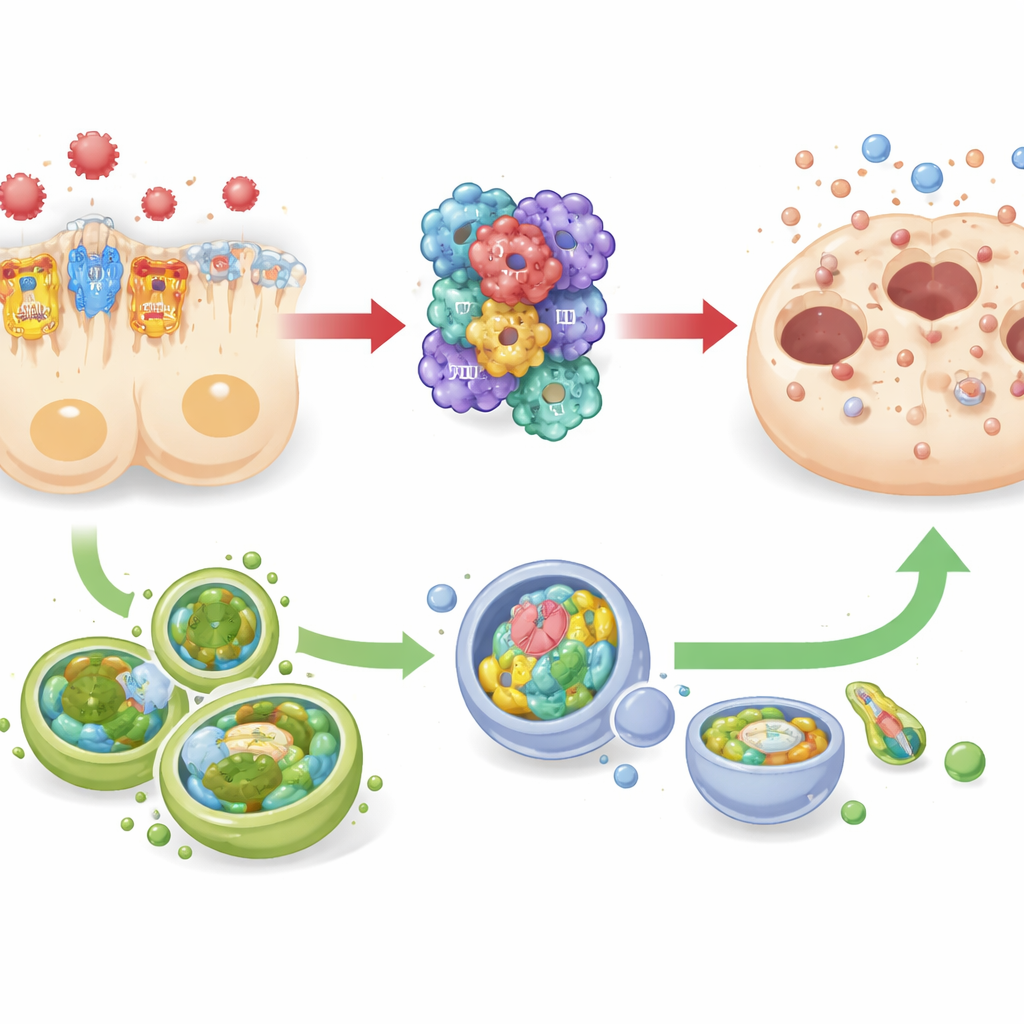
Une lutte entre l’accélérateur inflammatoire et l’équipe de nettoyage cellulaire
L’étude a également suivi les modifications de l’autophagie — un système intégré de nettoyage et de recyclage qui aide les cellules à survivre au stress en éliminant les composants endommagés. Chez les souris septicémiques et dans des cellules tubulaires rénales humaines cultivées en laboratoire, l’atténuation de TREM-1 était associée à des niveaux plus élevés de marqueurs liés à l’autophagie, tandis qu’une signalisation TREM-1 renforcée coïncidait avec une autophagie réduite. Dans le même temps, l’activité de l’inflammasome et les marqueurs de mort cellulaire évoluaient en sens inverse. Ce schéma suggère une relation de tiraillement : TREM-1 et NLRP3 agissant de concert comme une « pédale d’accélérateur » pour une inflammation destructrice, et l’autophagie se comportant davantage comme un « frein » susceptible de contrebalancer cette poussée. Toutefois, comme les chercheurs n’ont pas activé ou inhibé directement l’autophagie, ils précisent que son rôle protecteur, bien que fortement soupçonné, reste à démontrer.
Ce que cela pourrait signifier pour les patients
Pour les personnes atteintes de septicémie, les résultats ont deux implications principales. D’une part, la forme soluble de TREM-1 dans le sang ou l’urine pourrait servir de marqueur d’alerte précoce indiquant que cette voie délétère est active dans les reins avant l’apparition d’une défaillance complète. D’autre part, des médicaments qui atténuent TREM-1 ou l’inflammasome NLRP3 pourraient un jour protéger les reins contre les lésions liées à la septicémie, en particulier chez les patients dont les analyses montrent une forte activation de cette voie. Ce travail brosse le tableau de l’insuffisance rénale associée à la septicémie comme d’une bataille entre un accélérateur inflammatoire et un système interne de nettoyage, et identifie TREM-1 comme une cible prometteuse pour repérer les patients à haut risque et concevoir des traitements plus précis.
Citation: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Mots-clés: insuffisance rénale aiguë associée à la septicémie, TREM-1, inflammasome NLRP3, pyroptose, autophagie