Clear Sky Science · zh
巨噬细胞中的Notch-1通过调控EZH2/HSF1/BRD4/SIRPα/SHP2引发的ROS和凋亡促进缺血-再灌注损伤在心肌细胞中的发生
为何心脏修复有时会伤害心脏
当医生在心肌梗死后重新开放被堵塞的冠状动脉时,血液会涌回缺血的组织。这种挽救性的再灌注能挽救生命——但同时也可能进一步损伤心脏。该研究探讨了为什么本应有助于修复的免疫细胞反而会加剧所谓的“再灌注损伤”,并指出了可能被调控以在未来治疗中保护心脏的分子开关。
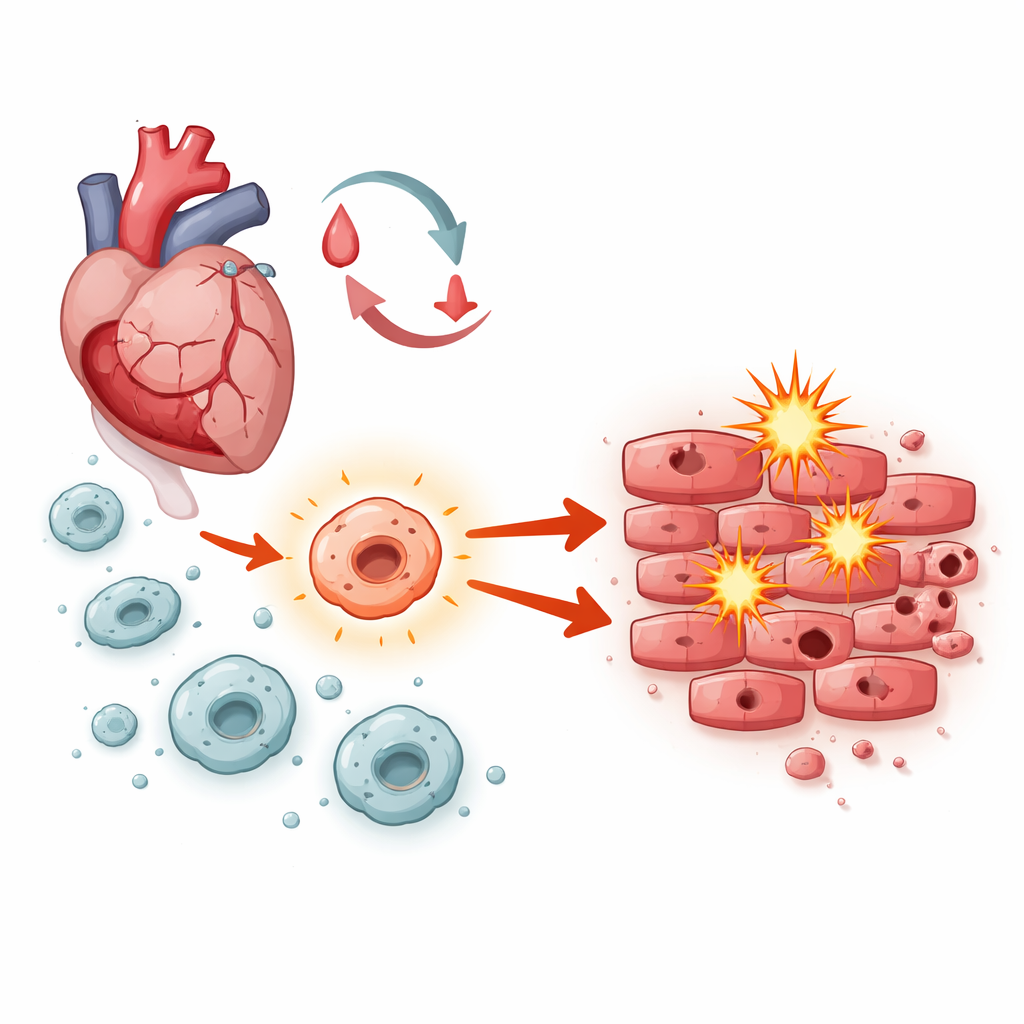
愈合心脏内部的拉锯战
在血流恢复后,心肌细胞面临一场压力风暴:氧气的骤变、不稳定分子的突发暴增以及炎症浪潮。巨噬细胞——作为冲到受损组织前线的免疫细胞——在决定后续进程中起核心作用。根据它们的激活状态不同,它们既能清除残骸并支持修复,也能推动肿胀和细胞死亡。研究人员关注巨噬细胞内的一套信号系统Notch‑1,探究它在缺血‑再灌注损伤中是否会将这种平衡倾向于修复还是伤害。
从基因到大鼠再到心肌细胞的深入探索
团队首先挖掘了来自急性心肌梗死患者的公共基因表达数据库。他们鉴定出100多个表达显著变化的基因,尤其集中在与炎症和细胞自杀相关的通路中。与Notch相关的基因尤为突出,提示该通路在心脏损伤期间处于活跃状态。随后科学家在大鼠身上模拟患者的情形,暂时阻断并重新开放冠状动脉。他们向动物体内输注经过基因改造以增强或改变Notch‑1信号的巨噬细胞,并通过超声评估心脏泵血功能、用显微镜观察组织结构,以及检测坏死组织和濒死细胞的范围。
一个免疫开关如何驱动损伤
接受高Notch‑1活性巨噬细胞的大鼠情况更差:心脏泵血效率下降、组织结构更紊乱、坏死肌肉区域更大且濒死细胞更多。通过有针对性地添加或阻断其他分子,研究团队绘制出Notch‑1在巨噬细胞内的下游事件链。在该链中,Notch‑1抑制了一个称为EZH2的基因调控因子,进而释放出包括BRD4、HSF1、SIRPα和SHP2在内的其他蛋白,使其活性增强。这些分子共同将巨噬细胞推向高度炎性状态,促使活性氧(reactive oxygen species)过度生成——这些具有化学侵袭性的氧化产物能打破细胞膜并损伤DNA。
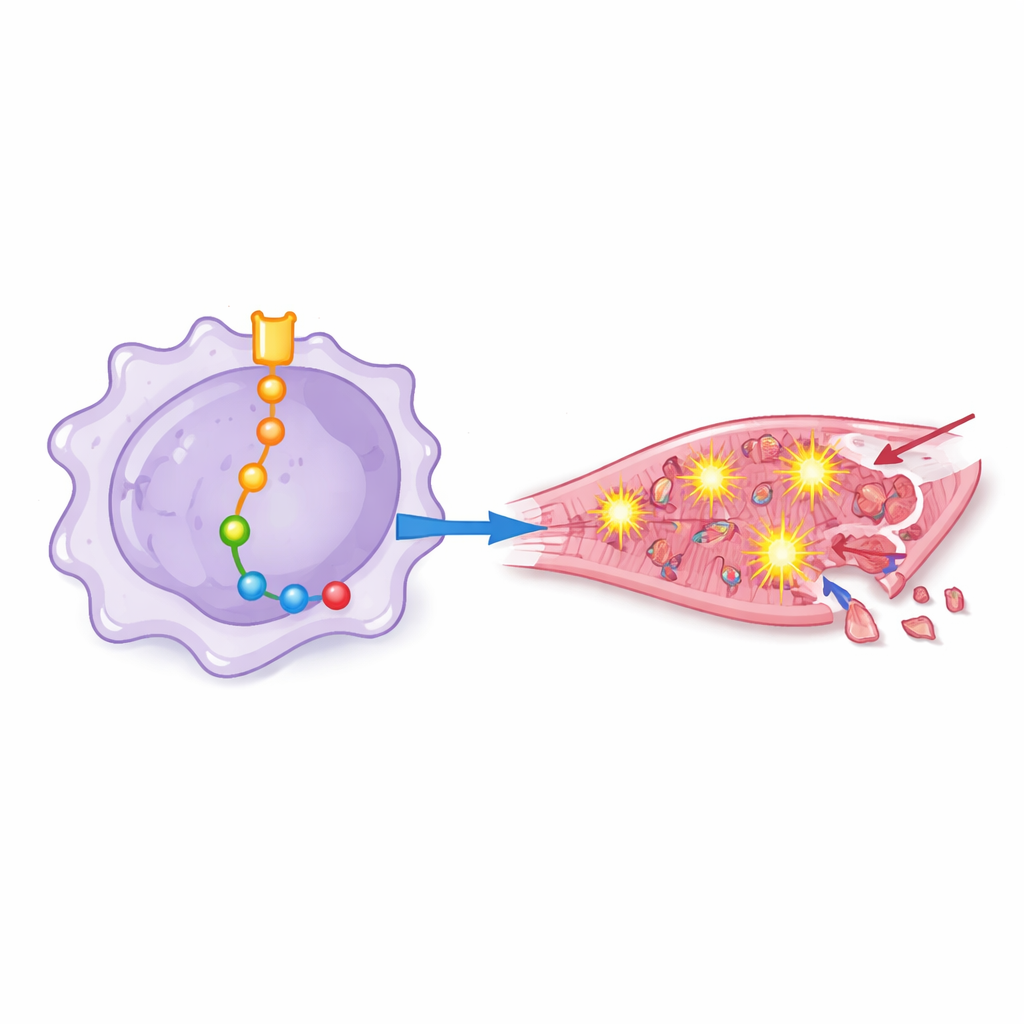
从化学性应激到心肌细胞死亡
为了观察这些“被激活”的巨噬细胞如何影响人类心肌细胞,研究者将培养的心肌细胞置于来自不同基因修饰巨噬细胞培养液的处理下。来自高Notch‑1信号巨噬细胞的培养液诱发了更高的氧化应激、促炎蛋白复合体(称为炎性小体)的更强激活,以及程序性细胞死亡标志物的激增。当Notch‑1或某些下游蛋白被阻断时,心肌细胞表现出较少的氧化损伤迹象、保持了更好的抗氧化防御,并且死亡率降低。这表明这些有害效应并非抽象的分子改变,而是直接导致心肌细胞丧失。
这对未来心脏护理意味着什么
简言之,该研究表明巨噬细胞内名为Notch‑1的信号开关可以在血流恢复的关键窗口期将其推向有害模式。通过包含EZH2、HSF1、BRD4、SIRPα和SHP2的多步分子接力,这些细胞向邻近心肌释放破坏性氧分子和触发细胞自毁的信号,从而扩大损伤。尽管这项工作在细胞和动物模型中完成,但它强调了可用于抑制过度活化巨噬细胞、在动脉再通时减少附带损伤的新药物靶点——有望帮助未来患者在心梗后保留更多心肌组织。
引用: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
关键词: 心肌缺血-再灌注, 巨噬细胞, Notch-1信号通路, 氧化应激, 心肌细胞凋亡