Clear Sky Science · nl
Notch-1 in macrofagen bevorderde ischemie-reperfusie via modulatie van EZH2/HSF1/BRD4/SIRPα/SHP2-geïnduceerde ROS en apoptose in cardiomyocyten
Waarom hartherstel het hart soms kan schaden
Wanneer artsen een geblokkeerde kransslagader openen na een hartinfarct, stroomt bloed weer terug in het eerder van zuurstof gespeende weefsel. Die redding, reperfusie genoemd, redt levens — maar kan het hart ook verder beschadigen. Deze studie onderzoekt waarom de eigen immuuncellen van het lichaam, bedoeld om te helpen bij herstel, deze reperfusieschade juist kunnen verergeren, en wijst op moleculaire schakelaars die mogelijk aangepast kunnen worden om het hart in toekomstige behandelingen te beschermen.
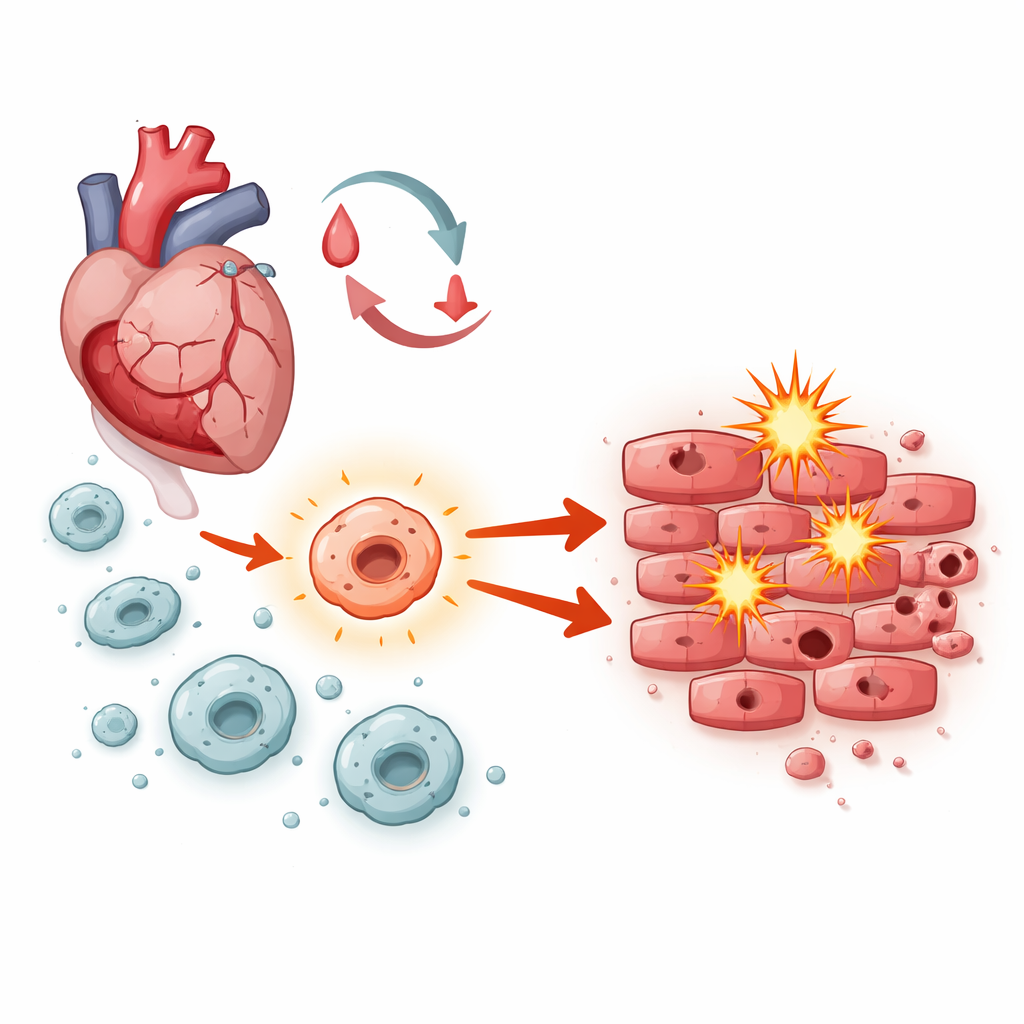
Het touwtrekken binnen een herstellend hart
Nadat de bloedstroom is hersteld, krijgen hartspiercellen te maken met een storm van stress: plotselinge veranderingen in zuurstof, uitbarstingen van onstabiele moleculen en golven van ontsteking. Macrofagen — eerstelijns immuuncellen die zich naar beschadigd weefsel haasten — spelen een centrale rol in het orkestreren van wat er vervolgens gebeurt. Afhankelijk van hoe ze geactiveerd worden, kunnen ze afval opruimen en herstel ondersteunen of juist zwelling en celdood aanjagen. De onderzoekers richtten zich op een signaleringssysteem in macrofagen dat bekendstaat als Notch‑1, en vroegen zich af of het tijdens ischemie‑reperfusieschade de balans richting herstel of schade kantelt.
Onder de motorkap: genen, ratten en hartcellen
Het team begon met het doorzoeken van een openbaar genexpresiedataset van mensen die een acuut hartinfarct hadden doorgemaakt. Ze identificeerden meer dan 100 genen met sterk veranderde activiteit, vooral in routes die verband houden met ontsteking en geprogrammeerde celdood. Notch-gerelateerde genen vielen op, wat suggereerde dat dit pad actief was tijdens hartschade. Vervolgens gebruikten de wetenschappers ratten, waarbij ze tijdelijk een kransslagader afsloten en weer openden om na te bootsen wat bij patiënten gebeurt. Ze gaven de dieren macrofagen die zodanig waren gemanipuleerd dat Notch‑1-signaalverwerking werd versterkt of veranderd, en bestudeerden de pompfunctie van het hart met echografie, de weefselstructuur onder de microscoop en de omvang van dode en stervende cellen.
Hoe één immuunschakel schade aanjaagt
Ratten die macrofagen met hoge Notch‑1-activiteit ontvingen, deden het slechter: hun harten pompten minder efficiënt, vertoonden meer structurele desorganisatie en bevatten grotere gebieden van afgestorven spier en meer stervende cellen. Door andere moleculen precies toe te voegen of te blokkeren, bracht het team een keten van gebeurtenissen in kaart die volgt op Notch‑1 in macrofagen. In deze keten remde Notch‑1 een genregulator genaamd EZH2, wat op zijn beurt andere eiwitten — waaronder BRD4, HSF1, SIRPα en SHP2 — vrijmaakte om actiever te worden. Gezamenlijk duwden deze moleculen macrofagen in een sterk pro‑inflammatoire toestand die overproductie van reactieve zuurstofsoorten (ROS) aanmoedigde, de chemisch agressieve zuurstofvormen die membranen kunnen doorboren en DNA kunnen beschadigen.
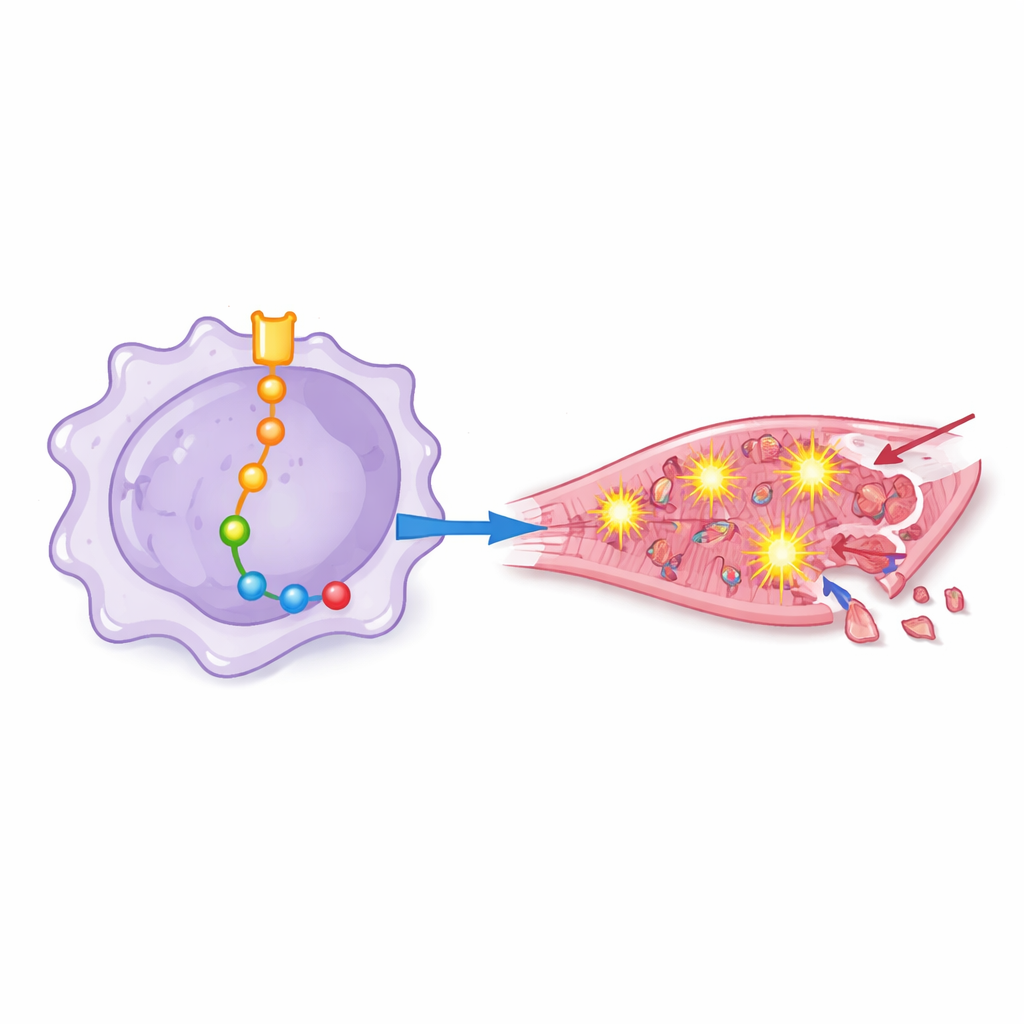
Van chemische stress naar hartcelsterfte
Om te zien hoe deze “geprimede” macrofagen menselijke hartcellen beïnvloeden, dompelden de onderzoekers gekweekte cardiomyocyten in vloeistof afkomstig van verschillend gemodificeerde macrophageculturen. Vloeistof van macrofagen met sterke Notch‑1-signalisering veroorzaakte hogere oxidatieve stress, meer activatie van een ontstekingscomplex dat bekendstaat als het inflammasoom, en een piek in markers van geprogrammeerde celdood. Toen Notch‑1 of bepaalde downstream-eiwitten werden geblokkeerd, toonden hartcellen minder tekenen van oxidatieve schade, behielden ze betere antioxidantverdediging en waren ze minder geneigd te sterven. Dit toonde aan dat de schadelijke effecten niet slechts abstracte moleculaire verschuivingen zijn, maar direct vertalen naar verlies van hartcellen.
Wat dit betekent voor toekomstige hartzorg
Kort gezegd laat de studie zien dat een signaalschakelaar genaamd Notch‑1 in macrofagen deze cellen tijdens het kritieke venster waarin de bloedstroom naar het hart terugkeert, in een schadelijke modus kan duwen. Via een meerstaps moleculair relais met EZH2, HSF1, BRD4, SIRPα en SHP2 overstelpen deze cellen het omliggend hartweefsel met destructieve zuurstofmoleculen en signalen die celdood triggeren, waardoor de beschadiging toeneemt. Hoewel het werk in cellen en dieren is uitgevoerd, belicht het nieuwe doelwitten voor geneesmiddelen die overactieve macrofagen kunnen kalmeren en nevenschade kunnen beperken wanneer een geblokkeerde slagader wordt geopend — wat mogelijk toekomstige patiënten helpt om meer van hun hartspier te behouden na een hartinfarct.
Bronvermelding: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
Trefwoorden: myocardiale ischemie-reperfusie, macrofagen, Notch-1 signalering, oxidatieve stress, apoptose van cardiomyocyten