Clear Sky Science · ru
Notch-1 в макрофагах усиливал ишемию‑реперфузию через модуляцию EZH2/HSF1/BRD4/SIRPα/SHP2, индуцировавших образование ОРВ и апоптоз в кардиомиоцитах
Почему восстановление работы сердца иногда вредит ему
Когда врачи восстанавливают проходимость заблокированной коронарной артерии после инфаркта, к истощённой ткани снова приливает кровь. Это спасительное восстановление — реперфузия — может приносить жизнь, но одновременно наносить дополнительный ущерб сердцу. В этом исследовании изучают, почему собственные иммунные клетки организма, призванные помогать заживлению, могут наоборот усугублять «реперфузионное повреждение», и указывают на молекулярные переключатели, которые в будущем можно будет направленно модулировать для защиты сердца.
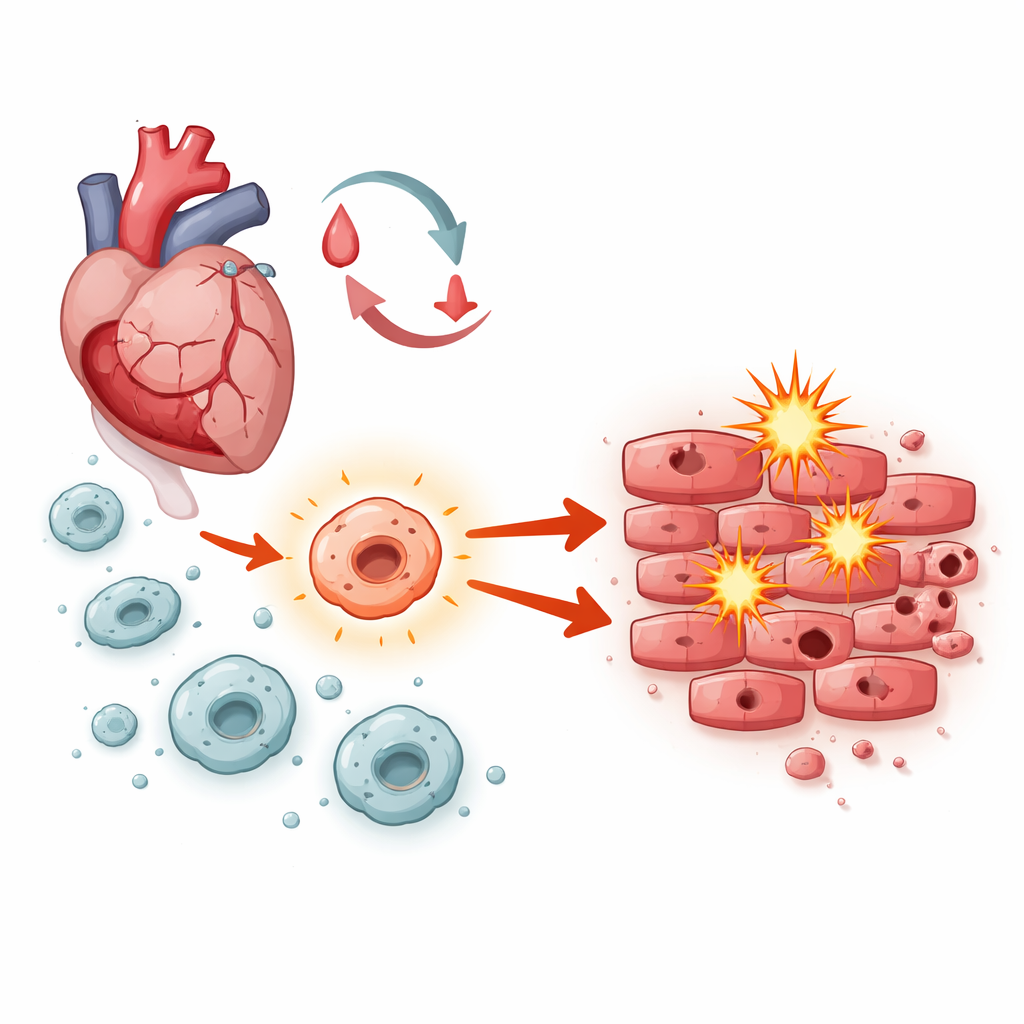
Внутреннее противоборство в заживающем сердце
После восстановления кровотока кардиомиоциты сталкиваются с бурей стрессовых факторов: резкими изменениями кислородного обеспечения, вспышками нестабильных молекул и волнами воспаления. Макрофаги — передовые иммунные клетки, которые вторгаются в повреждённую ткань — играют центральную роль в организации дальнейших событий. В зависимости от типа их активации они могут либо очищать участок и поддерживать восстановление, либо вызывать отёк и гибель клеток. Исследователи сосредоточились на сигнальной системе внутри макрофагов, известной как Notch‑1, чтобы выяснить, склоняет ли она этот баланс в сторону исцеления или вреда при ишемии‑реперфузии.
Гены, крысы и сердечные клетки: как изучали вопрос
Сначала команда проанализировала общедоступный набор данных по экспрессии генов у людей, переживших острый инфаркт. Они выявили более 100 генов с заметно изменённой активностью, особенно в путях, связанных с воспалением и программируемой гибелью клеток. Гены, связанные с Notch, выделялись, что указывало на активность этого пути при повреждении сердца. Затем учёные перешли к опыту на крысах, временно перекрывая и вновь открывая коронарную артерию, моделируя клиническую ситуацию. Животным вводили макрофаги, модифицированные для усиления или изменения сигнального потока Notch‑1, и оценивали сократительную функцию сердца с помощью ультразвука, структуру ткани под микроскопом, а также размеры некротизированных зон и число умирающих клеток.
Как один иммунный переключатель ведёт к повреждению
Крысы, получавшие макрофаги с высокой активностью Notch‑1, переносили нагрузку хуже: их сердца сокращались менее эффективно, демонстрировали более выраженное структурное нарушение и содержали большие участки мёртвой ткани и больше умирающих клеток. Путём точечного добавления или блокирования других молекул команда проследила цепочку событий, разворачивающуюся после активации Notch‑1 в макрофагах. В этой цепи Notch‑1 подавлял регулятор генов EZH2, что, в свою очередь, высвобождало для активации другие белки — включая BRD4, HSF1, SIRPα и SHP2. В совокупности эти молекулы переводили макрофаги в мощно воспалительное состояние, стимулируя чрезмерное образование реактивных форм кислорода — химически агрессивных частиц, способных повреждать мембраны и ДНК клеток.
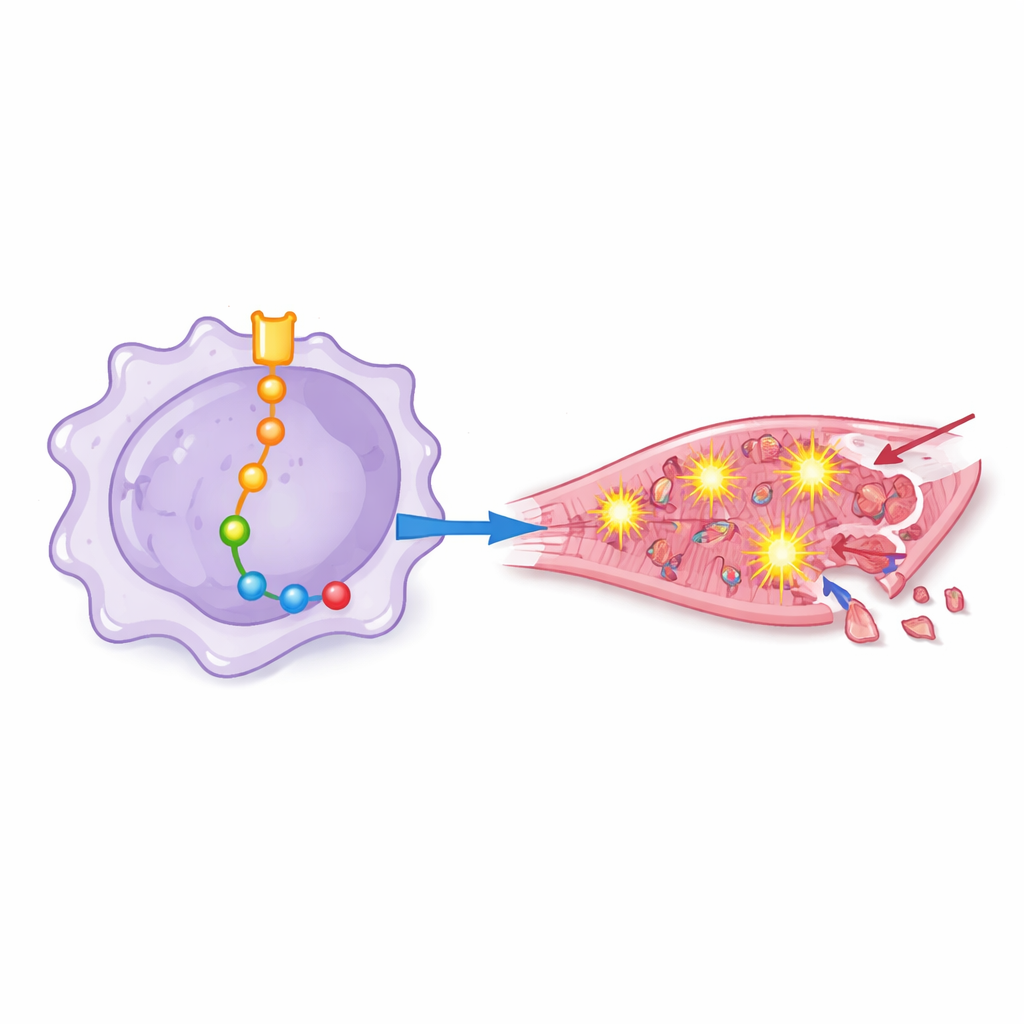
От химического стресса к гибели сердечных клеток
Чтобы проверить, как такие «запрограммированные» макрофаги воздействуют на человеческие кардиомиоциты, исследователи обрабатывали культивируемые сердечные клетки средой, полученной из культур макрофагов с разной инженерной модификацией. Среда от макрофагов с сильной активностью Notch‑1 вызывала повышенный уровень оксидативного стресса, усиление активации воспалительного комплекса — инфламмасомы, и рост маркеров программируемой гибели клеток. При блокировке Notch‑1 или отдельных белков по нисходящей линии кардиомиоциты демонстрировали меньше признаков окислительного повреждения, лучше сохраняли антиоксидантные механизмы и реже погибали. Это показало, что вредоносные эффекты — не просто абстрактные молекулярные сдвиги, а напрямую приводят к гибели сердечных клеток.
Что это значит для будущей терапии сердца
Проще говоря, исследование показывает, что сигнальный переключатель Notch‑1 в макрофагах может переводить их в вредоносный режим в критическое окно восстановления кровотока. Через многоступенчатую молекулярную релейную цепь с участием EZH2, HSF1, BRD4, SIRPα и SHP2 эти клетки насыщают соседний миокард разрушительными молекулами кислорода и сигналами, запускающими клеточный суицид, расширяя очаг поражения. Хотя работа выполнена на клетках и животных, она выделяет новые мишени для лекарственных вмешательств, направленных на подавление чрезмерно активных макрофагов и снижение побочного ущерба при восстановлении проходимости артерии — что потенциально поможет будущим пациентам сохранить больше сердечной ткани после инфаркта.
Цитирование: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
Ключевые слова: ишемия‑реперфузия миокарда, макрофаги, сигнальная система Notch‑1, окислительный стресс, апоптоз кардиомиоцитов