Clear Sky Science · ar
نوترش‑1 في البالعات عزز الإقفار‑إعادة التدفق من خلال تعديل EZH2/HSF1/BRD4/SIRPα/SHP2 المسببة للتأكسد المفاعل والموت المبرمج في خلية القلب
لماذا قد يضر إصلاح القلب القلب أحيانًا
عندما يعيد الأطباء فتح شريان قلب مسدود بعد أزمة قلبية، يتدفق الدم بسرعة إلى نسيج كان محرومًا. هذا الإجراء الإنقاذي، المسمى إعادة التدفق، ينقذ الحياة—لكنّه قد يسبب أيضًا ضررًا إضافيًا للقلب. تستكشف هذه الدراسة لماذا يمكن لخلايا المناعة في الجسم، التي يفترض أن تساعد على الشفاء، أن تساهم بدلًا من ذلك في تفاقم «إصابة إعادة التدفق»، وتشير إلى مفاتيح جزيئية قد يُمكن تعديلها لحماية القلب في علاجات مستقبلية.
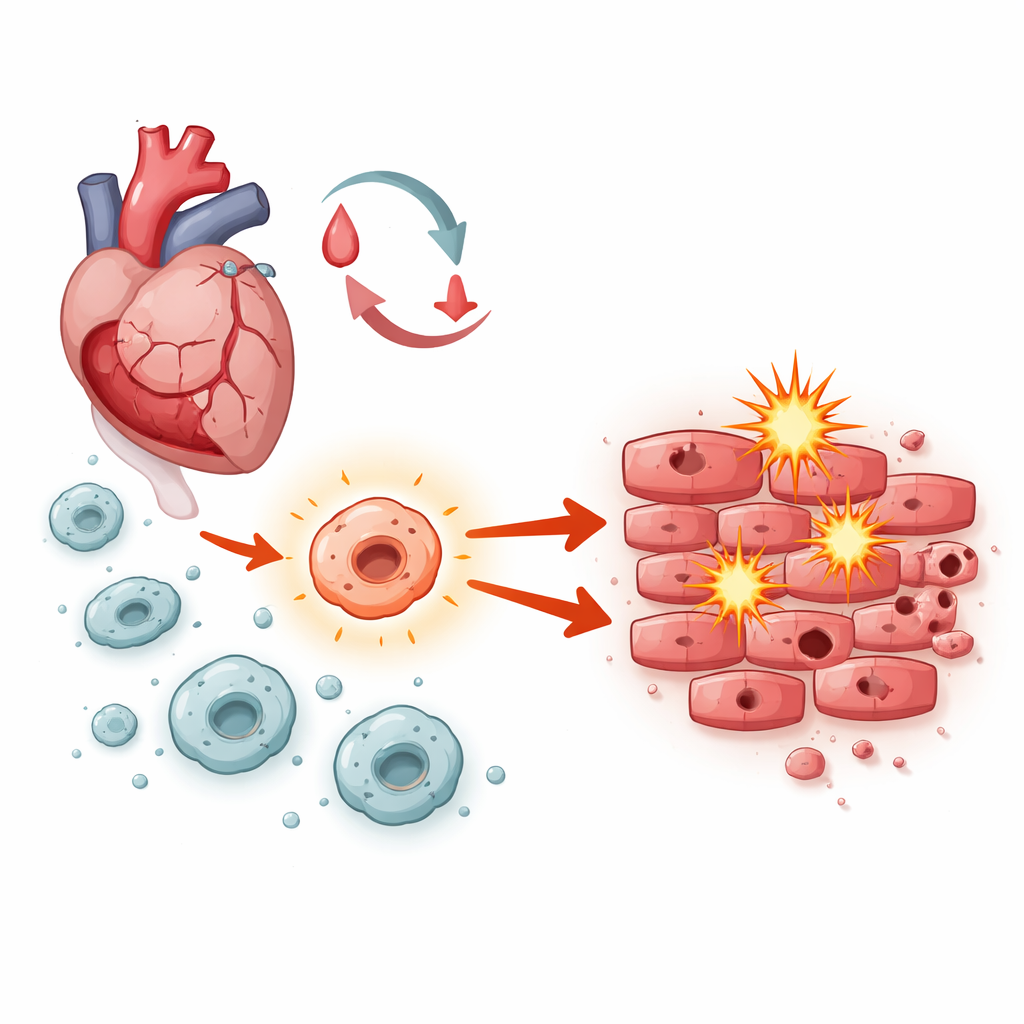
الصراع الداخلي داخل قلب يتعافى
بعد استعادة تدفق الدم، تواجه خلايا عضلة القلب عاصفة من الضغوط: تغيرات مفاجئة في الأكسجين، انفجارات من جزيئات غير مستقرة، وموجات من الالتهاب. تلعب البالعات—خلايا مناعية في الخطوط الأولى تتدفق إلى النسيج المتضرر—دورًا محوريًا في تنظيم ما يحدث بعد ذلك. اعتمادًا على كيفية تنشيطها، يمكنها إما إزالة الحطام ودعم الإصلاح أو دفع التورم وموت الخلايا. ركز الباحثون على نظام إشارة داخل البالعات يعرف باسم نوترش‑1، متسائلين عمّا إذا كان يحسم هذا التوازن نحو الشفاء أم الضرر أثناء إصابة الإقفار‑إعادة التدفق.
الحفر في الجينات، الجرذان، وخلايا القلب
نقّب الفريق أولًا في مجموعة بيانات عامة لتعبير الجينات مأخوذة من أشخاص عانوا نوبات قلبية حادة. حدّدوا أكثر من 100 جين تغيرت نشاطها بشكل ملحوظ، خاصة في المسارات المرتبطة بالالتهاب وانتحار الخلايا. برزت الجينات المرتبطة بنُهُج نوترش، مما يوحي بأن هذا المسار كان نشطًا أثناء تلف القلب. انتقل العلماء بعد ذلك إلى تجارب على جرذان، حيث أغلقوا مؤقتًا ثم أعادوا فتح شريان قلبي لمحاكاة ما يحدث للمرضى. زوّدوا الحيوانات بالبالعات المعدلة وراثيًا لتعزيز أو تعديل إشارة نوترش‑1، وفحصوا وظيفة الضخ القلبي بالموجات فوق الصوتية، وبنية النسيج تحت المجهر، ومدى النسيج الميت والخلايا المحتضرة.
كيف يقود مفتاح مناعي واحد الضرر
الجرذان التي تلقت بالعات ذات نشاط نوترش‑1 العالي كانت في حالة أسوأ: كانت قلوبها تضخ بكفاءة أقل، وأظهرت تفتتًا بنيويًا أكثر، واحتوت على مناطق أكبر من العضلة الميتة وخلايا أكثر موتًا. عبر إضافة أو حجب جزيئات أخرى بعناية، رسم الفريق سلسلة أحداث تالية لنوترش‑1 داخل البالعات. في هذه السلسلة، خفّض نوترش‑1 من نشاط منظم جيني يدعى EZH2، مما أتاح لبروتينات أخرى—من بينها BRD4 وHSF1 وSIRPα وSHP2—أن تصبح أكثر نشاطًا. معًا دفعت هذه الجزيئات البالعات إلى حالة التهابية عالية شجعت على الإفراط في إنتاج أنواع الأكسجين التفاعلية، وهي أشكال أكسجين كيميائية عدوانية يمكن أن تخترق أغشية الخلايا وتتلف الحمض النووي.
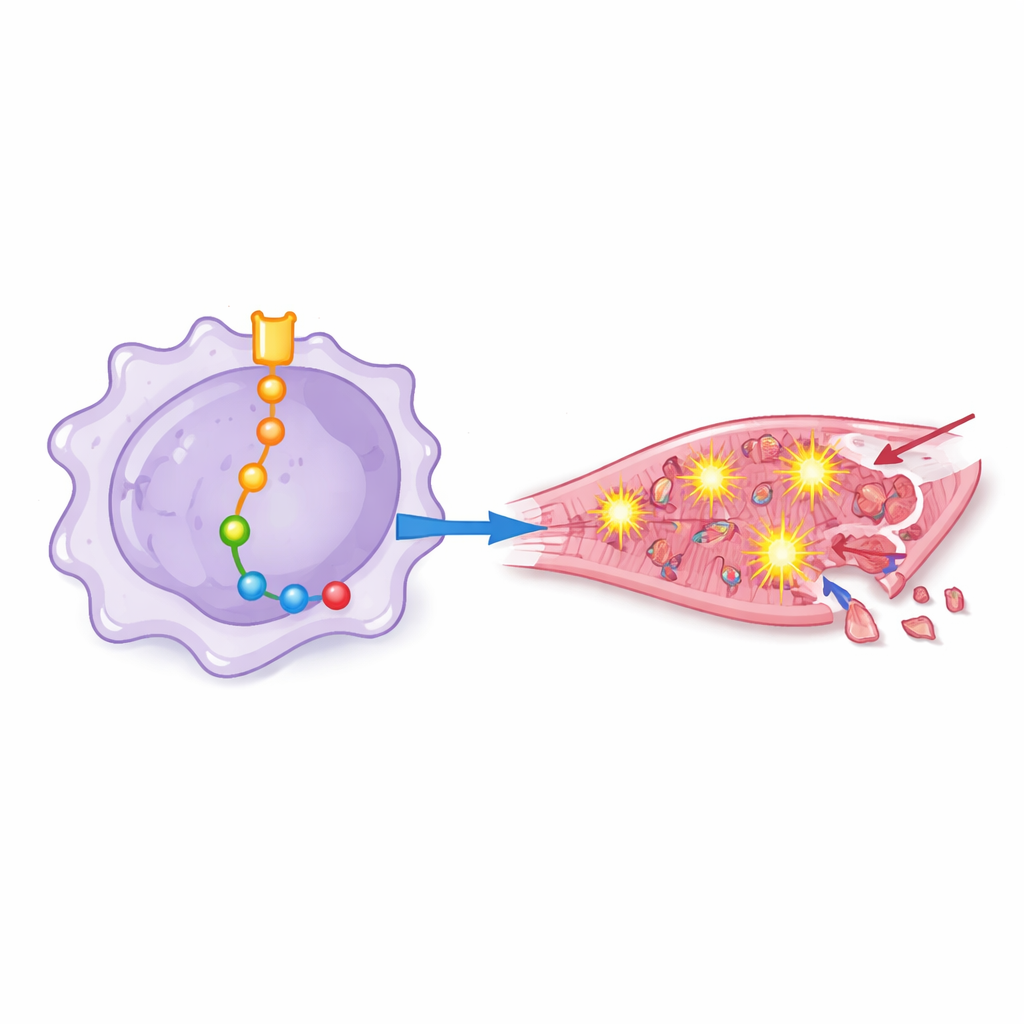
من الإجهاد الكيميائي إلى موت خلايا القلب
لمعرفة كيف تؤثر هذه البالعات «المهيأة» على خلايا قلب بشرية، حمَض الباحثون خلايا قلب نابذة في مزارع بمحلول مأخوذ من مزروعات بالعات مهندَسة بشكل مختلف. أدّت السوائل من بالعات ذات إشارة نوترش‑1 القوية إلى إجهاد تأكسدي أعلى، وتنشيط أكبر لمجمع بروتيني التهابي معروف بالإنفلامسوم، وارتفاع في مؤشرات الموت المبرمج. عندما حُجب نوترش‑1 أو بعض البروتينات التالية له، أظهرت خلايا القلب علامات أقل على التلف التأكسدي، حافظت على دفاعات مضادة للأكسدة أفضل، وكانت أقل عرضة للموت. دلّ هذا على أن التأثيرات الضارة ليست مجرد تحولات جزيئية نظرية بل تتحول مباشرة إلى فقدان خلايا القلب.
ماذا يعني هذا لرعاية القلب مستقبلًا
بعبارة مبسطة، تكشف الدراسة أن مفتاح إشارة يُدعى نوترش‑1 داخل البالعات يمكن أن يدفعها إلى وضع ضار خلال النافذة الحرجة عندما يعود تدفق الدم إلى القلب. عبر تتابع جزيئي متعدد المراحل يشمل EZH2 وHSF1 وBRD4 وSIRPα وSHP2، تغمر هذه الخلايا عضلة القلب المجاورة بجزيئات أكسجين مدمرة وإشارات تحفز الانتحار الخلوي، مما يكبر حجم الإصابة. ومع أن العمل أُجري في خلايا وحيوانات، فإنه يبرز أهدافًا جديدة للأدوية المصممة لتهدئة البالعات المفرطة النشاط والحد من الأضرار الجانبية عند إعادة فتح شريان مسدود—مما قد يساعد المرضى مستقبلًا على الاحتفاظ بمزيد من أنسجة القلب حية بعد النوبة القلبية.
الاستشهاد: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
الكلمات المفتاحية: إقفار‑إعادة تدفق عضلة القلب, البالعات, إشارة نوترش‑1, الإجهاد التأكسدي, موت خلايا القلب المبرمج