Clear Sky Science · sv
Notch-1 i makrofager främjade ischemia‑reperfusion genom att modulera EZH2/HSF1/BRD4/SIRPα/SHP2‑inducerad ROS och apoptos i kardiomyocyter
Varför hjärtåterställning ibland skadar hjärtat
När läkare öppnar en tilltäppt hjärtartär efter en hjärtinfarkt strömmar blodet tillbaka in i vävnad som varit utan syre. Denna räddning, kallad reperfusion, räddar liv – men kan också skada hjärtat ytterligare. Denna studie undersöker varför kroppens egna immunceller, som är tänkta att hjälpa till med läkning, ibland istället förvärrar denna "reperfusionsskada" och pekar på molekylära omkopplare som kan riktas för att skydda hjärtat i framtida behandlingar.
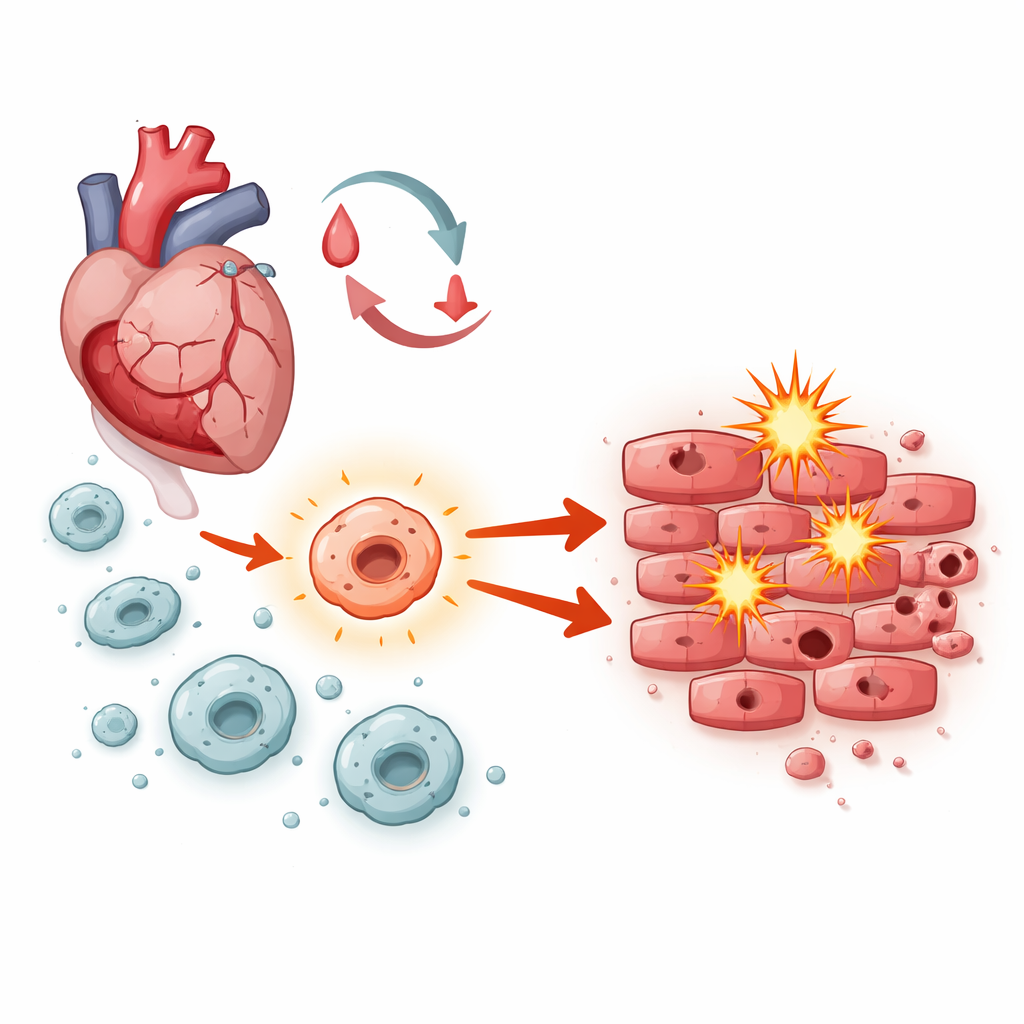
Dra‑kampen inne i ett läkande hjärta
När blodflödet återställs möter hjärtmuskelceller en storm av påfrestningar: plötsliga förändringar i syretillgång, utbrott av instabila molekyler och vågor av inflammation. Makrofager — frontlinjens immunceller som snabbt strömmar in i skadad vävnad — spelar en central roll i att orkestrera vad som händer härnäst. Beroende på hur de aktiveras kan de antingen hjälpa till att rensa upp skräp och stödja reparation eller driva svullnad och celldöd. Forskarna fokuserade på ett signalsystem inne i makrofager känt som Notch‑1 och undrade om det tippar balansen mot läkning eller skada under ischemia‑reperfusionsskada.
Grävande i gener, råttor och hjärtceller
Teamet började med att analysera ett öppet dataset för genuttryck från personer som drabbats av akut hjärtinfarkt. De identifierade mer än 100 gener vars aktivitet ändrades markant, särskilt i vägar kopplade till inflammation och cell självmord. Notch‑relaterade gener stack ut och antydde att denna väg var aktiv under hjärtskada. Forskarna gick sedan över till råttor och blockerade tillfälligt en hjärtartär för att sedan åter öppna den, för att efterlikna vad som händer hos patienter. De tillsatte makrofager som var genmodifierade för att förstärka eller förändra Notch‑1‑signalering och undersökte hjärtats pumpfunktion med ultraljud, vävnadsstruktur i mikroskop och omfattningen av död vävnad och döende celler.
Hur en immunomkopplare driver skada
Råttor som fick makrofager med hög Notch‑1‑aktivitet klarade sig sämre: deras hjärtan pumpade mindre effektivt, visade mer strukturell oordning och innehöll större områden med död muskel och fler döende celler. Genom att noggrant tillsätta eller blockera andra molekyler kartlade teamet en kedja av händelser nedströms Notch‑1 inne i makrofagerna. I denna kedja dämpade Notch‑1 en genreglerare kallad EZH2, vilket i sin tur frigjorde andra proteiner — inklusive BRD4, HSF1, SIRPα och SHP2 — att bli mer aktiva. Tillsammans drev dessa molekyler makrofager in i ett starkt inflammatoriskt tillstånd som uppmuntrade överproduktion av reaktiva syrearter, de kemiskt aggressiva formerna av syre som kan slå hål på cellmembran och skada DNA.
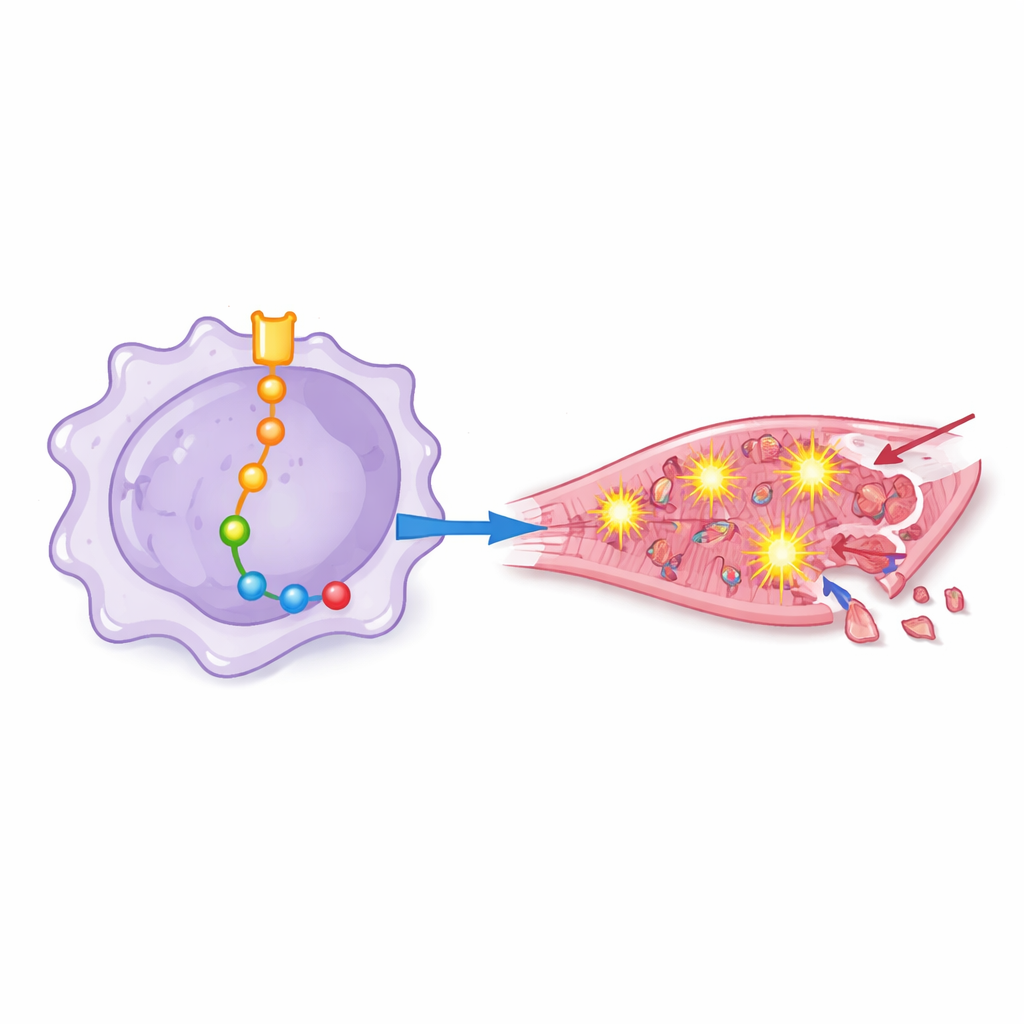
Från kemisk stress till hjärtcellernas död
För att se hur dessa "primade" makrofager påverkar mänskliga hjärtceller badade forskarna odlade kardiomyocyter i vätska hämtad från olika genmodifierade makrofagkulturer. Vätska från makrofager med stark Notch‑1‑signalering gav upphov till högre oxidativ stress, mer aktivering av ett inflammatoriskt proteinkomplex känt som inflammasomen, och en våg av markörer för programmerad celldöd. När Notch‑1 eller vissa nedströmsproteiner blockerades visade hjärtcellerna färre tecken på oxidativ skada, bättre bevarade antioxidativa försvar och var mindre benägna att dö. Detta visade att de skadliga effekterna inte bara är abstrakta molekylära förändringar utan direkt översätts till förlust av hjärtceller.
Vad detta betyder för framtidens hjärtvård
Enkelt uttryckt visar studien att en signalomkopplare kallad Notch‑1 inne i makrofager kan driva dem mot ett skadligt läge under det kritiska fönstret när blodflödet återkommer till hjärtat. Genom en flerstegs molekylär kedja involverande EZH2, HSF1, BRD4, SIRPα och SHP2 översvämmar dessa celler närliggande hjärtmuskel med destruktiva syremolekyler och signaler som utlöser celldöd, vilket förstorar skadan. Trots att arbetet utförts i celler och djur framhäver det nya mål för läkemedel utformade för att lugna överaktiva makrofager och begränsa kollaterala skador när en blockerad artär öppnas igen – vilket potentiellt kan hjälpa framtida patienter att behålla mer av sin hjärtmuskel efter en hjärtinfarkt.
Citering: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
Nyckelord: myokardiell ischemia‑reperfusion, makrofager, Notch‑1‑signalering, oxidativ stress, kardiomyocytapoptos