Clear Sky Science · ja
マクロファージ内Notch-1はEZH2/HSF1/BRD4/SIRPα/SHP2を介したROSと心筋細胞アポトーシスの誘導によって虚血再灌流障害を促進した
なぜ心修復が時に心臓を傷つけるのか
心臓発作の後に閉塞した冠動脈を再開通させると、飢餓状態にあった組織に血液が一気に流れ込む。この再灌流は命を救う処置だが、同時に心臓にさらなる損傷を与えることがある。本研究は、本来は治癒を助けるはずの免疫細胞がいかにしてこの「再灌流障害」を悪化させるのかを探り、将来の治療で心臓を保護するために切り替えられる可能性のある分子スイッチを指し示す。
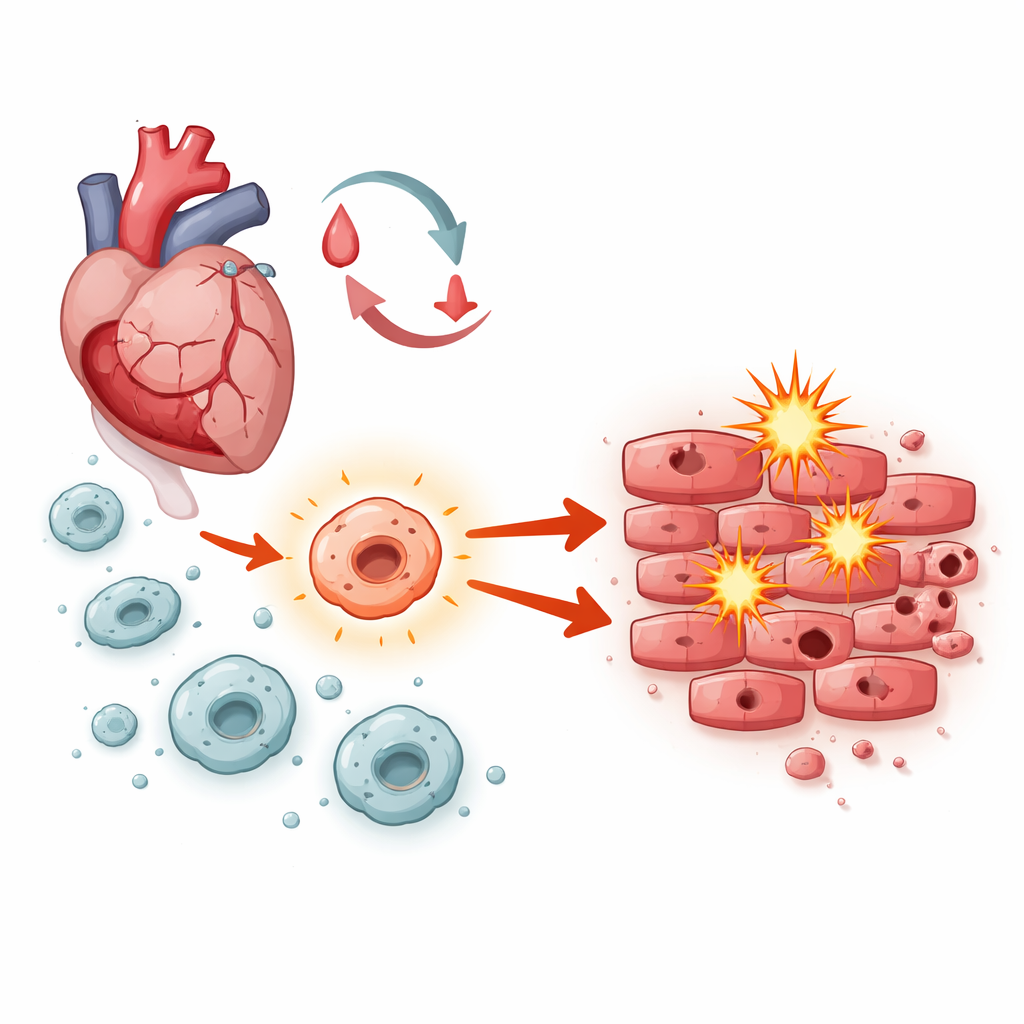
修復中の心臓内での綱引き
血流が回復すると、心筋細胞は酸素の急変、反応性の高い分子の発生、そして炎症の波に直面する。損傷組織に急行する先鋒の免疫細胞であるマクロファージは、その後の展開を指揮する中心的存在だ。活性化のされ方によって、彼らは破片の除去と修復を助けるか、あるいは腫脹や細胞死を促進するかのいずれかになる。本研究では、マクロファージ内のNotch‑1として知られるシグナル系に着目し、虚血再灌流傷害時に治癒寄りか有害寄りかの天秤をどちらに傾けるかを問うた。
遺伝子解析、ラット、心筋細胞の掘り下げ
研究チームはまず、心筋梗塞を経験した患者の公的遺伝子発現データセットを解析した。炎症や細胞死に関連する経路で特に顕著に変化した100以上の遺伝子を同定した。Notch関連遺伝子が際立っており、この経路が心損傷時に活性化していることを示唆した。次に研究者らはラットを用いて、患者で起こる現象を模した冠動脈の一時閉塞と再開通を行った。Notch‑1シグナルを増強または改変するよう操作したマクロファージを注入し、超音波で心機能を評価し、顕微鏡で組織構造を観察し、壊死領域や死にゆく細胞の程度を調べた。
一つの免疫スイッチが損傷を駆動する仕組み
Notch‑1活性の高いマクロファージを受けたラットはより悪化した。心拍出能が低下し、組織の乱れが大きく、壊死領域や死細胞の範囲が拡大していた。研究者らは他の分子を丁寧に付加・阻害することで、マクロファージ内のNotch‑1から始まる事象の連鎖を描いた。その連鎖では、Notch‑1がEZH2という遺伝子調節因子を抑制し、結果としてBRD4、HSF1、SIRPα、SHP2などの他のタンパク質がより活性化されるようになった。これらの分子が協働してマクロファージを強い炎症状態へと駆り立て、細胞膜に穴を開けたりDNAを損傷したりする化学的に攻撃的な酸素種(ROS)の過剰産生を助長した。
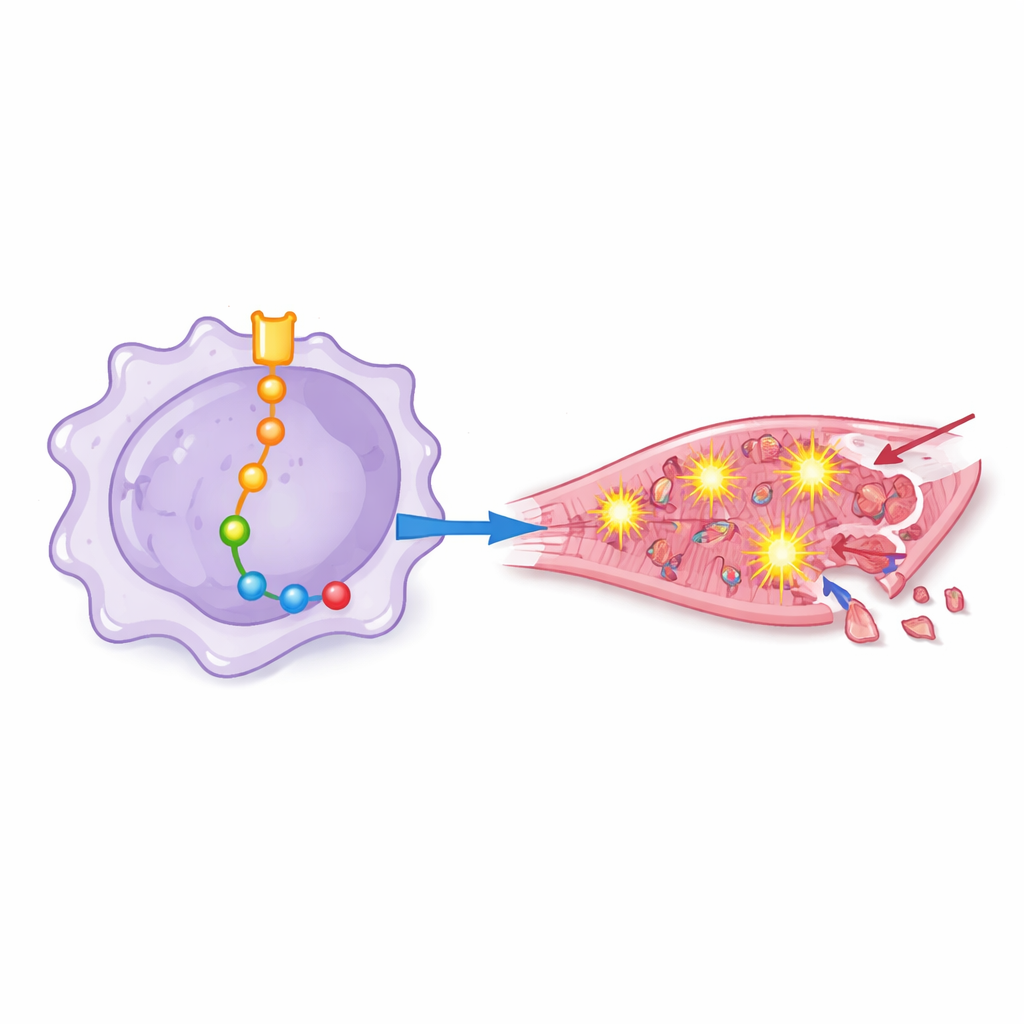
化学的ストレスから心筋細胞死へ
これらの「賦活された」マクロファージがヒト心筋細胞にどのように影響するかを確かめるため、研究者らは培養心筋細胞を異なる操作を施したマクロファージ培養液で処理した。Notch‑1シグナルが強いマクロファージの培養上清は、より高い酸化ストレス、インフラマソームと呼ばれる炎症性タンパク質複合体の活性化、そしてプログラム細胞死のマーカーの急増を引き起こした。Notch‑1や特定の下流タンパク質が阻害されると、心筋細胞は酸化的損傷の兆候が減り、抗酸化防御をより維持し、死に至る割合が低下した。これは、損傷効果が抽象的な分子変化にとどまらず、直接的に心筋細胞の喪失につながることを示している。
将来の心臓治療への示唆
簡潔に言えば、本研究はマクロファージ内のNotch‑1というシグナルスイッチが、血流が心臓に戻る重要な時期にこれらの細胞を有害なモードへ押しやる可能性を示した。EZH2、HSF1、BRD4、SIRPα、SHP2を含む多段階の分子リレーを介して、これらの細胞は近傍の心筋に破壊的な酸素種や細胞死を誘導する信号を送り、損傷を拡大させる。研究は細胞と動物で行われたものだが、過剰に活性化したマクロファージを鎮め、閉塞血管の再開通時に生じる付随的損傷を抑えることを目的とした薬剤の新たな標的を示しており、将来の患者が心筋をより多く残せる可能性を示唆している。
引用: Tong, C., Zhang, J., Zuo, Y. et al. Notch-1 in macrophages promoted the ischemia-reperfusion via modulating EZH2/HSF1/BRD4/SIRPα/SHP2 induced ROS and apoptosis in cardiomyocyte. Sci Rep 16, 11020 (2026). https://doi.org/10.1038/s41598-026-40683-4
キーワード: 心筋虚血再灌流, マクロファージ, Notch-1シグナル伝達, 酸化ストレス, 心筋細胞アポトーシス