Clear Sky Science · zh
钙依赖性激活的TMEM16F扰动酶与离子通道
为何这个微小的膜阀重要
每一秒,我们细胞周围的膜都在悄然移动分子以维持生命平衡。在这场平衡动作中,一种名为TMEM16F的蛋白质是并不显眼但不可或缺的参与者。它参与止血、修复撕裂的膜、引导大脑免疫细胞,甚至会被像SARS‑CoV‑2这样的病毒劫持以感染细胞。然而,直到现在,科学家们尚未弄清这种蛋白如何开启与关闭,或如何既能充当离子通道,又能作为将脂质在膜两侧翻转的“扰位酶”。本研究结合高分辨率成像与计算模拟,前所未有地揭示了TMEM16F的工作构象与运动。
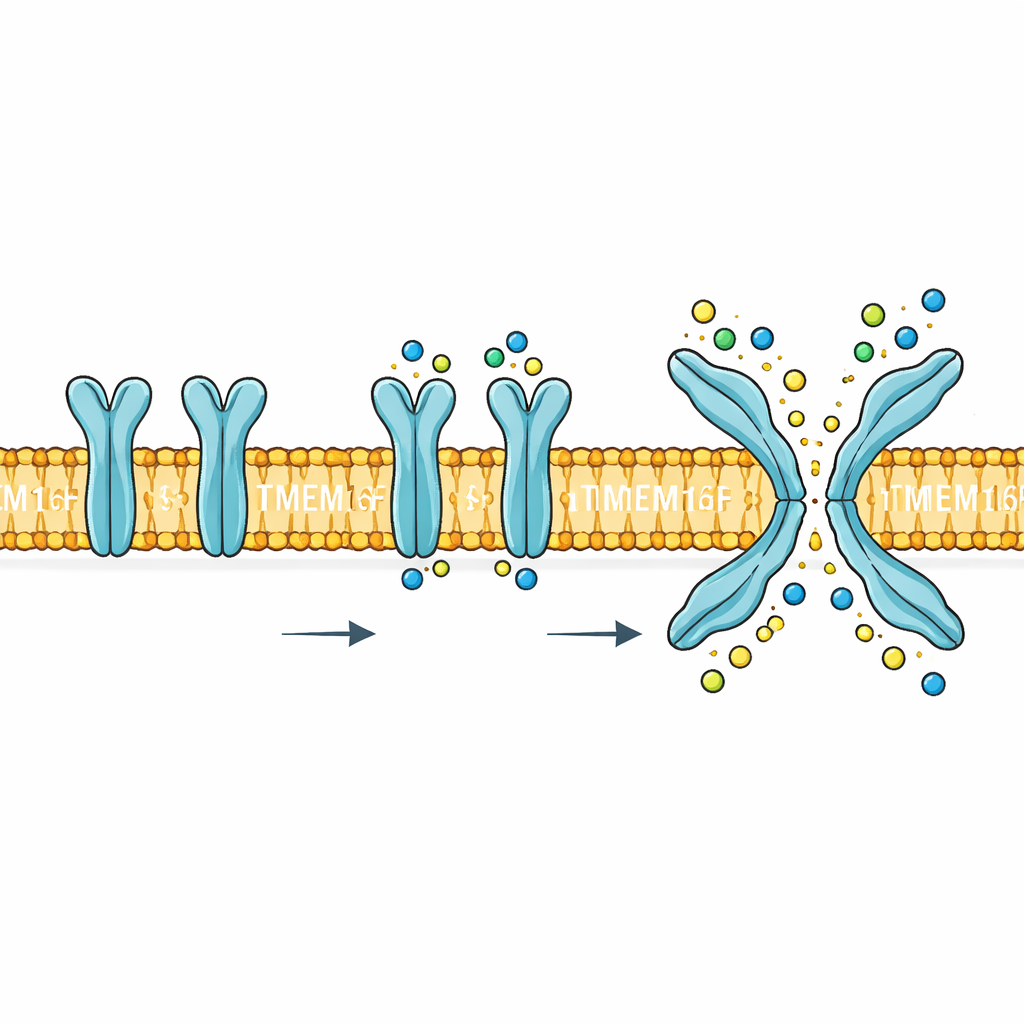
位于细胞边界的双重阀门
TMEM16F位于细胞外膜,响应细胞内钙浓度的升高。被激活时,它执行两项截然不同的任务。其一,它形成一条通路,允许诸如钠、钾和氯等小带电粒子穿过膜。其二,它将某些脂质,尤其是磷脂酰丝氨酸,从膜的内侧面翻到外侧面。这种脂质翻转是强有力的生物学信号:它帮助血小板形成血栓、标记受损细胞以便清除,并可能被病毒利用来进入细胞。TMEM16F的突变或调控紊乱与血液、骨骼和神经系统疾病有关,使其机制不仅是学术趣味,而是一个潜在的药物靶点。
在天然环境中观察蛋白
先前的结构研究在表面活性剂或纳米盘等人工环境中考察TMEM16F,并在有钙存在时仍多次观测到其看似闭合的状态。这带来了一个难题:功能实验明确显示蛋白是活性的,但结构上似乎不存在离子或脂质通道。为了解决这个问题,作者将小鼠TMEM16F重建到由简单、定义明确的脂质组成的微小自由漂浮膜泡(脂质体)中——这种环境能够直接测量离子流动和脂质扰位。随后,他们使用低温电镜捕获了数百万张蛋白质快照,并将这些图像分类为代表不同活性状态的独立构象。
钙如何重塑阀门
在无钙条件下,TMEM16F呈现两种相似的非活性构象,其间穿过蛋白的重要沟槽紧密封闭。加入钙后,蛋白既有一种常见的钙结合但仍闭合的构象,也出现一种较为罕见但显著不同的构象。在这种活性状态中,一段称为TM4的蛋白片段相对于邻近的TM6滑动,形成一个交叉状(X形)的沟槽穿过膜。该沟槽的中央部分构成了一个连续的、由蛋白壁围成的孔,足够宽以容纳部分水化的离子,而靠近膜表面的区域则开放为更宽的前庭。研究者通过工程化突变验证了这种构象的重要性:那些使蛋白更偏向X形构象的突变使扰位更易发生,而将其困在闭合形式的突变几乎完全消除了活性。
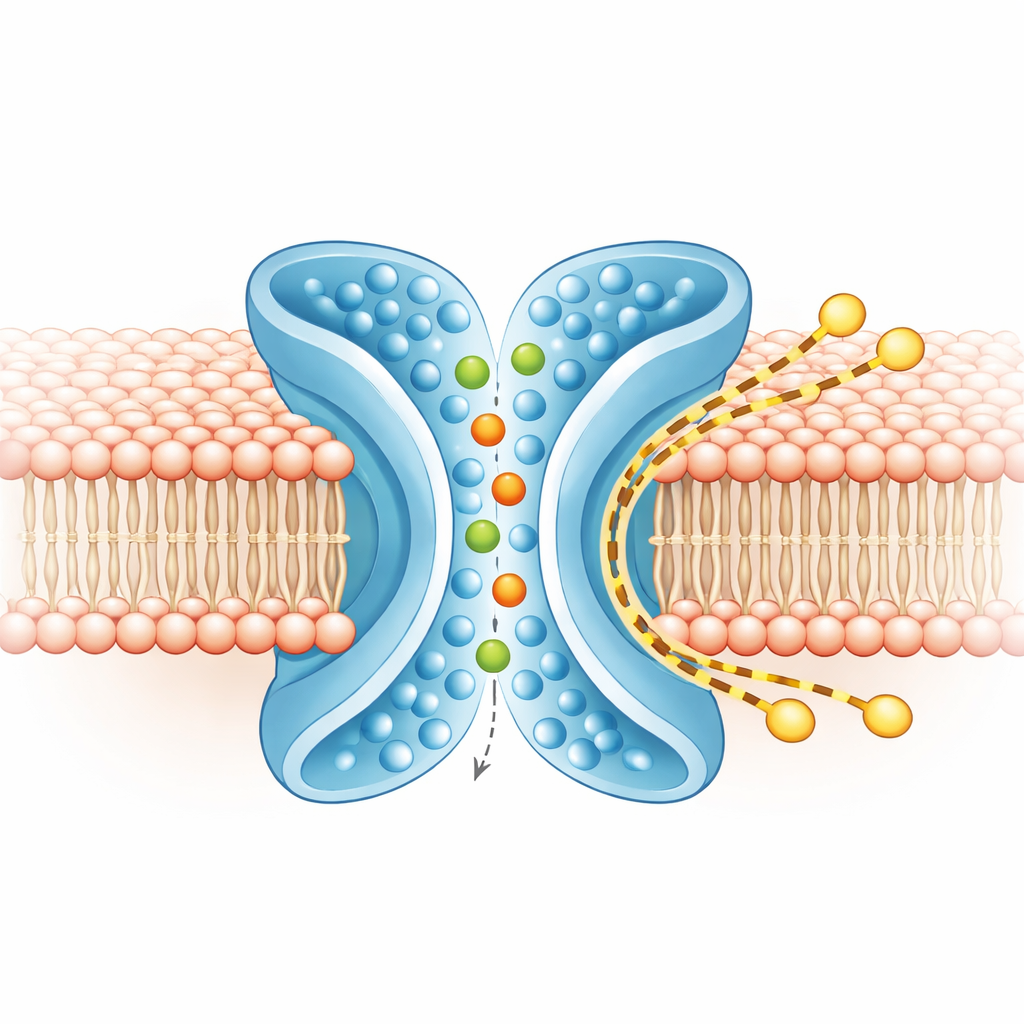
离子与脂质的分离通道
为了弄清什么沿着哪条路径移动,团队在真实膜环境中对TMEM16F的闭合与活性构象进行了大规模计算模拟。在活性X形构象中,离子沿着中央孔穿行,从任一侧进入,并保持大部分周围的水化层,这与该蛋白在正负离子间不强烈区分的特性一致。与此同时,围绕TM4和TM6的外层膜变薄并弯曲。较粗粒度的长期模拟显示,数百个脂质分子沿着X形沟槽的外侧从一层穿过到另一层,基本绕开了离子孔。离子与脂质的路线只有极少重叠,表明该蛋白并非共享单一混合通道,而是在并列位置运行两条大致独立的通路:内侧用于离子,外侧用于脂质。
与细胞信号相连的可塑控制器
研究还揭示了蛋白的内侧胞质域如何像机械连杆一样将钙结合转换为这些大型构象变化。在静息状态下,该域形成由特定氨基酸之间的静电“锁”网络维持的紧凑结构。钙结合使TM6片段变直并推动该胞质域;破坏这些盐桥锁则使该域的一部分向上旋转并扣住TM6。这一运动传递到TM4–TM5区,导致TM4滑动并形成X形沟槽。削弱这些“锁”的突变会加速扰位,而有利于闭合状态的突变则会减慢或阻断其功能。
对健康与疾病的意义
通俗地说,这项工作表明TMEM16F是一台由钙控制的微型机械,能够同时为离子打开一条内孔,并塑造周围膜以便脂质穿过。离子与脂质并不是通过一个混合通道分担通道,而是主要沿着由相同蛋白运动塑造的独立路径行进。通过揭示钙结合、内部重排与膜弯曲如何协同工作,本研究为理解与TMEM16F相关的疾病提供了蓝图,并为设计可精细调节其在止血、膜修复与病毒感染中活性的药物奠定了基础。
引用: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
关键词: TMEM16F, 脂质扰位, 离子通道, 细胞膜, 钙信号