Clear Sky Science · it
Attivazione dipendente dal calcio della scramblasi e canale ionico TMEM16F
Perché questa piccola valvola di membrana è importante
Ogni secondo, le membrane intorno alle nostre cellule spostano silenziosamente molecole per mantenerci in vita. Uno dei protagonisti meno celebrati di questo equilibrio è una proteina chiamata TMEM16F. Contribuisce alla coagulazione del sangue, ripara membrane lacerate, guida le cellule immunitarie del cervello e viene persino sfruttata da virus come SARS‑CoV‑2 per infettare le cellule. Eppure, fino ad ora, gli scienziati non comprendevano come questa proteina si attivi e si disattivi, né come possa funzionare sia come canale ionico sia come “scramblasi” di lipidi che capovolge le molecole lipidiche tra i due lati della membrana. Questo studio utilizza immagini ad alta risoluzione e simulazioni al computer per rivelare i movimenti funzionali di TMEM16F con dettagli senza precedenti.
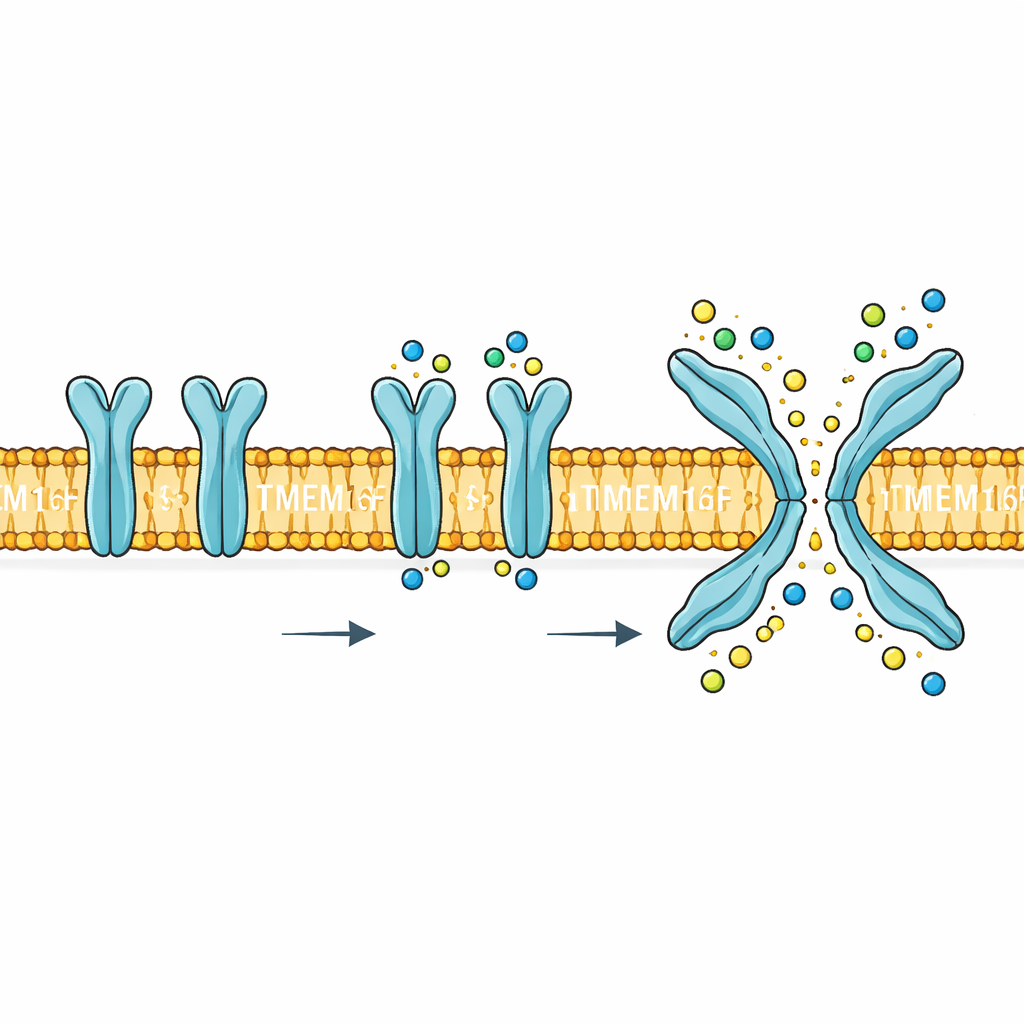
Un cancello con doppia funzione al confine cellulare
TMEM16F è inserito nella membrana esterna della cellula e risponde agli aumenti di calcio all’interno della cellula. Quando si attiva, svolge due compiti molto diversi. Innanzitutto, forma un percorso che permette a piccole particelle cariche come sodio, potassio e cloruro di attraversare la membrana. In secondo luogo, capovolge certi lipidi, in particolare la fosfatidilserina, dalla faccia interna a quella esterna della membrana. Questo spostamento di lipidi è un potente segnale biologico: favorisce la formazione del coagulo da parte delle piastrine, segnala le cellule danneggiate per la rimozione e può essere sfruttato dai virus per entrare nelle cellule. Mutazioni o una regolazione scorretta di TMEM16F sono associate a problemi del sangue, delle ossa e del sistema nervoso, rendendo il suo meccanismo più di una curiosità—è un potenziale bersaglio farmacologico.
Osservare la proteina nel suo habitat nativo
Studi strutturali precedenti hanno esaminato TMEM16F in ambienti artificiali come detergenti o nanodischi e lo hanno visto in modo coerente in quello che sembrava uno stato chiuso, anche quando il calcio era presente. Questo ha sollevato un enigma: esperimenti funzionali mostravano chiaramente che la proteina era attiva, ma la sua struttura non sembrava aprire una via per ioni o lipidi. Per risolvere il problema, gli autori hanno ricostituito la TMEM16F murina in piccole bolle di membrana libere (liposomi) composte da lipidi semplici e ben definiti—lo stesso tipo di ambiente in cui potevano misurare direttamente il movimento degli ioni e il rimodellamento dei lipidi. Hanno quindi utilizzato la criomicroscopia elettronica per catturare milioni di istantanee della proteina e le hanno classificate in forme distinte che rappresentano diversi stati di attività.
Come il calcio rimodella il cancello
In assenza di calcio, TMEM16F assumeva due forme inattive simili in cui una scanalatura chiave attraverso la proteina era saldamente sigillata. Quando è stato aggiunto il calcio, la proteina ha favorito una forma convenzionale legata al calcio ma ancora chiusa, e una seconda forma, più rara ma sorprendentemente diversa. In questo stato attivo, un segmento della proteina chiamato TM4 scivolava rispetto a un segmento vicino, TM6, creando una scanalatura a forma di X che attraversava la membrana. La parte centrale di questa scanalatura formava un poro continuo, delimitato dalla proteina, sufficientemente largo da permettere il passaggio di ioni parzialmente idratati, mentre le regioni più vicine alle superfici della membrana si aprivano in vestiboli più ampi. I ricercatori hanno confermato l’importanza di questa conformazione ingegnerizzando mutazioni: quelle che spostavano la proteina verso lo stato a forma di X facilitavano il rimodellamento lipidico, mentre quelle che la intrappolavano nella forma chiusa quasi abolivano l’attività.
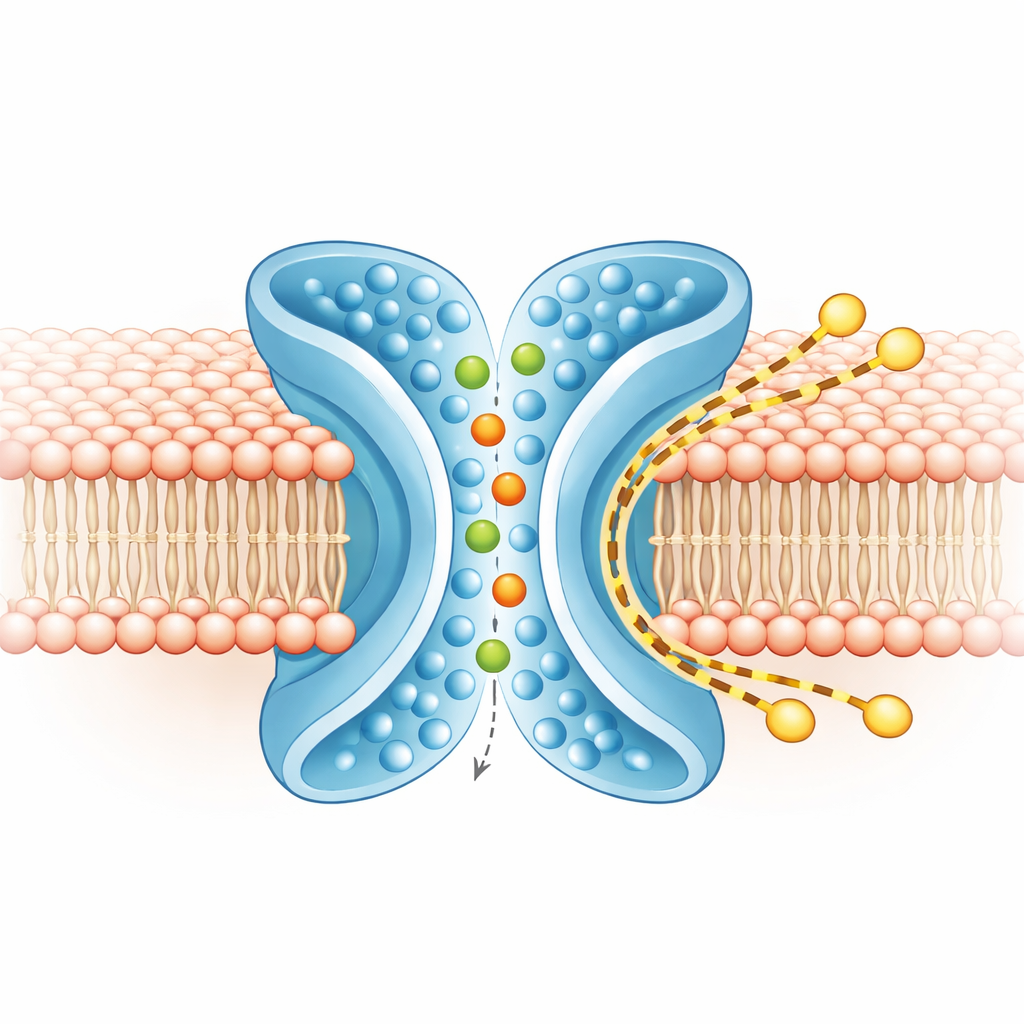
Percorsi separati per ioni e lipidi
Per capire cosa si muoveva e dove, il gruppo ha eseguito estese simulazioni al computer di TMEM16F in una membrana realistica, sia nelle conformazioni chiusa sia attiva. Nella forma attiva a X, gli ioni serpeggiavano attraverso il poro centrale, entrando da entrambi i lati e mantenendo gran parte della loro guaina d’acqua circostante, coerente con la preferenza debole della proteina tra ioni positivi e negativi. Contemporaneamente, lo strato esterno della membrana attorno a TM4 e TM6 si assottigliava e si incurvava. Simulazioni a grana grossa, eseguite per tempi più lunghi, hanno mostrato centinaia di molecole lipidiche che passavano da un foglietto all’altro lungo l’esterno della scanalatura a X, evitando in gran parte il poro ionico. I percorsi di ioni e lipidi si sovrapponevano solo minimamente, indicando che la proteina gestisce due percorsi per lo più indipendenti affiancati: uno interno per gli ioni e uno esterno per i lipidi.
Un regolatore flessibile legato ai segnali cellulari
Lo studio svela inoltre come il dominio interno citosolico della proteina funzioni come un collegamento meccanico che converte il legame del calcio in questi ampi movimenti. Nello stato di riposo, questo dominio forma una struttura compatta tenuta insieme da una rete di “chiavistelli” elettrostatici tra aminoacidi specifici. Il legame del calcio raddrizza il segmento TM6 e spinge questo dominio; la rottura dei ponti salini permette a una parte del dominio di ruotare verso l’alto e agganciarsi a TM6. Questo movimento viene trasmesso alla regione TM4–TM5, causando lo scivolamento di TM4 e la formazione della scanalatura a X. Mutazioni che indeboliscono il chiavistello accelerano il rimodellamento, mentre quelle che favoriscono lo stato chiuso lo rallentano o lo bloccano.
Cosa significa per la salute e la malattia
In termini pratici, questo lavoro mostra che TMEM16F è una piccola macchina controllata dal calcio che può contemporaneamente aprire un condotto interno per gli ioni e rimodellare la membrana circostante in modo che i lipidi la attraversino. Piuttosto che condividere un unico percorso misto, ioni e lipidi viaggiano per lo più su tracce separate modellate dallo stesso movimento proteico. Rivelando come il legame del calcio, le riorganizzazioni interne e la curvatura della membrana cooperino, lo studio fornisce un progetto per comprendere le malattie legate a TMEM16F e per ideare farmaci in grado di modulare finemente la sua attività nella coagulazione, nella riparazione della membrana e nelle infezioni virali.
Citazione: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Parole chiave: TMEM16F, rimodellamento dei lipidi, canali ionici, membrana cellulare, segnalazione del calcio