Clear Sky Science · nl
Calciumafhankelijke activatie van de TMEM16F-scramblase en ionenkanaal
Waarom dit kleine membraanklepje ertoe doet
Elke seconde schuiven de membranen rond onze cellen stilletjes moleculen heen en weer om ons in leven te houden. Een onvermoede speler in dit evenwicht is een eiwit dat TMEM16F heet. Het helpt bij bloedstolling, herstelt gescheurde membranen, stuurt immuuncellen van de hersenen en wordt zelfs gekaapt door virussen zoals SARS‑CoV‑2 om cellen te infecteren. Toch begrepen wetenschappers tot nu toe niet hoe dit eiwit aan‑ en uitgezet wordt, of hoe het zowel als ionenkanaal kan functioneren als een lipiden “scrambler” die vetmoleculen tussen de twee zijden van het membraan omdraait. Deze studie gebruikt beelden met hoge resolutie en computersimulaties om TMEM16F’s werkbewegingen in ongekend detail te onthullen.
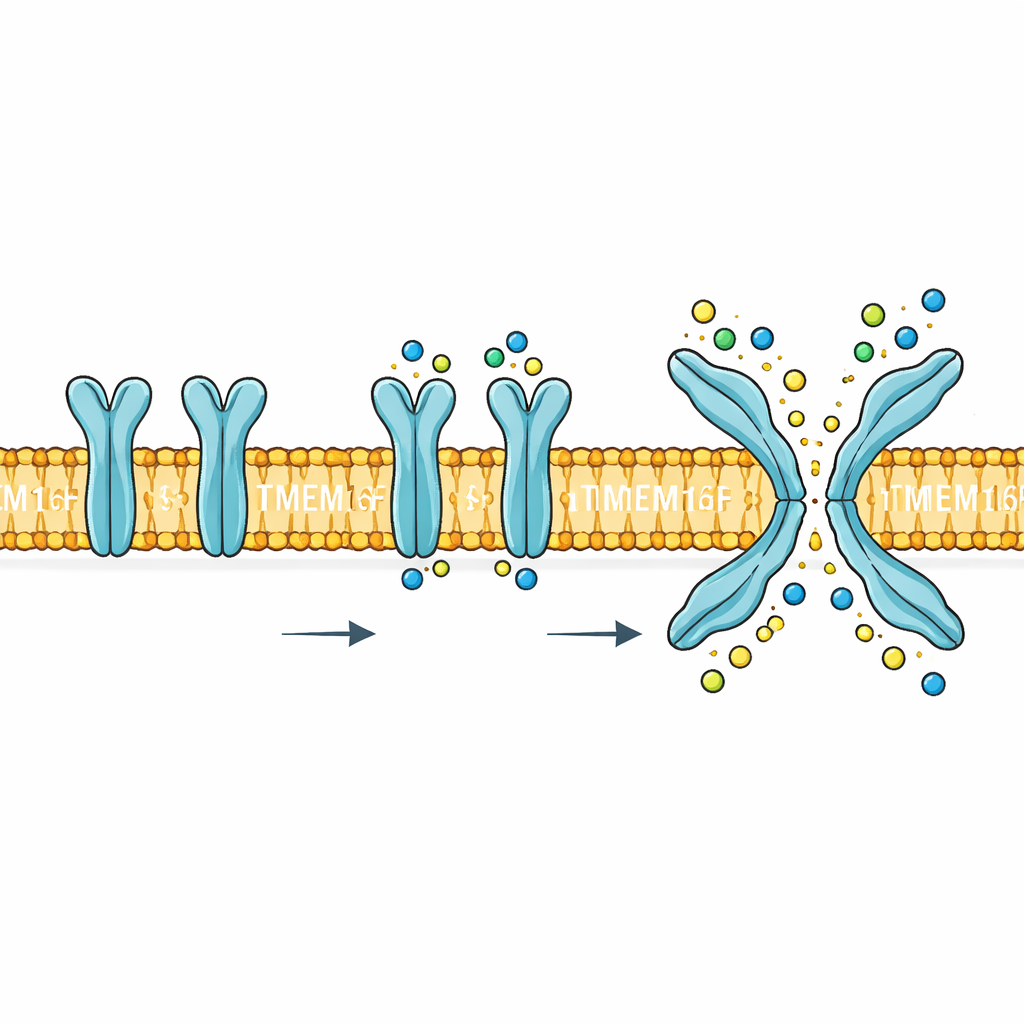
Een dubbeldoelige poort in de celgrens
TMEM16F bevindt zich in het buitenste membraan van de cel en reageert op stijgingen van calcium binnen de cel. Wanneer het geactiveerd wordt, vervult het twee heel verschillende taken. Ten eerste vormt het een doorgang die kleine geladen deeltjes zoals natrium, kalium en chloride door het membraan laat bewegen. Ten tweede draait het bepaalde lipiden, vooral fosfatidylserine, van de binnenzijde van het membraan naar de buitenzijde. Die lipide‑flip is een krachtig biologisch signaal: het helpt bloedplaatjes stolsels vormen, markeert beschadigde cellen voor opruiming en kan door virussen worden benut om cellen binnen te dringen. Mutaties of verkeerde regulatie van TMEM16F worden in verband gebracht met problemen in bloed, bot en zenuwstelsel, waardoor het mechanisme meer is dan een curiositeit—het is een potentieel geneesmiddeldoelwit.
Het eiwit zien in zijn natuurlijke omgeving
Eerdere structurele studies onderzochten TMEM16F in kunstmatige omgevingen zoals detergenten of nanodiscs en zagen het consequent in wat leek op een gesloten staat, zelfs wanneer calcium aanwezig was. Dit riep een raadsel op: functionele experimenten toonden duidelijk aan dat het eiwit actief was, maar de structuur leek geen route voor ionen of lipiden te openen. Om dit te verduidelijken, brachten de auteurs muizen‑TMEM16F terug in kleine, vrij drijvende membraanblaasjes (liposomen) gemaakt van eenvoudige, goed gedefinieerde lipiden—dezelfde soort omgeving waarin ze direct ionbeweging en lipide‑scrambling konden meten. Vervolgens gebruikten ze cryo‑elektronenmicroscopie om miljoenen momentopnamen van het eiwit vast te leggen en sorteerden deze in uiteenlopende vormen die verschillende activiteitsstaten vertegenwoordigden.
Hoe calcium de poort hervormt
In afwezigheid van calcium nam TMEM16F twee vergelijkbare, inactieve vormen aan waarin een belangrijke groef door het eiwit strak was afgesloten. Toen calcium werd toegevoegd, bevoordeelde het eiwit een conventionele calciumgebonden maar nog steeds gesloten vorm, en een tweede, zeldzamere maar opvallend andere vorm. In deze actieve staat schoof een segment van het eiwit genaamd TM4 langs een aangrenzend segment TM6, waardoor een X‑vormige groef ontstond die het membraan kruiste. Het centrale deel van deze groef vormde een continue, door het eiwit omrande porie breed genoeg voor gedeeltelijk gehydrateerde ionen, terwijl de gebieden dichter bij de membraanfases opengingen naar bredere vestibules. De onderzoekers bevestigden het belang van deze conformatie door mutaties te ontwerpen: diegenen die het eiwit naar de X‑vormige staat verschoven maakten scrambling makkelijker, terwijl mutaties die het in de gesloten vorm vastzetten de activiteit vrijwel uitschakelden.
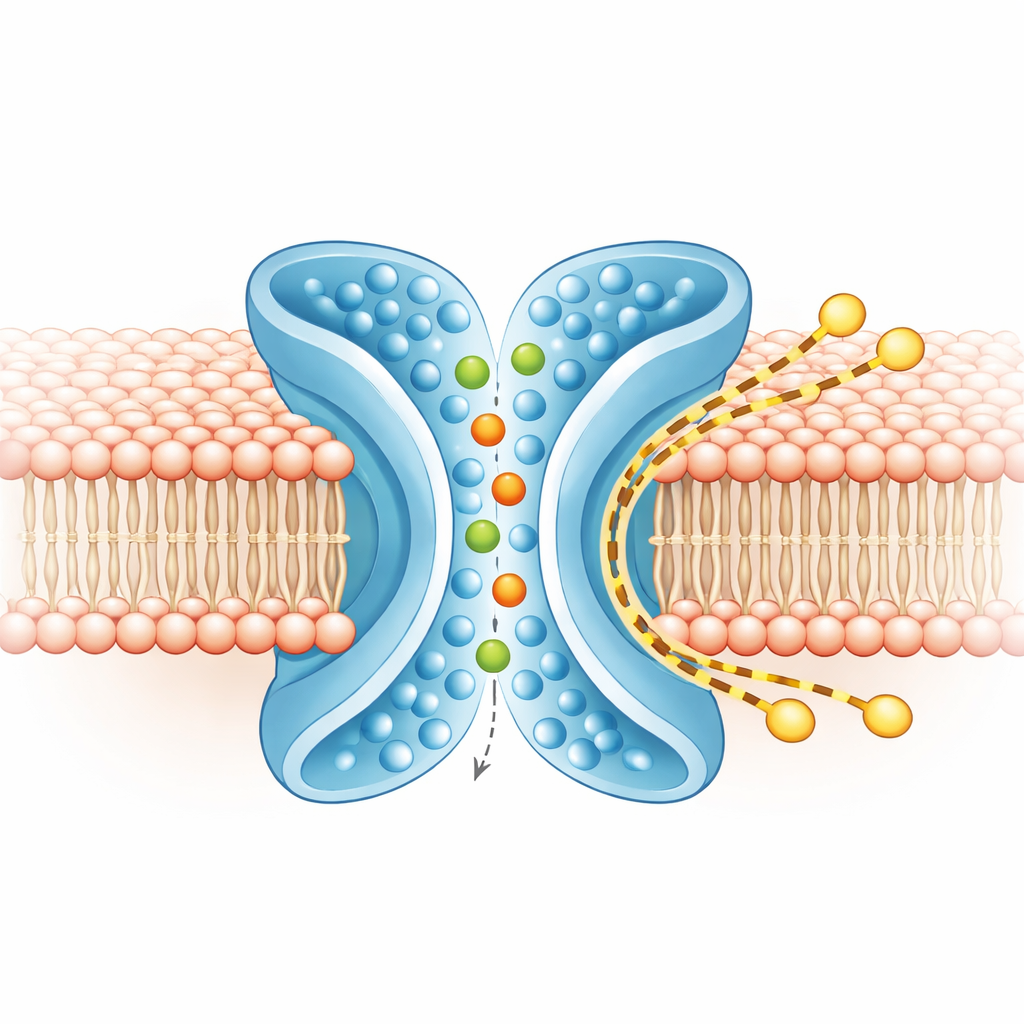
Gescheiden sporen voor ionen en lipiden
Om te begrijpen wat waarheen beweegt, voerde het team uitgebreide computersimulaties uit van TMEM16F in een realistisch membraan, zowel in de gesloten als in de actieve vormen. In de actieve, X‑vormige staat kronkelden ionen door de centrale porie, binnenkomend vanaf beide zijden en behielden daarbij het grootste deel van hun omringende waterschil, in overeenstemming met de losse voorkeur van het eiwit tussen positieve en negatieve ionen. Tegelijkertijd werd de buitenste laag van het membraan rond TM4 en TM6 dunner en boog deze. Grove‑grained simulaties, uitgevoerd voor langere tijden, toonden honderden lipidemoleculen die van het ene blaadje naar het andere trokken langs de buitenkant van de X‑vormige groef, grotendeels langs de ionenpoort heen. De routes van ionen en lipiden overlappen slechts minimaal, wat aangeeft dat het eiwit twee grotendeels onafhankelijke sporen naast elkaar beheert: een binnenste voor ionen en een buitenste voor lipiden.
Een flexibele schakelaar gekoppeld aan celsignalen
De studie onthult ook hoe de inwendige, cytosolische domein van het eiwit werkt als een mechanische koppeling die calciumbinding omzet in deze grote bewegingen. In de rusttoestand vormt dit domein een compacte structuur die bijeen wordt gehouden door een netwerk van elektrostatische “sloten” tussen specifieke aminozuren. Calciumbinding maakt het TM6‑segment rechter en duwt aan dit domein; het verbreken van de zoutbrug‑sloten laat een deel van het domein omhoog draaien en vastklikken op TM6. Die beweging wordt doorgegeven aan het TM4–TM5‑gebied, waardoor TM4 schuift en de X‑vormige groef vormt. Mutaties die het slot verzwakken versnellen scrambling, terwijl diegenen die de gesloten staat bevoordelen het proces vertragen of blokkeren.
Wat dit betekent voor gezondheid en ziekte
In gewone bewoordingen toont dit werk dat TMEM16F een klein, calciumgestuurd machientje is dat tegelijk een interne pijp voor ionen kan openen en het omliggende membraan zo vormt dat lipiden eroverheen glijden. In plaats van een gemengde gedeelde route, reizen ionen en lipiden grotendeels langs gescheiden sporen die door dezelfde eiwitbeweging worden gevormd. Door te onthullen hoe calciumbinding, interne herordening en membraangebogenheid samenwerken, biedt de studie een blauwdruk om ziekten die met TMEM16F samenhangen te begrijpen en om geneesmiddelen te ontwerpen die de activiteit ervan in bloedstolling, membraanherstel en virusinfecties fijn kunnen afstemmen.
Bronvermelding: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Trefwoorden: TMEM16F, lipid scrambling, ion channels, cell membrane, calcium signaling