Clear Sky Science · sv
Kalciumberoende aktivering av TMEM16F‑scramblasen och jonkanalen
Varför denna lilla membranventil är viktig
Varje sekund omorganiserar membranen kring våra celler tyst molekyler för att hålla oss vid liv. En osjungad aktör i detta balansspel är ett protein som kallas TMEM16F. Det hjälper blodet att koagulera, reparerar trasiga membran, styr immunceller i hjärnan och blir till och med kapat av virus som SARS‑CoV‑2 för att infektera celler. Ändå förstod forskare fram tills nu inte hur detta protein slås av och på, eller hur det kan fungera både som jonkanal och som en lipid‑”scrambler” som vänder fettmolekyler mellan membranets två sidor. Denna studie använder högupplöst avbildning och datorsimuleringar för att avslöja TMEM16F:s rörelser i detalj som aldrig förr.
En dubbelfunktionell port i cellgränsen
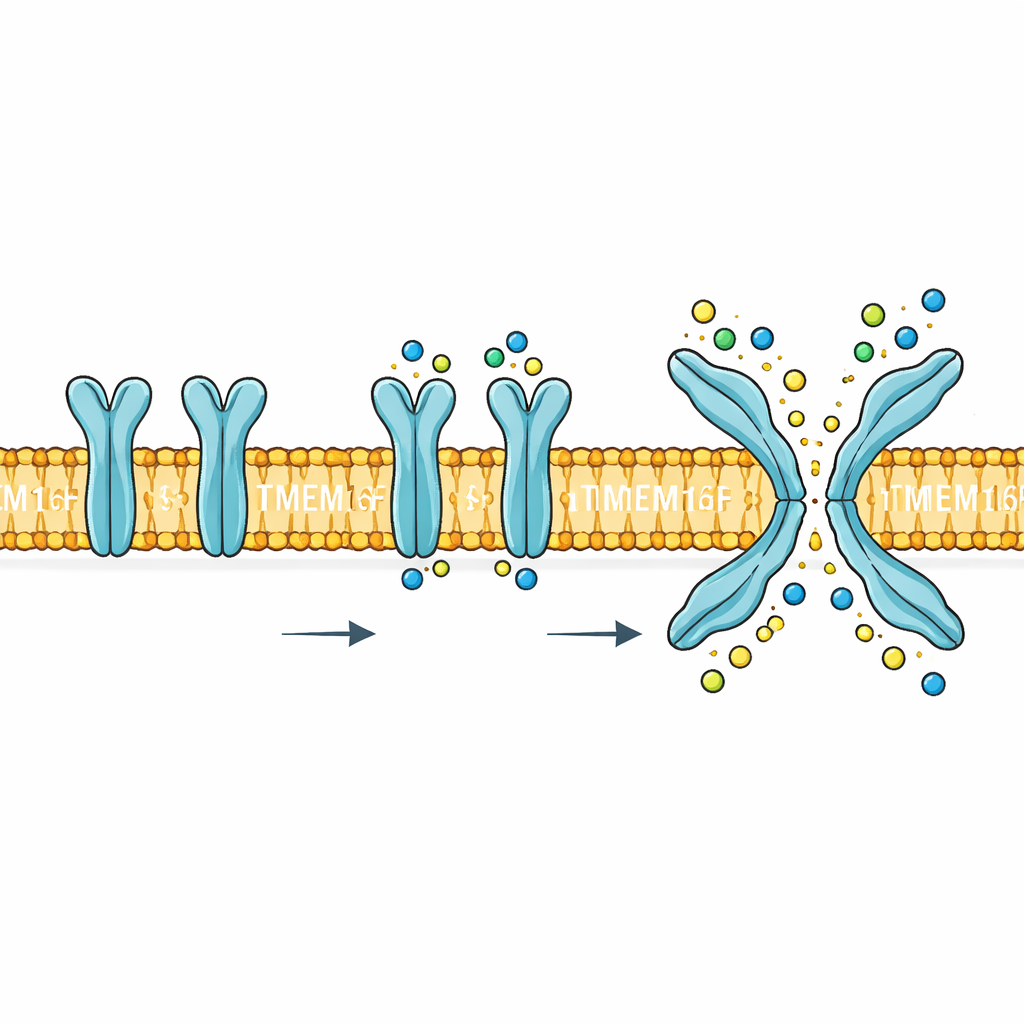
TMEM16F sitter i cellens yttre membran och reagerar på ökningar av kalcium inuti cellen. När det aktiveras utför det två mycket olika uppgifter. För det första bildar det en väg som låter små laddade partiklar såsom natrium, kalium och klorid passera membranet. För det andra vänder det vissa lipider, särskilt fosfatidylserin, från membranets inre yta till den yttre. Denna lipidvändning är en kraftfull biologisk signal: den hjälper blodplättar att bilda koagel, markerar skadade celler för borttagning och kan utnyttjas av virus för att ta sig in i celler. Mutationer eller felreglering av TMEM16F är kopplade till problem i blod, ben och nervsystemet, vilket gör dess mekanism till mer än en kuriositet — det är ett potentiellt läkemedelsmål.
Att se proteinet i dess naturliga miljö
Tidigare strukturella studier undersökte TMEM16F i artificiella miljöer som tensider eller nanodiskar, och såg konsekvent det i vad som såg ut som ett stängt tillstånd, även när kalcium var närvarande. Det väckte ett mysterium: funktionella experiment visade tydligt att proteinet var aktivt, men dess struktur verkade inte öppna någon väg för joner eller lipider. För att lösa detta återställde författarna mus‑TMEM16F i små, fritt flytande membranblåsor (liposomer) gjorda av enkla, väldefinierade lipider — samma typ av miljö där de kunde mäta jonrörelser och lipid‑scrambling direkt. De använde sedan kryoelektronmikroskopi för att fånga miljontals ögonblicksbilder av proteinet och sorterades dessa in i distinkta former som representerar olika aktivitetsstater.
Hur kalcium omformar porten
I frånvaro av kalcium intog TMEM16F två liknande, inaktiva former där en viktig fåra genom proteinet var tätt sluten. När kalcium tillsattes favoriserade proteinet en konventionell kalciumbunden men fortfarande stängd form, och en andra, mer sällsynt men slående annorlunda form. I detta aktiva tillstånd gled ett segment av proteinet kallat TM4 mot ett närliggande segment TM6 och skapade en X‑formad fåra som korsade membranet. Den centrala delen av denna fåra bildade en kontinuerlig, proteinomgärdad por tillräckligt bred för delvis hydrerade joner, medan regionerna närmare membranytorna öppnade upp i bredare vestibyler. Forskarna bekräftade betydelsen av denna konformation genom att skapa mutationer: de som försköt proteinet mot den X‑formade staten gjorde scrambling lättare, medan de som fångade det i den stängda formen nästan eliminerade aktiviteten.
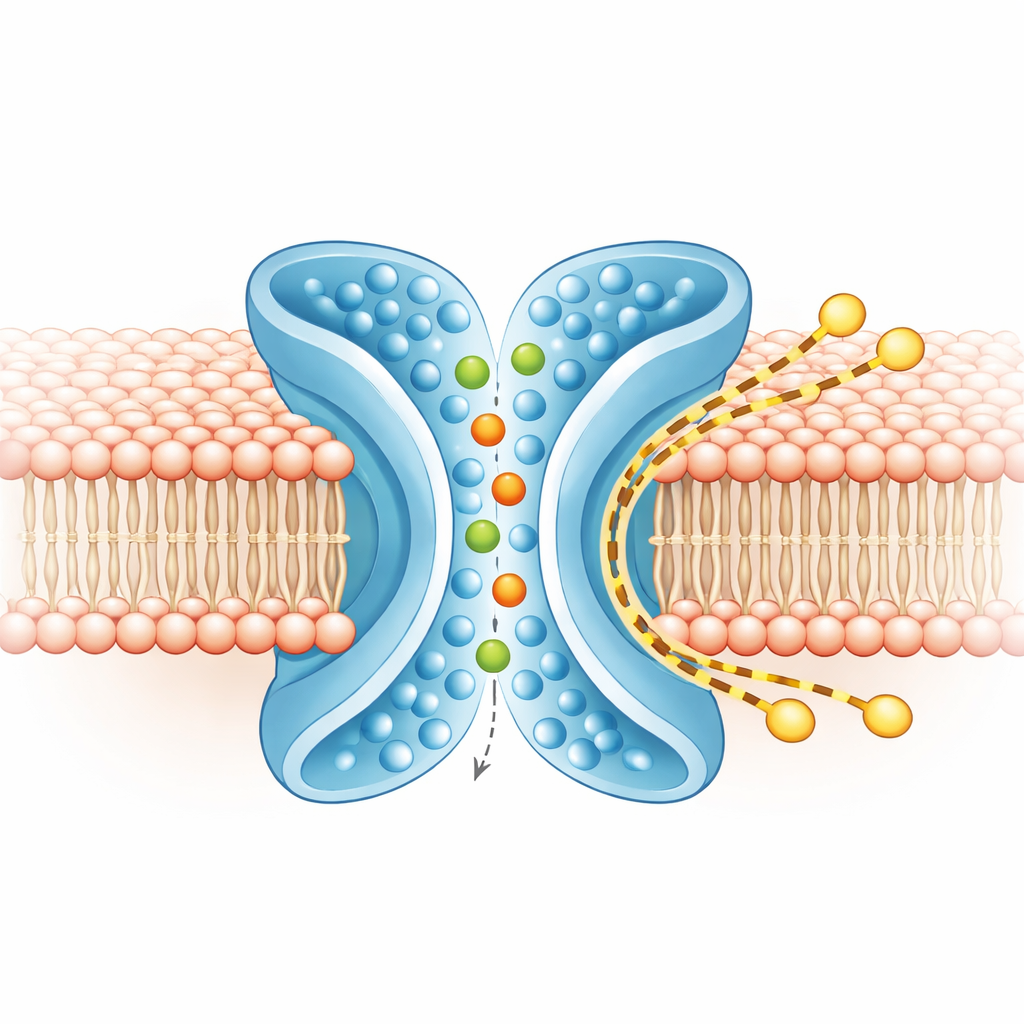
Separata spår för joner och lipider
För att förstå vad som rör sig var körde teamet omfattande datorsimuleringar av TMEM16F i ett realistiskt membran, både i de stängda och aktiva formerna. I den aktiva, X‑formade konfigurationen slingrade sig joner genom den centrala poren, inträdande från båda sidor och behöll större delen av sitt omgivande vattenskal, vilket stämmer med proteinets svaga preferens mellan positiva och negativa joner. Samtidigt tunnades det yttre membranet runt TM4 och TM6 ut och böjde sig. Grovskaliga simuleringar, körda under längre tider, visade hundratals lipidmolekyler som korsade från ett lager till det andra längs utsidan av den X‑formade fåran, i stort sett utan att gå genom jonporen. Jonernas och lipidernas vägar överlappade bara i liten utsträckning, vilket indikerar att proteinet driver två i huvudsak oberoende spår sida vid sida: ett inre för joner och ett yttre för lipider.
En flexibel reglerare kopplad till cellsignaler
Studien visar också hur proteinets inre, cytosoliska domän fungerar som en mekanisk länk som omvandlar kalciumbindning till dessa stora rörelser. I vilotillståndet bildar denna domän en kompakt struktur hålls ihop av ett nätverk av elektrostatisk ”låsning” mellan specifika aminosyror. Kalciumbindning rätar ut TM6‑segmentet och knuffar denna domän; att bryta saltbryggslåsen tillåter en del av domänen att rotera uppåt och haka fast vid TM6. Den rörelsen överförs till TM4–TM5‑regionen, vilket får TM4 att glida och bilda den X‑formade fåran. Mutationer som försvagar låset snabbare scrambling, medan de som gynnar det stängda tillståndet saktar ner eller blockerar det.
Vad detta betyder för hälsa och sjukdom
I vardagliga termer visar detta arbete att TMEM16F är en liten, kalciumstyrd maskin som samtidigt kan öppna ett inre rör för joner och forma det omgivande membranet så att lipider glider över det. Istället för att dela en enda blandad väg färdas joner och lipider mestadels på separata spår formade av samma proteinrörelse. Genom att avslöja hur kalciumbindning, interna omorganiseringar och membranböjning samarbetar, ger studien en ritning för att förstå sjukdomar kopplade till TMEM16F och för att designa läkemedel som kan finjustera dess aktivitet i blodkoagulation, membranreparation och virusinfektioner.
Citering: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Nyckelord: TMEM16F, lipidsortering, jonkanaler, cellmembran, kalciumsignalering