Clear Sky Science · de
Calciumabhängige Aktivierung des TMEM16F-Scramblase und Ionenkanals
Warum dieses winzige Membranventil wichtig ist
Sekunde für Sekunde bewegen die Membranen rund um unsere Zellen still und unaufdringlich Moleküle hin und her, damit wir leben. Ein wenig beachteter Akteur in diesem Gleichgewicht ist ein Protein namens TMEM16F. Es unterstützt die Blutgerinnung, repariert eingerissene Membranen, lenkt Immunzellen des Gehirns und wird sogar von Viren wie SARS‑CoV‑2 ausgenutzt, um Zellen zu infizieren. Bislang verstanden Forschende jedoch nicht, wie dieses Protein an- und abgeschaltet wird oder wie es sowohl als Ionenkanal als auch als Lipid‑„Scrambler“ fungieren kann, der Fettmoleküle zwischen den Membranseiten umdreht. Diese Studie benutzt hochauflösende Abbildungen und Computersimulationen, um TMEM16F‑Bewegungen mit beispielloser Detailtreue zu enthüllen.
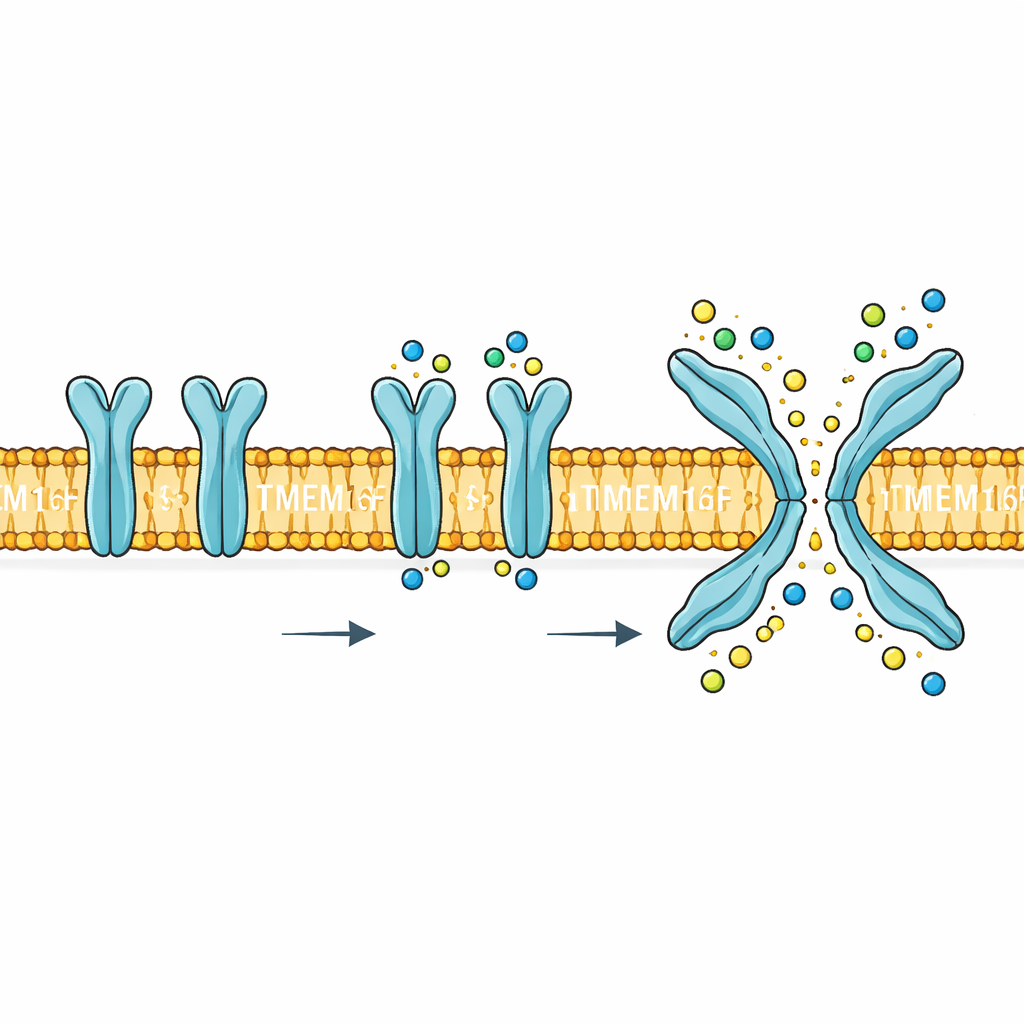
Ein doppelter Schalter an der Zellgrenze
TMEM16F sitzt in der äußeren Zellmembran und reagiert auf Anstiege des Calciumspiegels im Zellinneren. Nach der Aktivierung erfüllt es zwei sehr unterschiedliche Aufgaben. Erstens bildet es einen Weg, der kleinen geladenen Teilchen wie Natrium, Kalium und Chlorid erlaubt, die Membran zu passieren. Zweitens dreht es bestimmte Lipide, vor allem Phosphatidylserin, von der inneren zur äußeren Membranseite. Dieses Lipid‑Flip ist ein starkes biologisches Signal: Es hilft Blutplättchen bei der Gerinnung, markiert beschädigte Zellen zur Beseitigung und kann von Viren zur Zellaufnahme ausgenutzt werden. Mutationen oder Fehlregulation von TMEM16F stehen im Zusammenhang mit Problemen im Blut-, Knochen‑ und Nervensystem, wodurch sein Mechanismus mehr als nur eine wissenschaftliche Kuriosität wird — er ist ein potenzielles Arzneimittelziel.
Das Protein in seiner natürlichen Umgebung sehen
Frühere Strukturstudien untersuchten TMEM16F in künstlichen Umgebungen wie Detergenzien oder Nanodiscs und beobachteten es durchweg in einem scheinbar geschlossenen Zustand, selbst wenn Calcium vorhanden war. Das ergab ein Rätsel: Funktionelle Experimente zeigten deutlich Aktivität des Proteins, doch die Struktur schien keinen Weg für Ionen oder Lipide zu öffnen. Um das zu klären, rekonstruierten die Autorinnen und Autoren Maus‑TMEM16F in winzige, frei schwebende Membranbläschen (Liposome) aus einfachen, gut definierten Lipiden — der Art von Umgebung, in der sie direkt Ionenbewegung und Lipid‑Scrambling messen konnten. Anschließend nutzten sie Kryo‑Elektronenmikroskopie, um Millionen Momentaufnahmen des Proteins zu erfassen und diese in verschiedene Konformationen zu sortieren, die unterschiedliche Aktivitätszustände repräsentieren.
Wie Calcium das Ventil umformt
Ohne Calcium nahm TMEM16F zwei ähnliche, inaktive Formen an, in denen eine wichtige Rinne durch das Protein fest verschlossen war. Nach Zugabe von Calcium bevorzugte das Protein eine konventionelle, Calcium‑gebundene, aber weiterhin geschlossene Form und eine zweite, seltener auftretende, aber auffallend unterschiedliche Form. In diesem aktiven Zustand glitt ein Segment des Proteins, TM4, an dem benachbarten Segment TM6 vorbei und bildete eine X‑förmige Rinne, die die Membran überspannte. Der zentrale Abschnitt dieser Rinne bildete einen durch Protein begrenzten, durchgehenden Kanal, breit genug für teilweise hydrierte Ionen, während die Bereiche näher an den Membranoberflächen sich zu weiteren Vorhöfen öffneten. Die Forschenden bestätigten die Bedeutung dieser Konformation durch gezielte Mutationen: Varianten, die das Protein zugunsten des X‑förmigen Zustands verschoben, erleichterten das Scrambling, während solche, die es in der geschlossenen Form einkerkerten, die Aktivität nahezu aufhoben.
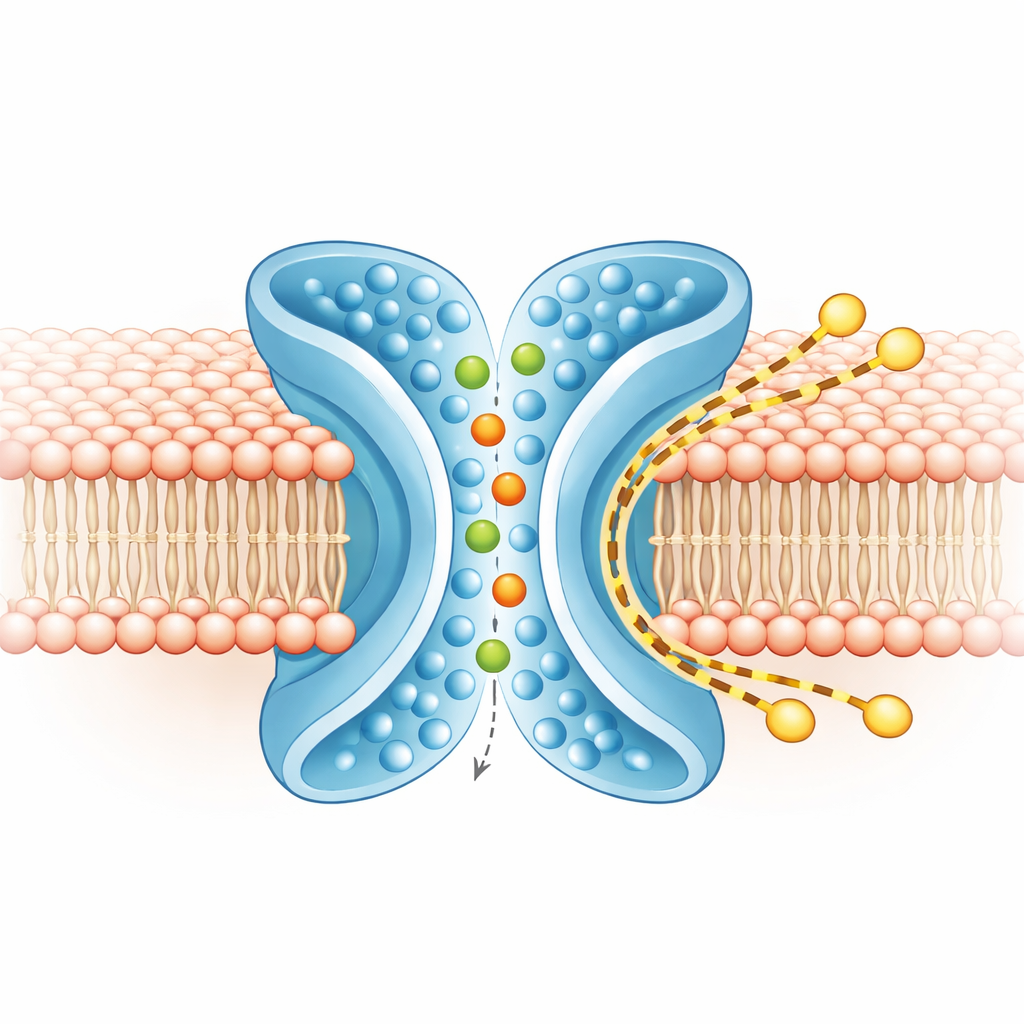
Getrennte Bahnen für Ionen und Lipide
Um zu verstehen, was wo entlangwandert, führten die Autorinnen und Autoren umfangreiche Computersimulationen von TMEM16F in einer realistischen Membran durch, sowohl in der geschlossenen als auch in der aktiven Gestalt. In der aktiven, X‑förmigen Form schlängelten sich Ionen durch den zentralen Kanal, traten von beiden Seiten ein und behielten größtenteils ihre umgebende Wasserschale, was zur lockeren Präferenz des Proteins zwischen positiven und negativen Ionen passt. Gleichzeitig wurde die äußere Membranschicht um TM4 und TM6 dünner und bog sich. Grobskalige Simulationen über längere Zeiten zeigten Hunderte von Lipidmolekülen, die entlang der Außenseite der X‑förmigen Rinne von einem Blatt zum anderen wechselten und dabei größtenteils den Ionenkanal umgingen. Die Wege von Ionen und Lipiden überlappten nur minimal, was darauf hindeutet, dass das Protein zwei weitgehend unabhängige Bahnen nebeneinander betreibt: eine innere für Ionen und eine äußere für Lipide.
Ein flexibler Regler, der an zelluläre Signale gebunden ist
Die Studie zeigt außerdem, wie die innere, zytosolische Domäne des Proteins wie eine mechanische Verbindung funktioniert, die Calciumbindung in diese großen Bewegungen übersetzt. Im Ruhe‑ zustand bildet diese Domäne eine kompakte Struktur, zusammengehalten von einem Netzwerk elektrostatischer „Schlösser“ zwischen bestimmten Aminosäuren. Calciumbindung richtet das TM6‑Segment auf und schiebt diese Domäne; das Aufbrechen der Salzbrücken‑Schlösser erlaubt einem Teil der Domäne, sich aufzudrehen und an TM6 anzudocken. Diese Bewegung wird an den TM4–TM5‑Bereich weitergegeben, wodurch TM4 gleitet und die X‑förmige Rinne bildet. Mutationen, die das Schloss schwächen, beschleunigen das Scrambling, während solche, die den geschlossenen Zustand begünstigen, es verlangsamen oder blockieren.
Was das für Gesundheit und Krankheit bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass TMEM16F eine winzige, calciumgesteuerte Maschine ist, die gleichzeitig ein inneres Rohr für Ionen öffnet und die umgebende Membran so formt, dass Lipide darüber hinweggleiten. Anstatt einen einzigen gemischten Pfad zu teilen, reisen Ionen und Lipide größtenteils auf getrennten Bahnen, die durch dieselbe Proteinbewegung geformt werden. Indem die Studie offenlegt, wie Calciumbindung, interne Umordnungen und Membranverformung zusammenwirken, liefert sie einen Bauplan zum Verständnis von Krankheiten, die mit TMEM16F verbunden sind, und für das Design von Wirkstoffen, die seine Aktivität bei Blutgerinnung, Membranreparatur und Virusinfektionen feinabstimmen können.
Zitation: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Schlüsselwörter: TMEM16F, Lipidscrambling, Ionenkanäle, Zellmembran, Calcium-Signalgebung