Clear Sky Science · fr
Activation dépendante du calcium du scramblase et canal ionique TMEM16F
Pourquoi cette minuscule vanne membranaire compte
À chaque seconde, les membranes qui entourent nos cellules réorganisent discrètement des molécules pour nous maintenir en vie. Un acteur peu célébré de cet équilibre est une protéine nommée TMEM16F. Elle contribue à la coagulation sanguine, répare les membranes déchirées, guide les cellules immunitaires du cerveau et se fait même détourner par des virus comme le SARS‑CoV‑2 pour infecter des cellules. Pourtant, jusqu’à présent, les scientifiques ne comprenaient pas comment cette protéine s’active et se désactive, ni comment elle peut à la fois fonctionner comme canal ionique et comme « scrambler » de lipides qui inverse des molécules grasses entre les deux faces de la membrane. Cette étude utilise l’imagerie à haute résolution et des simulations informatiques pour révéler les mouvements de TMEM16F avec un niveau de détail sans précédent.
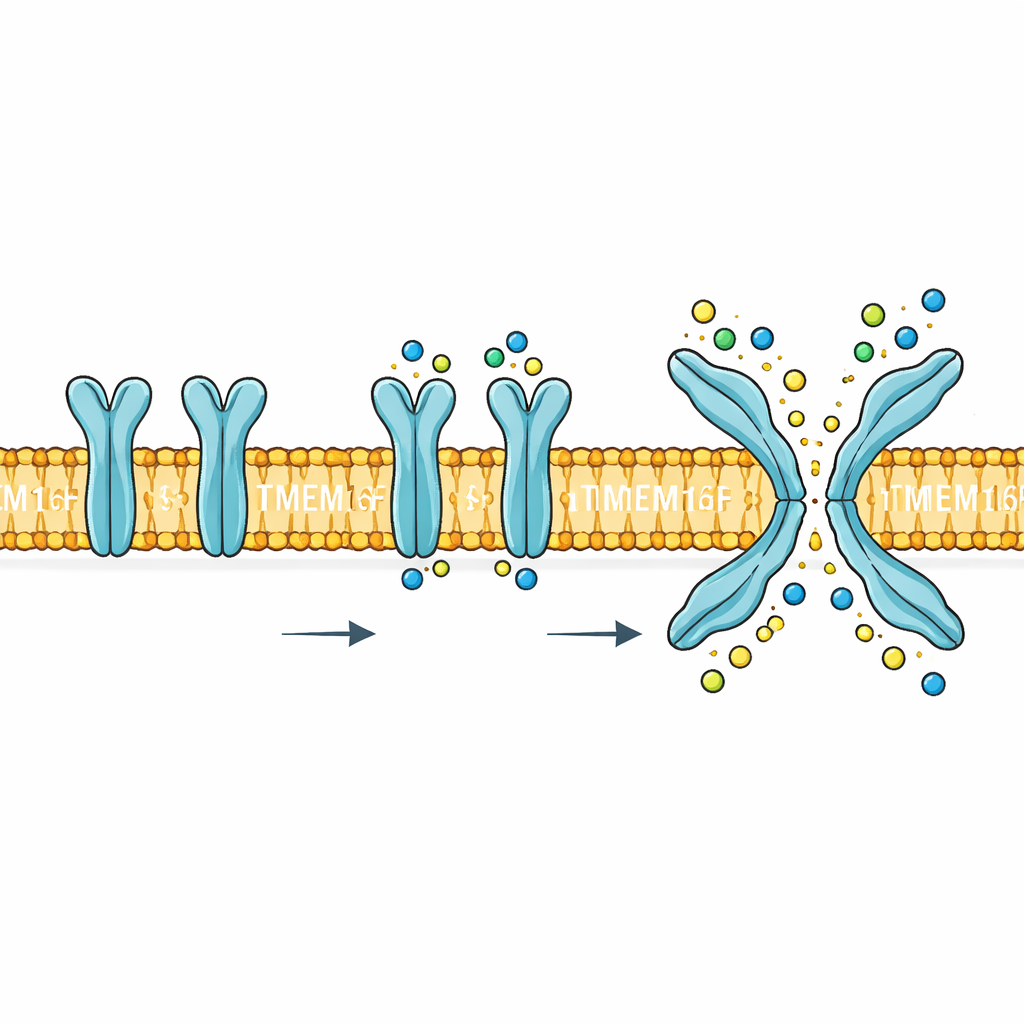
Une porte à double fonction à la frontière cellulaire
TMEM16F est ancrée dans la membrane externe de la cellule et répond aux augmentations de calcium à l’intérieur de la cellule. Lorsqu’elle s’active, elle accomplit deux tâches très différentes. D’une part, elle forme une voie qui laisse passer de petites particules chargées comme le sodium, le potassium et le chlorure à travers la membrane. D’autre part, elle bascule certains lipides, en particulier la phosphatidylsérine, de la face interne de la membrane vers la face externe. Ce retournement lipidique est un signal biologique puissant : il aide les plaquettes à former des caillots, signale les cellules endommagées pour leur élimination et peut être exploité par des virus pour pénétrer dans les cellules. Des mutations ou une régulation anormale de TMEM16F sont associées à des troubles sanguins, osseux et du système nerveux, ce qui fait de son mécanisme plus qu’une curiosité — c’est une cible médicamenteuse potentielle.
Voir la protéine dans son habitat natif
Les études structurales précédentes ont examiné TMEM16F dans des environnements artificiels comme des détergents ou des nanodisque, et l’ont systématiquement observée dans ce qui ressemblait à un état fermé, même en présence de calcium. Cela posait un casse‑tête : les expériences fonctionnelles montraient clairement que la protéine était active, mais sa structure ne semblait pas ouvrir de passage pour les ions ou les lipides. Pour résoudre ce point, les auteurs ont reconstitué la TMEM16F de souris dans de petites bulles membranaires flottantes (liposomes) composées de lipides simples et bien définis — le même type d’environnement dans lequel ils pouvaient mesurer directement le mouvement des ions et le réarrangement des lipides. Ils ont ensuite utilisé la cryo‑microscopie électronique pour capturer des millions d’instantanés de la protéine et ont trié ces images en formes distinctes représentant différents états d’activité.
Comment le calcium remodèle la porte
En l’absence de calcium, la TMEM16F adoptait deux formes inactives similaires dans lesquelles une rainure clé traversant la protéine était hermétiquement scellée. Lorsqu’on ajoutait du calcium, la protéine favorisait une forme conventionnelle liée au calcium mais encore fermée, et une seconde forme plus rare mais frappante. Dans cet état actif, un segment de la protéine appelé TM4 glissait le long d’un segment voisin TM6, créant une rainure en forme de X qui traversait la membrane. La partie centrale de cette rainure formait un pore continu, délimité par la protéine, suffisamment large pour des ions partiellement hydratés, tandis que les régions proches des surfaces membranaires s’ouvraient en vestibules plus larges. Les chercheurs ont confirmé l’importance de cette conformation en concevant des mutations : celles qui faisaient basculer la protéine vers l’état en X facilitaient le scrambling, tandis que celles qui la piégeaient dans la forme fermée réduisaient presque totalement l’activité.
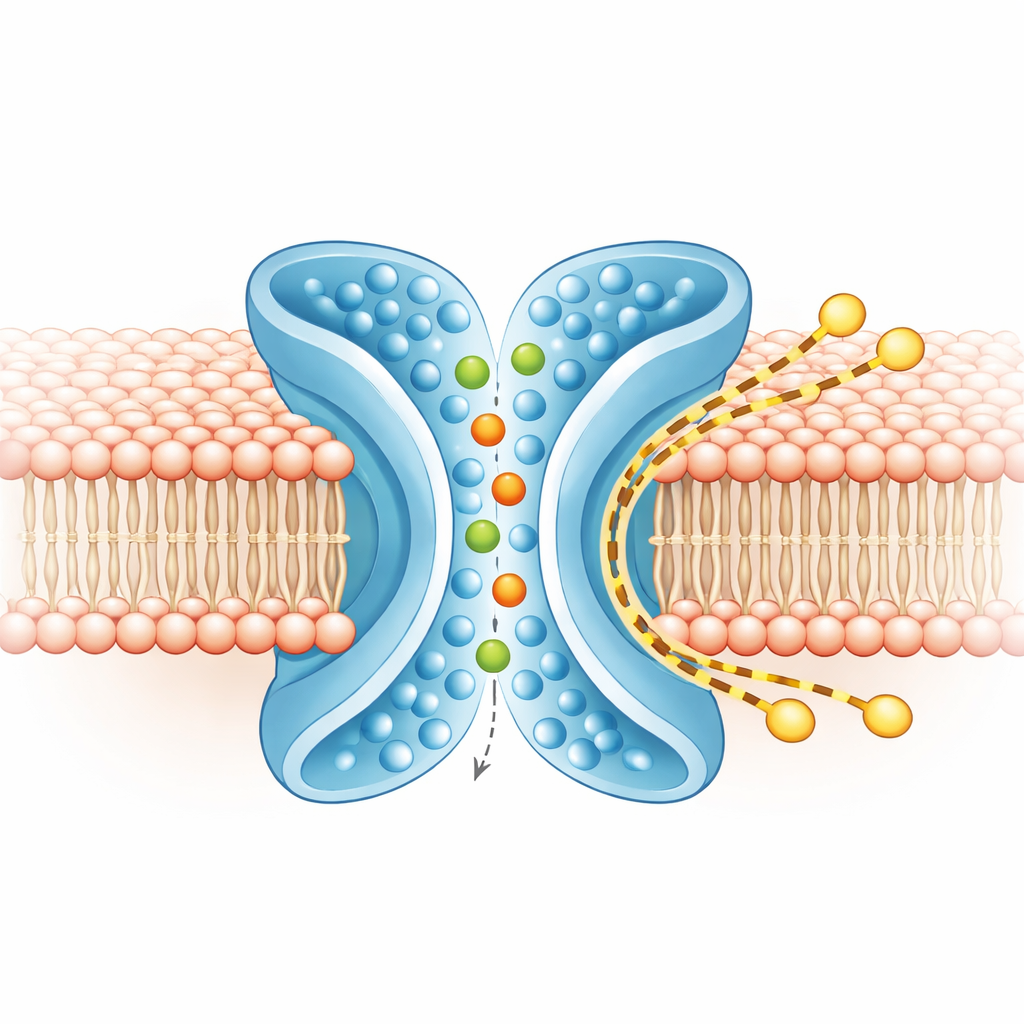
Voies séparées pour ions et lipides
Pour comprendre ce qui se déplace et où, l’équipe a réalisé de vastes simulations informatiques de TMEM16F dans une membrane réaliste, à la fois dans les formes fermées et actives. Dans la forme active en X, les ions s’insinuaient à travers le pore central, entrant de chaque côté et conservant la majeure partie de leur enveloppe d’eau, ce qui correspond à la préférence lâche de la protéine entre ions positifs et négatifs. Parallèlement, la couche externe de la membrane autour de TM4 et TM6 s’amincissait et se courbait. Des simulations à résolution grossière, exécutées sur des temps plus longs, ont montré des centaines de molécules lipidiques traversant d’un feuillet à l’autre le long de l’extérieur de la rainure en X, contournant en grande partie le pore ionique. Les trajectoires des ions et des lipides se chevauchaient très peu, indiquant que la protéine exploite deux voies largement indépendantes côte à côte : une intérieure pour les ions et une extérieure pour les lipides.
Un régulateur flexible lié aux signaux cellulaires
L’étude révèle également comment le domaine interne cytosolique de la protéine agit comme une liaison mécanique qui convertit la liaison du calcium en ces grands mouvements. À l’état de repos, ce domaine forme une structure compacte maintenue par un réseau de « verrous » électrostatiques entre certains acides aminés. La liaison du calcium redresse le segment TM6 et pousse ce domaine ; la rupture des ponts salins permet à une partie du domaine de pivoter vers le haut et de s’accrocher à TM6. Ce mouvement se transmet à la région TM4–TM5, provoquant le glissement de TM4 et la formation de la rainure en X. Les mutations qui affaiblissent le verrou accélèrent le scrambling, tandis que celles qui favorisent l’état fermé le ralentissent ou le bloquent.
Ce que cela signifie pour la santé et la maladie
Concrètement, ce travail montre que TMEM16F est une minuscule machine contrôlée par le calcium qui peut simultanément ouvrir un conduit interne pour les ions et sculpter la membrane environnante pour permettre aux lipides de la traverser. Plutôt que de partager une seule voie mixte, les ions et les lipides empruntent principalement des trajectoires séparées, façonnées par le même mouvement protéique. En révélant comment la liaison du calcium, les réarrangements internes et la flexion membranaire coopèrent, l’étude fournit un plan pour comprendre les maladies liées à TMEM16F et pour concevoir des médicaments capables d’ajuster finement son activité dans la coagulation, la réparation membranaire et les infections virales.
Citation: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Mots-clés: TMEM16F, réarrangement des lipides, canaux ioniques, membrane cellulaire, signalisation calcique