Clear Sky Science · ru
Кальций‑зависимая активация скрамблазы и ионного канала TMEM16F
Почему этот крошечный «клапан» мембраны важен
Каждую секунду мембраны вокруг наших клеток незаметно перетасовывают молекулы, чтобы поддерживать жизнь. Один из малозаметных участников этого баланса — белок под названием TMEM16F. Он помогает свертыванию крови, ремонтирует повреждённые мембраны, направляет иммунные клетки мозга и даже используется вирусами, такими как SARS‑CoV‑2, для проникновения в клетки. Однако до сих пор учёным было неясно, как этот белок включаетcя и выключается и как он может одновременно работать как ионный канал и как «скрамблер» липидов, перекидывая жировые молекулы с одной стороны мембраны на другую. В этом исследовании используются высокоразрешающая визуализация и компьютерные моделирования, чтобы показать движения TMEM16F в беспрецедентных деталях.
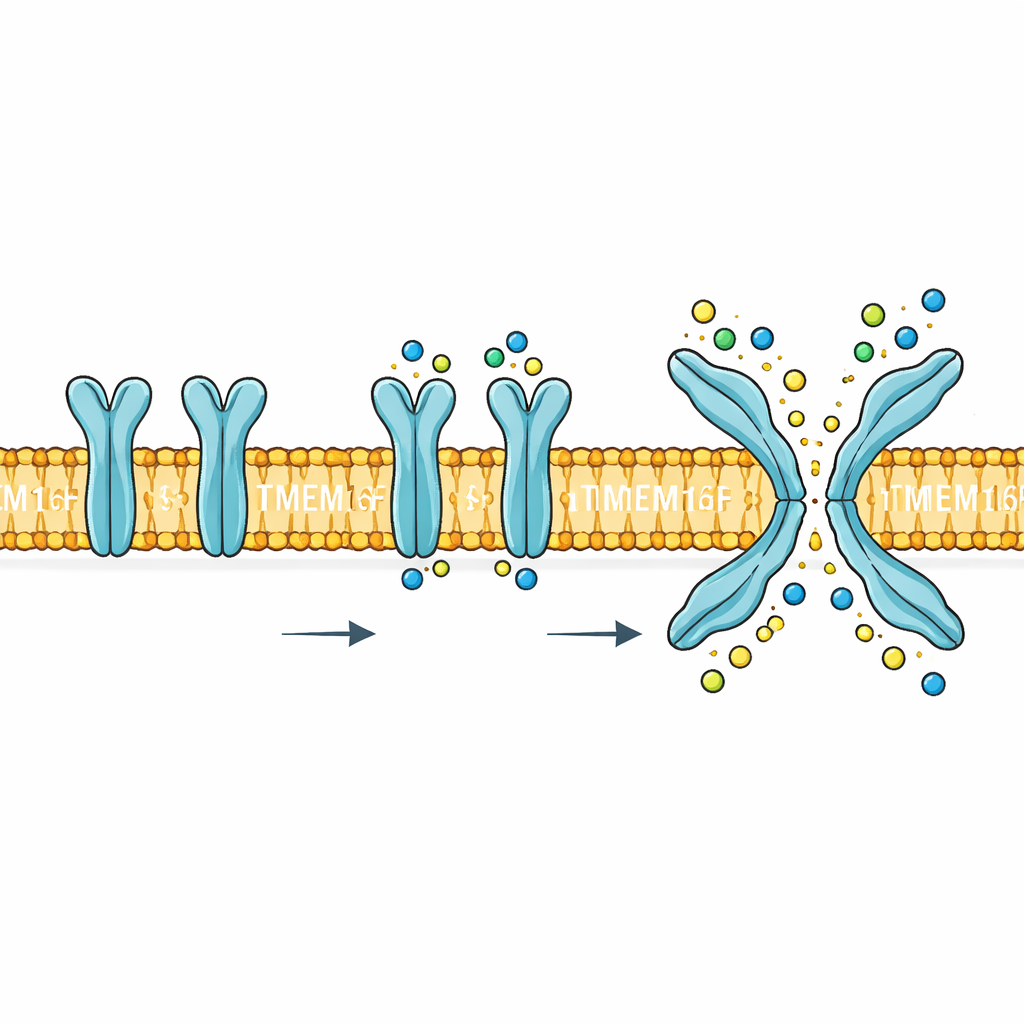
Двухфункциональный затвор на границе клетки
TMEM16F располагается в плазматической мембране клетки и реагирует на повышение уровня кальция внутри клетки. После активации он выполняет две принципиально разные задачи. Во‑первых, образует путь, по которому мелкие заряженные частицы — натрий, калий, хлор — проходят через мембрану. Во‑вторых, перекидывает определённые липиды, особенно фосфатидилсерин, с внутренней стороны мембраны на наружную. Такое перераспределение липидов — мощный биологический сигнал: оно помогает тромбоцитам формировать сгустки, помечает повреждённые клетки для удаления и может быть использовано вирусами для проникновения в клетку. Мутации или неправильная регуляция TMEM16F связаны с нарушениями крови, костей и нервной системы, поэтому его механизм — не просто любопытство, а потенциальная мишень для лекарств.
Наблюдая белок в его естественной среде
Предыдущие структурные исследования изучали TMEM16F в искусственных условиях — в детергентах или нанодисках — и постоянно видели его в состоянии, похожем на закрытое, даже при наличии кальция. Это породило загадку: функциональные эксперименты ясно показывали активность белка, но его структура не выглядела открывающей путь для ионов или липидов. Чтобы разрешить это, авторы заново воссоздали мышиный TMEM16F в крошечных свободно плавающих пузырьках мембраны (липосомах), сделанных из простых, точно определённых липидов — в той же среде, где можно было напрямую измерять движение ионов и перемешивание липидов. Затем они использовали крио‑электронную микроскопию, чтобы захватить миллионы снимков белка и отсортировать их по отдельным формам, соответствующим разным состояниям активности.
Как кальций меняет форму «затвора»
В отсутствие кальция TMEM16F принимал две похожие неактивные формы, в которых ключевой желобок через белок был плотно закрыт. При добавлении кальция белок предпочитал обычную кальций‑связанную, но всё ещё закрытую форму, и вторую, более редкую, но заметно отличную форму. В этом активном состоянии сегмент белка, называемый TM4, сдвигался относительно соседнего сегмента TM6, создавая X‑образный желобок, пересекающий мембрану. Центральная часть этого желобка образовывала непрерывный канал, выложенный белком и достаточно широкий для частично гидратированных ионов, тогда как участки ближе к поверхностям мембраны открывались в более широкие преддверия. Исследователи подтвердили значимость этой конформации при помощи инженерных мутаций: те, что смещали белок в сторону X‑образного состояния, облегчали скрамблинг, тогда как мутации, запирающие его в закрытой форме, почти полностью подавляли активность.
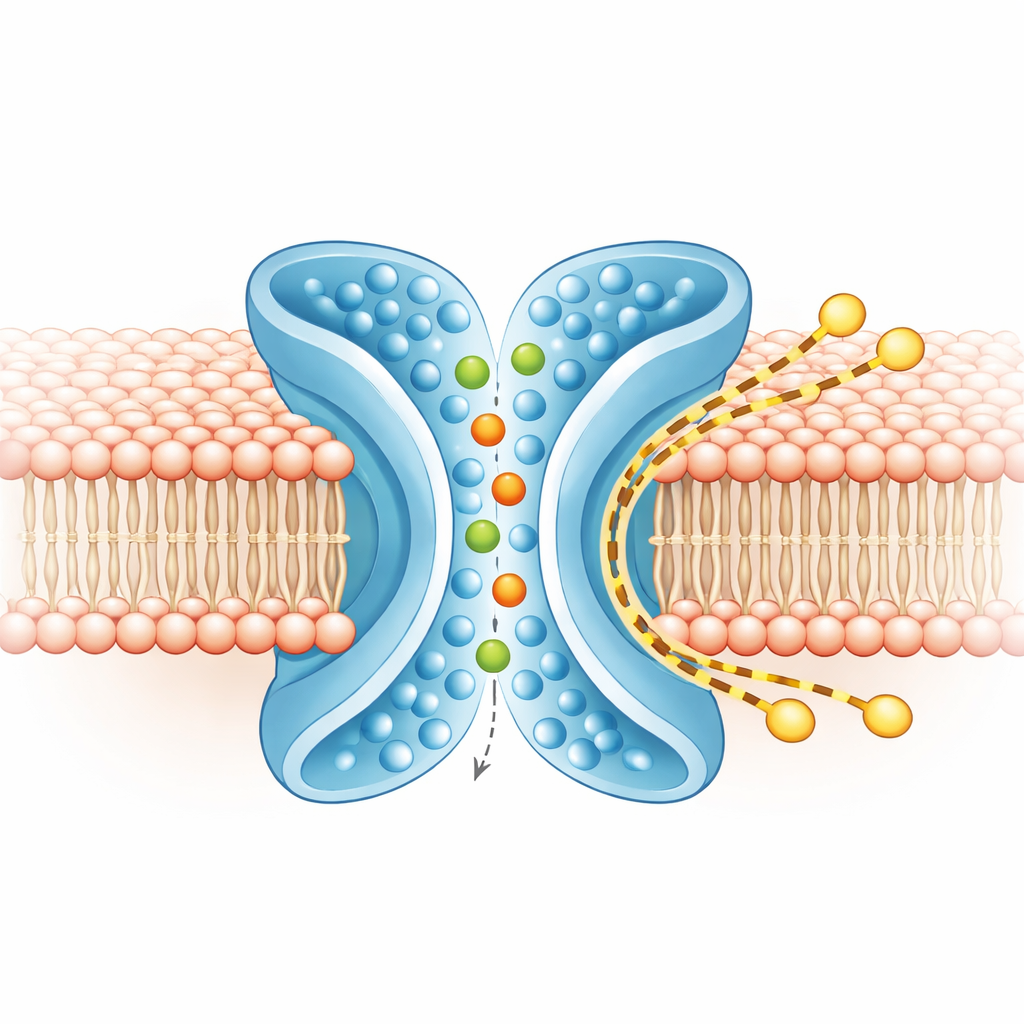
Отдельные пути для ионов и липидов
Чтобы понять, что куда перемещается, команда провела обширные компьютерные симуляции TMEM16F в реалистичной мембране, как в закрытых, так и в активных формах. В активной X‑образной форме ионы пробегали через центральный канал, заходя с обеих сторон и сохраняя большую часть своей оболочки воды, что согласуется со слабым предпочтением белка между катионами и анионами. Одновременно внешний слой мембраны вокруг TM4 и TM6 истончался и изгибался. Крупномасштабные, долгие симуляции показали сотни липидных молекул, переходящих с одного листа мембраны на другой вдоль внешней стороны X‑образного желобка, в основном обходя ионный канал. Маршруты ионов и липидов лишь минимально перекрывались, что указывает на то, что белок обеспечивает два по сути независимых пути рядом друг с другом: внутренний для ионов и внешний для липидов.
Гибкий контролёр, связанный с клеточными сигналами
Исследование также выявляет, как внутренняя цитозольная домен белка действует как механическая тяга, преобразующая связывание кальция в эти крупные движения. В состоянии покоя этот домен образует компактную структуру, удерживаемую сетью электростатических «замков» между определёнными аминокислотами. Связывание кальция выпрямляет сегмент TM6 и толкает этот домен; разрыв солевых мостов позволяет части домена повернуться вверх и защёлкнуться за TM6. Это движение передаётся на область TM4–TM5, вызывая сдвиг TM4 и формирование X‑образного желобка. Мутации, ослабляющие эти «замки», ускоряют скрамблинг, тогда как мутации, стабилизирующие закрытое состояние, замедляют или блокируют его.
Что это значит для здоровья и болезней
Проще говоря, работа показывает, что TMEM16F — крошечная кальций‑управляемая машина, которая одновременно может открыть внутренний канал для ионов и изменить форму окружающей мембраны так, чтобы липиды переходили через неё. Вместо единого смешанного пути ионы и липиды в основном идут по отдельным дорожкам, сформированным одним и тем же движением белка. Показав, как связывание кальция, внутренние перестройки и изгиб мембраны действуют вместе, исследование даёт чертёж для понимания заболеваний, связанных с TMEM16F, и для разработки препаратов, способных тонко регулировать его активность в свертывании крови, ремонте мембран и вирусных инфекциях.
Цитирование: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Ключевые слова: TMEM16F, перемешивание липидов, ионные каналы, клеточная мембрана, кальциевые сигналы