Clear Sky Science · pl
Aktywacja zależna od wapnia scramblazy i kanału jonowego TMEM16F
Dlaczego ta malutka membranowa zaworka ma znaczenie
Co sekundę błony otaczające nasze komórki dyskretnie przestawiają molekuły, by utrzymać funkcje życiowe. Jednym z niedocenianych graczy w tym równoważeniu jest białko o nazwie TMEM16F. Ułatwia krzepnięcie krwi, naprawia rozerwane błony, kieruje komórkami układu odpornościowego w mózgu, a nawet bywa wykorzystywane przez wirusy, takie jak SARS‑CoV‑2, do infekowania komórek. Jednak dotąd naukowcy nie rozumieli, jak to białko się włącza i wyłącza ani jak może pełnić jednocześnie funkcję kanału jonowego i „scramblazy” lipidów — przenosząc cząsteczki tłuszczowe między dwiema stronami błony. W badaniu zastosowano obrazowanie o wysokiej rozdzielczości i symulacje komputerowe, by ujawnić ruchy TMEM16F w bezprecedensowych szczegółach.
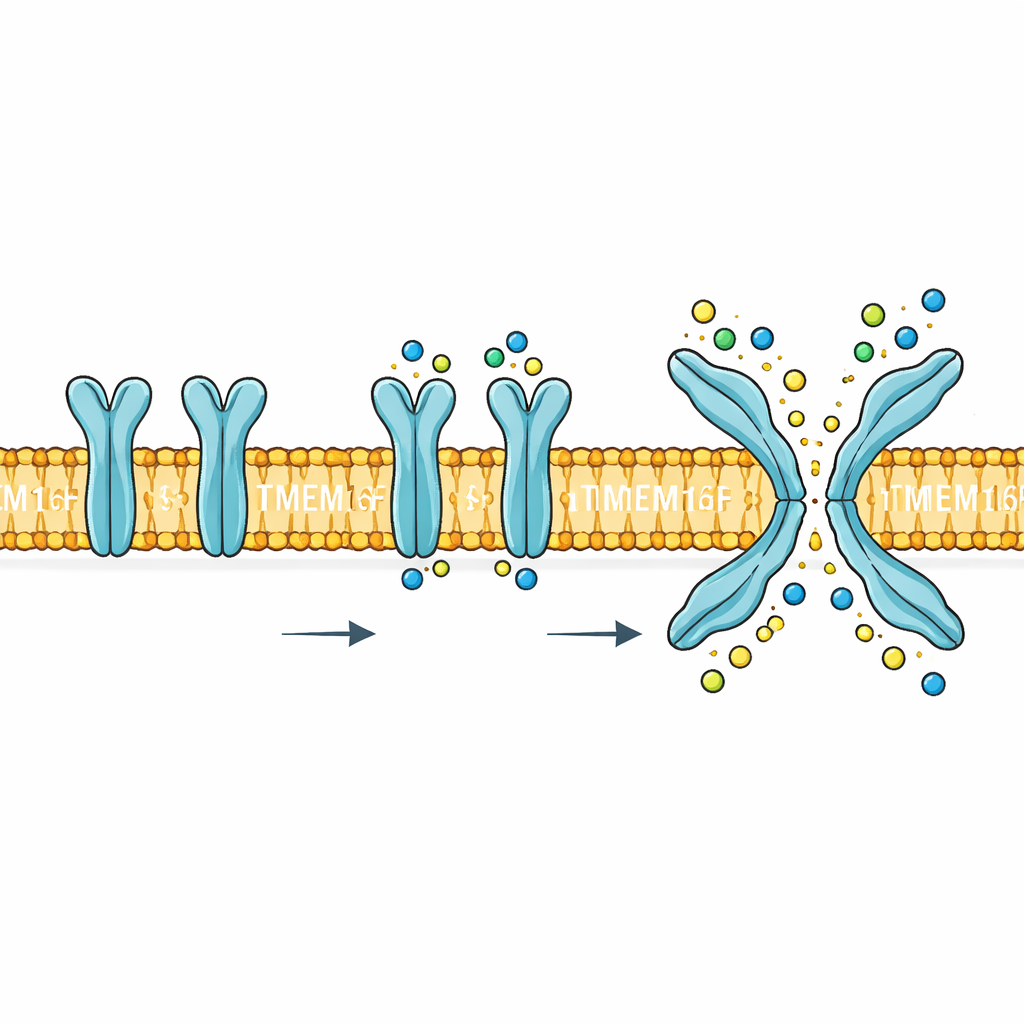
Dwufunkcyjna bramka w granicy komórki
TMEM16F osadza się w błonie zewnętrznej komórki i reaguje na wzrost stężenia wapnia wewnątrz komórki. Po aktywacji wykonuje dwie bardzo różne czynności. Po pierwsze, tworzy ścieżkę umożliwiającą przejście małych naładowanych cząstek, takich jak sód, potas i chlorki, przez błonę. Po drugie, odwraca orientację niektórych lipidów, zwłaszcza fosfatydyloseryny, z wewnętrznej strony błony na zewnętrzną. Ten flip lipidowy jest silnym sygnałem biologicznym: pomaga płytkom krwi tworzyć skrzepy, oznacza uszkodzone komórki do usunięcia i może być wykorzystany przez wirusy do wnikania do komórek. Mutacje lub zaburzenia regulacji TMEM16F wiążą się z problemami krwi, kości i układu nerwowego, co czyni jego mechanizm czymś więcej niż ciekawostką — to potencjalny cel terapeutyczny.
Obserwacja białka w jego naturalnym środowisku
Wcześniejsze badania strukturalne analizowały TMEM16F w środowiskach sztucznych, takich jak detergenty czy nanodyski, i konsekwentnie widziały go w pozornie zamkniętym stanie, nawet przy obecności wapnia. To rodziło zagadkę: eksperymenty funkcjonalne wyraźnie pokazywały aktywność białka, lecz jego struktura nie wydawała się otwierać drogi dla jonów ani lipidów. Aby to rozwiązać, autorzy odtworzyli mysi TMEM16F w maleńkich, swobodnie unoszących się pęcherzykach błonowych (liposomach) z prostych, dobrze zdefiniowanych lipidów — w takim środowisku mogli bezpośrednio mierzyć przepływ jonów i przestawianie lipidów. Następnie użyli krio‑mikroskopii elektronowej, by uchwycić miliony migawkowych obrazów białka i posortować je na odrębne konformacje reprezentujące różne stany aktywności.
Jak wapń przebudowuje zaworkę
W nieobecności wapnia TMEM16F przyjmował dwa podobne, nieaktywne kształty, w których kluczowy rowek przez białko był szczelnie zamknięty. Po dodaniu wapnia białko preferowało konwencjonalną formę związaną z wapniem, lecz wciąż zamkniętą, oraz drugą, rzadszą lecz uderzająco odmienną formę. W tym stanie aktywnym segment białka zwany TM4 przesunął się względem sąsiedniego segmentu TM6, tworząc X‑kształtny rowek przecinający błonę. Centralna część tego rowka utworzyła ciągły, białkowy kanał na tyle szeroki, by przepuszczać częściowo zhydratowane jony, podczas gdy obszary bliżej powierzchni błony otworzyły się w szersze przedsionki. Badacze potwierdzili znaczenie tej konformacji poprzez inżynierię mutacji: te, które przesuwały białko w stronę stanu X‑kształtnego, ułatwiały scrambling, podczas gdy mutacje blokujące je w zamkniętej formie prawie całkowicie znosiły aktywność.
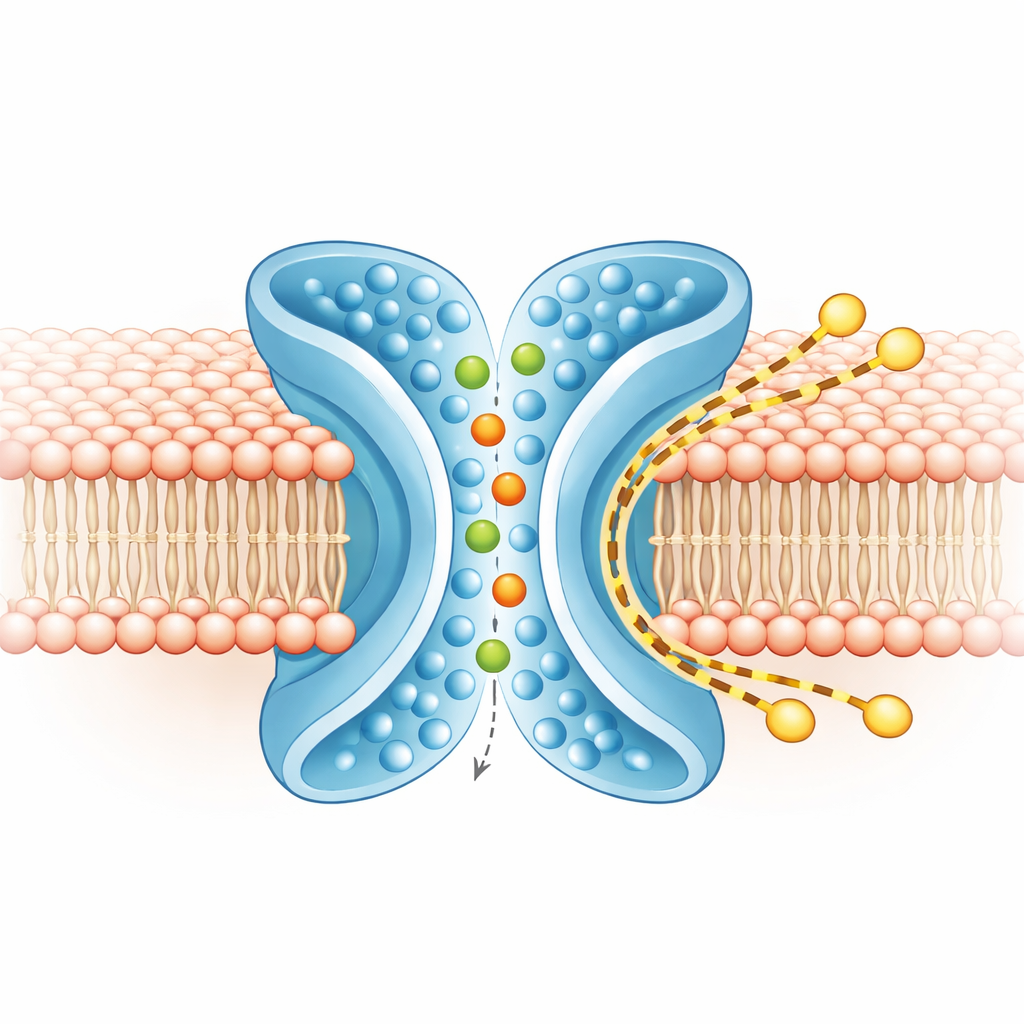
Oddzielne tory dla jonów i lipidów
Aby zrozumieć, co porusza się gdzie, zespół przeprowadził obszerne symulacje komputerowe TMEM16F w realistycznej błonie, zarówno w kształtach zamkniętych, jak i aktywnych. W aktywnej, X‑kształtnej formie jony przeciskały się przez centralny kanał, wchodząc z obu stron i zachowując większość swojej otaczającej powłoki wodnej, co jest zgodne z luźnym preferowaniem przez białko zarówno jonów dodatnich, jak i ujemnych. Jednocześnie zewnętrzna warstwa błony wokół TM4 i TM6 była cieńsza i wygięta. Symulacje o uproszczonej skali, prowadzone przez dłuższy czas, wykazały setki cząsteczek lipidów przechodzących z jednej warstwy do drugiej po zewnętrznej stronie X‑kształtnego rowka, w dużej mierze omijając kanał jonowy. Trasy jonów i lipidów nachodziły na siebie tylko minimalnie, co wskazuje, że białko prowadzi dwa w dużej mierze niezależne tory obok siebie: wewnętrzny dla jonów i zewnętrzny dla lipidów.
Elastyczny regulator powiązany z sygnałami komórkowymi
Badanie ujawnia również, jak wewnętrzna, cytosolowa domena białka działa jak mechaniczne połączenie, które przekształca wiązanie wapnia w te duże ruchy. W stanie spoczynkowym ta domena tworzy zwartą strukturę utrzymywaną przez sieć elektrostatycznych „zamków” między określonymi aminokwasami. Wiązanie wapnia prostuje segment TM6 i popycha tę domenę; rozerwanie mostków solnych pozwala części domeny obrócić się do góry i zaczepić o TM6. Ten ruch jest przekazywany do regionu TM4–TM5, powodując przesunięcie TM4 i utworzenie X‑kształtnego rowka. Mutacje osłabiające zamki przyspieszają scrambling, natomiast te, które faworyzują stan zamknięty, spowalniają lub blokują go.
Co to oznacza dla zdrowia i chorób
Mówiąc prostymi słowami, praca pokazuje, że TMEM16F jest maleńką, kontrolowaną przez wapń maszyną, która potrafi jednocześnie otworzyć wewnętrzną rurę dla jonów i ukształtować otaczającą błonę tak, by lipidy mogły się przez nią przesunąć. Zamiast dzielić jedną, wymieszaną ścieżkę, jony i lipidy w większości podróżują po oddzielnych torach ukształtowanych przez ten sam ruch białka. Ujawniając, jak wiązanie wapnia, wewnętrzne przestawienia i wygięcie błony współdziałają, badanie dostarcza mapy pozwalającej zrozumieć choroby związane z TMEM16F i projektować leki, które mogą precyzyjnie regulować jego aktywność w procesach krzepnięcia, naprawy błon i infekcji wirusowych.
Cytowanie: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Słowa kluczowe: TMEM16F, przegregowywanie lipidów, kanały jonowe, błona komórkowa, sygnalizacja wapniowa