Clear Sky Science · he
הפעלת ה‑TMEM16F התלויה בסידן כסקראמלייזר וכנקודת תעלה יונית
מדוע השסתום הקטן הזה בממברנה חשוב
כל שנייה, הממברנות סביב תאי הגוף שלנו מסדרות באופן שקט מולקולות כדי לשמור על חיינו. שחקן שלא זוכה להרבה תשומת לב במאזן הזה הוא חלבון בשם TMEM16F. הוא מסייע בקרישת דם, מתקן ממברנות קרועות, מכווין תאי חיסון במוח, ואפילו מנוצל על ידי וירוסים כמו SARS‑CoV‑2 כדי לחדור לתאים. ועד כה, לא היה ברור כיצד החלבון נדלק וכיצד הוא מתחלף בין תפקוד כערוץ יוני לבין תפקוד כ"סקראמלייזר" של ליפידים שמתהפכים מצד לצד של הממברנה. המחקר הזה משתמש בהדמיה ברזולוציה גבוהה ובסימולציות ממוחשבות כדי לחשוף את תנועות העבודה של TMEM16F בפירוט חסר־תקדים.
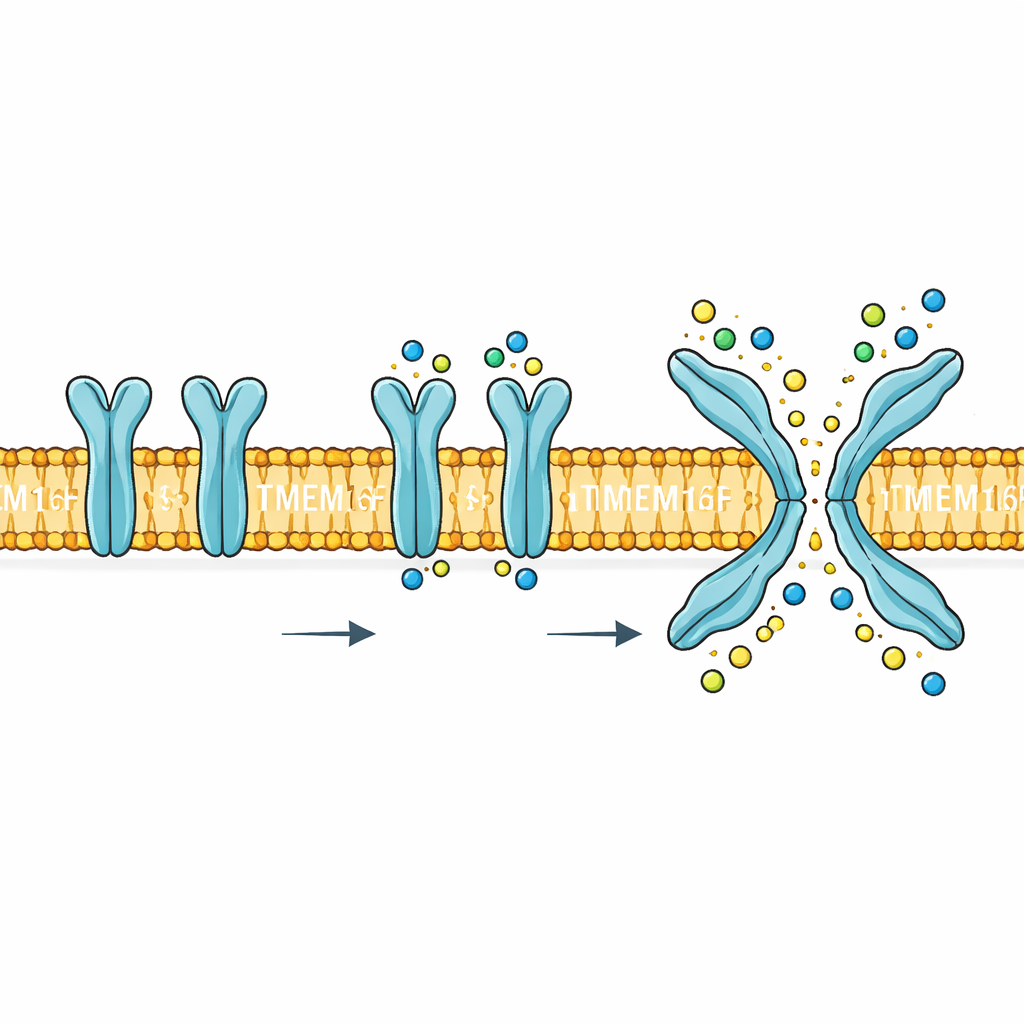
שסתום בעל מטרה כפולה בגבול התא
TMEM16F נמצא בממברנת התא החיצונית ומגיב לעליות בריכוז הסידן בתוך התא. כאשר הוא מופעל, הוא מבצע שתי משימות מאוד שונות. ראשית, הוא יוצר מסלול שמאפשר לחלקיקים טעונים קטנים כמו נתרן, אשלגן וכלור לעבור דרך הממברנה. שנית, הוא הופך ליפידים מסוימים, ובפרט פוספטידילסרין, מפני הממברנה הפנימיים אל פני השטח החיצוניים. שינוי זה של ליפידים הוא איתות ביולוגי רב‑עוצמה: הוא עוזר לטסיות להיווצר לקריש, מסמן תאים פגועים לפינוי, ויכול לשמש מניפולציה על ידי וירוסים לחדירה לתאים. מוטציות או ויסות לקוי של TMEM16F מקושרים לבעיות בדם, בעצם ובמערכת העצבים, מה שהופך את ההבנה של המנגנון ליותר מסקרנות — הוא יעד אפשרי לתרופות.
לראות את החלבון בסביבתו הטבעית
מחקרים מבניים קודמים בדקו את TMEM16F בסביבות מלאכותיות כמו דטרגנטים או נאנודיסקים, וראו תמיד מצב שנראה סגור, אפילו בנוכחות סידן. הדבר יצר חידה: ניסויים פונקציונליים הראו בבירור שהחלבון פעיל, אך המבנה שלו לא נראה ככזה שפותח מסלול ליונים או ליפידים. כדי לפתור את זה, החוקרים השיבו TMEM16F של עכבר לתוך בועיות ממברנה קטנות וצפות (ליפוזומים) שעשויות ליפידים פשוטים ומוגדרים היטב — אותה סוג סביבה שבה הם יכלו למדוד ישירות תנועת יונים והחלפת ליפידים. לאחר מכן השתמשו במיקרוסקופיה קריואלקטרונית כדי ללכוד מיליוני תמונות של החלבון, ומיינו אותן לצורות מובחנות המייצגות מצבי פעילות שונים.
כיצד הסידן מעצב מחדש את השסתום
בהעדר סידן, TMEM16F התקבל בשני צורות דומות ולא פעילות שבהן חריץ מרכזי דרך החלבון היה אטום חזק. כאשר נוספה סידן, החלבון נטה לצורה המקובלת של קשירה לסידן אך עדיין סגורה, ולצורה שנייה, נדירה אך בולטת ושונה מאוד. במצב הפעיל הזה, מקטע בחלבון שנקרא TM4 החל להחליק מול מקטע שכנה TM6, ויצר חריץ בצורת X שחוצה את הממברנה. החלק המרכזי של החריץ יצר נקב רציף מוקף בחלבון, רחב דיו עבור יונים חלקית מימיים, בעוד האזורים הקרובים לפני הממברנה נפתחו לקהילות רחבות יותר. החוקרים אימתו את חשיבות הקונפורמציה הזאת על‑ידי הנדסת מוטציות: אלו שדחפו את החלבון לעבר מצב בצורת X הקלו על ההחלפה של ליפידים, בעוד אלו שתקעו אותו בצורה הסגורה כמעט ביטלו את הפעילות.
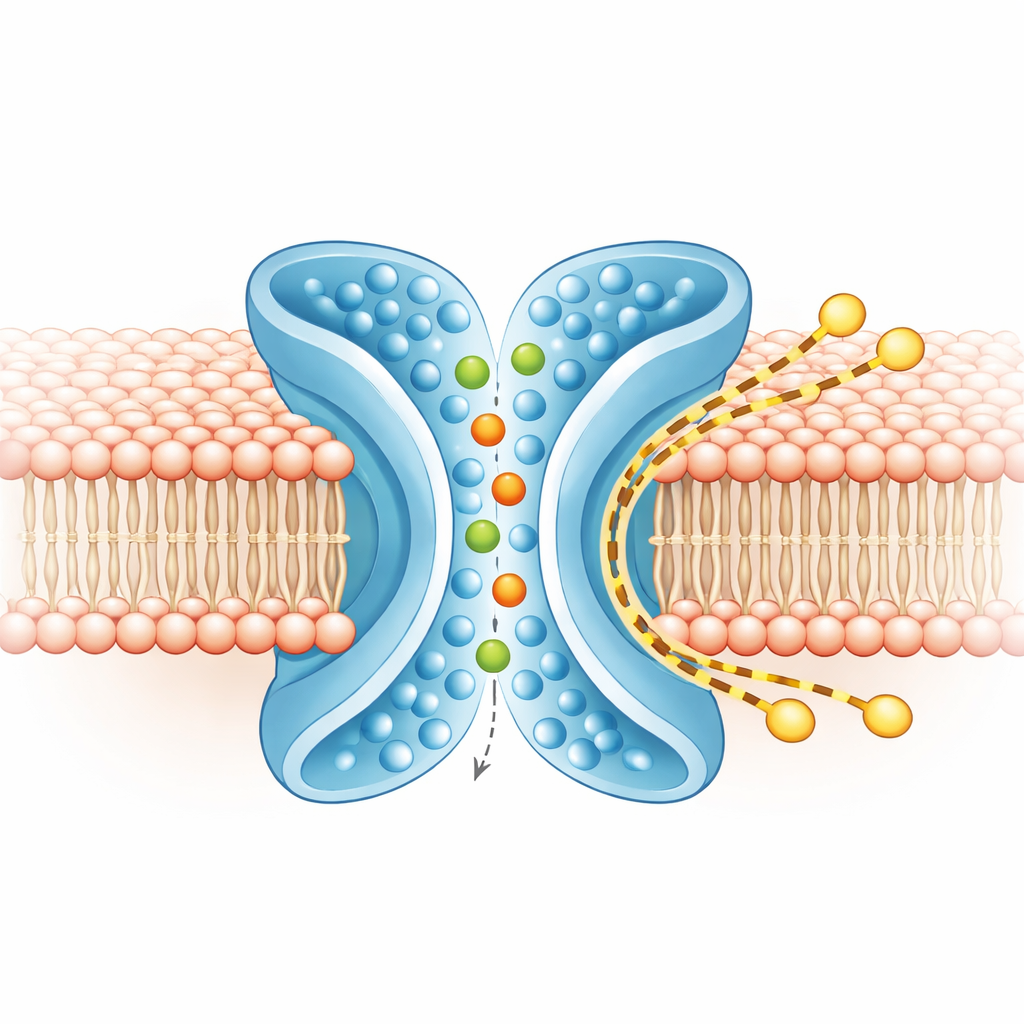
מסלולים נפרדים ליונים ולליפידים
כדי להבין מה נע ואליו, הצוות הריץ סימולציות ממוחשבות נרחבות של TMEM16F בממברנה ריאליסטית, הן בצורות הסגורות והן בפעילות. בצורה הפעילה בצורת X, יונים זחלו דרך הנקב המרכזי, נכנסים מכל צד ושומרים על רוב מעטפת המים שסביבן — דבר שתואם להעדפה הרופפת של החלבון בין קטיאונים לאניונים. באותו זמן, השכבה החיצונית של הממברנה סביב TM4 ו‑TM6 התקשטה ונמעכה. סימולציות בקנה מידה גס יותר, שרצו לזמנים ארוכים יותר, הראו מאות מולקולות ליפיד שחוצות מעלון אחד לשני לאורך הצד החיצוני של החריץ בצורת X, תוך עקיפה יחסית של הנקב הייניוני. מסלולי היונים והליפידים חופפו רק במידה מועטה, מה שמעיד שהחלבון מפעיל שני מסלולים נפרדים במידה רבה לצד זה לצד זה: פנימי ליונים וחיצוני לליפידים.
בקר גמיש הקשור לאותות תאיים
המחקר מגלה גם כיצד הדומיין הציטוזולי הפנימי של החלבון פועל כקישור מכני שממיר את קשירת הסידן לתנועות הגדולות האלה. במצב המנוחה, הדומיין הזה יוצר מבנה קומפקטי שמוחזק על‑ידי רשת "מנעולים" אלקטרוסטטיים בין חומצות אמינו ספציפיות. קשירת הסידן מיישרת את מקטע TM6 ומדחיקה דומיין זה; שבירת גשרים המלחים מאפשרת לחלק מהדומיין להסתובב מעלה ולהינעל על TM6. התנועה הזו מועברת לאזורי TM4–TM5, מה שגורם ל‑TM4 להחליק וליצור את החריץ בצורת X. מוטציות שמחלישות את המנעול מזרזות את ההחלפה, בעוד אלו שמעדיפות את המצב הסגור מאטות או חוסמות אותה.
מסקנות לגבי בריאות ומחלה
במונחים פשוטים, העבודה מראה ש‑TMEM16F הוא מכונה קטנה הנשלטת על‑ידי סידן שיכולה בבת אחת לפתוח "צינור" פנימי ליונים ולעצב את הממברנה סביבו כך שליפידים יחלפו דרכה. במקום לחלוק מסלול מעורב אחד, יונים וליפידים נוסעים ברובם על מסלולים נפרדים שמעוצבים על‑ידי אותה תנועת חלבון. על ידי חשיפת אופן שבו קשירת סידן, ארגונים פנימיים וכיפוף הממברנה פועלים בשיתוף, המחקר מספק מפת דרכים להבנת מחלות המקושרות ל‑TMEM16F ולפיתוח תרופות שיכולות לכוונן את פעילותו בקרישת דם, תיקון ממברנות וזיהומים ויראליים.
ציטוט: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
מילות מפתח: TMEM16F, החלפת ליפידים, תעלות יוניות, ממברנת תא, אותות סידן