Clear Sky Science · es
Activación dependiente del calcio de la escamblasa y canal iónico TMEM16F
Por qué importa esta pequeña válvula de la membrana
Cada segundo, las membranas que rodean nuestras células reorganizan silenciosamente moléculas para mantenernos con vida. Un actor poco reconocido en este acto de equilibrio es una proteína llamada TMEM16F. Ayuda a coagular la sangre, repara membranas desgarradas, guía a las células inmunitarias del cerebro e incluso es aprovechada por virus como el SARS‑CoV‑2 para infectar células. Sin embargo, hasta ahora los científicos no comprendían cómo esta proteína se activa y desactiva, ni cómo puede actuar tanto como canal iónico como “escamblasa” de lípidos que invierte moléculas grasas entre las dos caras de la membrana. Este estudio utiliza imágenes de alta resolución y simulaciones por ordenador para revelar los movimientos funcionales de TMEM16F con un detalle sin precedentes.
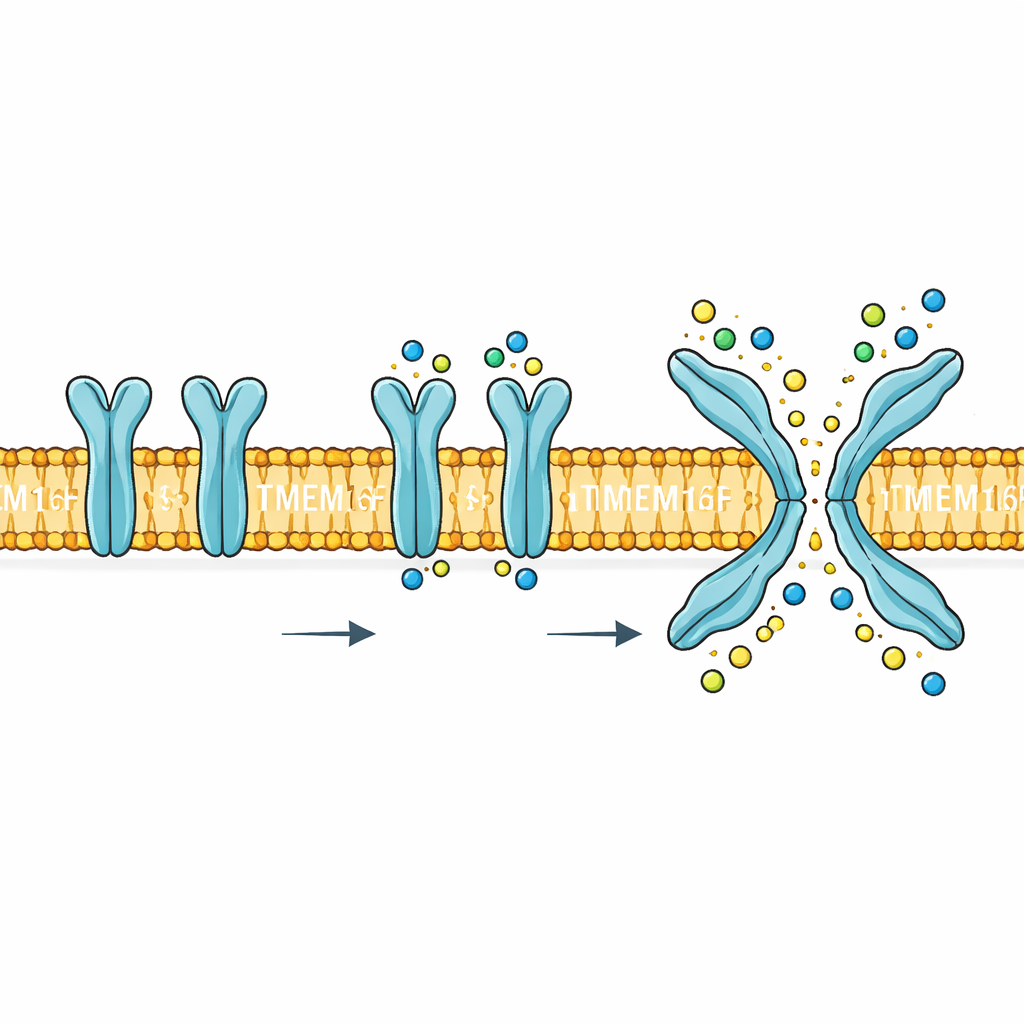
Una compuerta con doble propósito en el límite celular
TMEM16F se sitúa en la membrana externa de la célula y responde a los aumentos de calcio en el interior celular. Cuando se activa, realiza dos trabajos muy distintos. Primero, forma una vía que permite que partículas pequeñas cargadas, como sodio, potasio y cloruro, atraviesen la membrana. Segundo, invierte ciertos lípidos, especialmente la fosfatidilserina, desde la cara interna de la membrana hacia la externa. Este volteo de lípidos es una señal biológica potente: ayuda a que las plaquetas formen coágulos, marca células dañadas para su eliminación y puede ser explotado por virus para entrar en las células. Mutaciones o una regulación deficiente de TMEM16F se han vinculado a problemas en la sangre, los huesos y el sistema nervioso, lo que convierte su mecanismo en algo más que una curiosidad: es un potencial objetivo terapéutico.
Ver la proteína en su hábitat nativo
Estudios estructurales previos examinaron TMEM16F en entornos artificiales como detergentes o nanodiscos, y vieron de forma consistente lo que parecía un estado cerrado, incluso cuando había calcio presente. Esto planteó un enigma: los experimentos funcionales mostraban claramente que la proteína estaba activa, pero su estructura no parecía abrir una ruta para iones o lípidos. Para resolver esto, los autores reconstituyeron TMEM16F de ratón en pequeñas burbujas de membrana flotantes (liposomas) hechas de lípidos simples y bien definidos —el mismo tipo de entorno en el que podían medir directamente el movimiento de iones y el reordenamiento de lípidos. Luego usaron criomicroscopía electrónica para capturar millones de instantáneas de la proteína y las clasificaron en formas distintas que representan diferentes estados de actividad.
Cómo el calcio remodela la compuerta
En ausencia de calcio, TMEM16F adoptó dos formas inactivas similares en las que una ranura clave a través de la proteína estaba fuertemente sellada. Cuando se añadió calcio, la proteína favoreció una forma convencional ligada al calcio pero aún cerrada, y una segunda forma, más rara pero notablemente diferente. En este estado activo, un segmento de la proteína llamado TM4 se deslizó contra un segmento vecino, TM6, creando una ranura en forma de X que cruzaba la membrana. La parte central de esta ranura formó un poro continuo, delimitado por proteína, lo bastante ancho para iones parcialmente hidratados, mientras que las regiones más cercanas a las superficies de la membrana se abrieron en vestíbulos más amplios. Los investigadores confirmaron la importancia de esta conformación mediante ingeniería de mutaciones: aquellas que desplazaron la proteína hacia el estado en forma de X facilitaron el escambleo, mientras que las que la atraparon en la forma cerrada prácticamente abolieron la actividad.
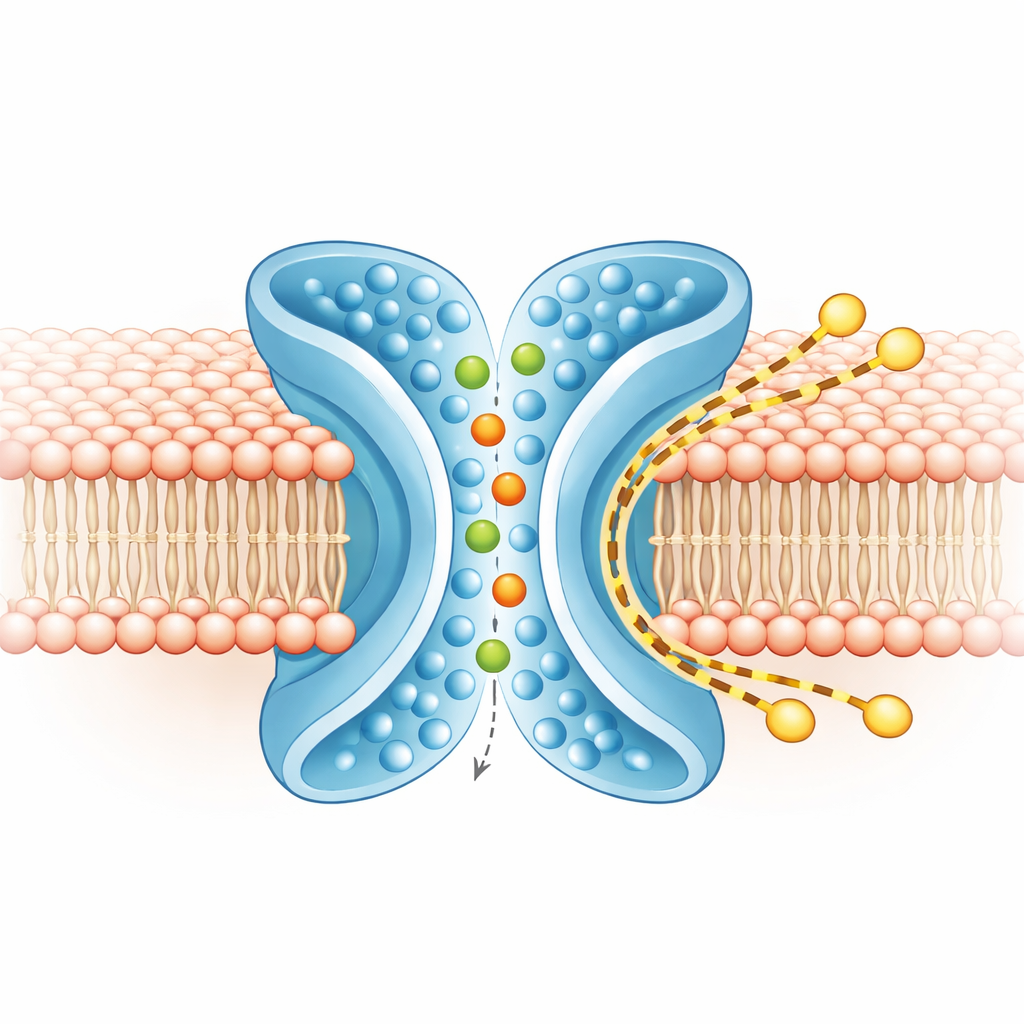
Pistas separadas para iones y lípidos
Para entender qué se mueve y por dónde, el equipo realizó extensas simulaciones por ordenador de TMEM16F en una membrana realista, tanto en las formas cerrada como activa. En la forma activa en X, los iones serpenteaban a través del poro central, entrando desde cualquiera de los lados y conservando la mayor parte de su capa de agua circundante, consistente con la preferencia laxa de la proteína entre cationes y aniones. Al mismo tiempo, la capa externa de la membrana alrededor de TM4 y TM6 se afinó y dobló. Simulaciones a grano grueso, ejecutadas durante tiempos más largos, mostraron cientos de moléculas lipídicas cruzando de una monocapa a la otra a lo largo del exterior de la ranura en X, en gran medida evitando el poro iónico. Las rutas de iones y lípidos se solaparon solo de forma mínima, lo que indica que la proteína gestiona dos pistas en gran parte independientes lado a lado: una interna para iones y otra externa para lípidos.
Un controlador flexible ligado a las señales celulares
El estudio también revela cómo el dominio interno citosólico de la proteína funciona como un enlace mecánico que convierte la unión de calcio en estos grandes movimientos. En el estado de reposo, este dominio forma una estructura compacta mantenida por una red de “cerrojos” electrostáticos entre aminoácidos específicos. La unión de calcio endereza el segmento TM6 y empuja este dominio; la ruptura de los puentes salinos permite que parte del dominio rote hacia arriba y se acople a TM6. Ese movimiento se transmite a la región TM4–TM5, provocando que TM4 se deslice y forme la ranura en forma de X. Mutaciones que debilitan el cerrojo aceleran el escambleo, mientras que las que favorecen el estado cerrado lo ralentizan o bloquean.
Qué significa esto para la salud y la enfermedad
En términos cotidianos, este trabajo muestra que TMEM16F es una pequeña máquina controlada por calcio que puede abrir simultáneamente una tubería interna para iones y modelar la membrana circundante para que los lípidos se deslicen a través de ella. En lugar de compartir una única vía mixta, iones y lípidos viajan mayormente por pistas separadas formadas por el mismo movimiento de la proteína. Al revelar cómo la unión de calcio, las reorganizaciones internas y la curvatura de la membrana cooperan, el estudio proporciona un plano para entender enfermedades vinculadas a TMEM16F y para diseñar fármacos que puedan afinar su actividad en la coagulación, la reparación de membranas y las infecciones virales.
Cita: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Palabras clave: TMEM16F, reordenamiento de lípidos, canales iónicos, membrana celular, señalización por calcio