Clear Sky Science · pt
Ativação dependente de cálcio do scramblase e canal iônico TMEM16F
Por que essa pequena válvula da membrana importa
Cada segundo, as membranas ao redor de nossas células silenciosamente reorganizam moléculas para nos manter vivos. Um ator pouco celebrado nesse equilíbrio é uma proteína chamada TMEM16F. Ela auxilia na coagulação do sangue, repara membranas rompidas, orienta células imunes do cérebro e até é sequestrada por vírus como o SARS‑CoV‑2 para infectar células. Ainda assim, até agora, os cientistas não entendiam como essa proteína liga e desliga sua função, ou como pode atuar tanto como canal iônico quanto como um “scrambler” de lipídios que inverte moléculas gordurosas entre os dois lados da membrana. Este estudo usa imagens de alta resolução e simulações computacionais para revelar os movimentos de trabalho do TMEM16F com detalhes sem precedentes.
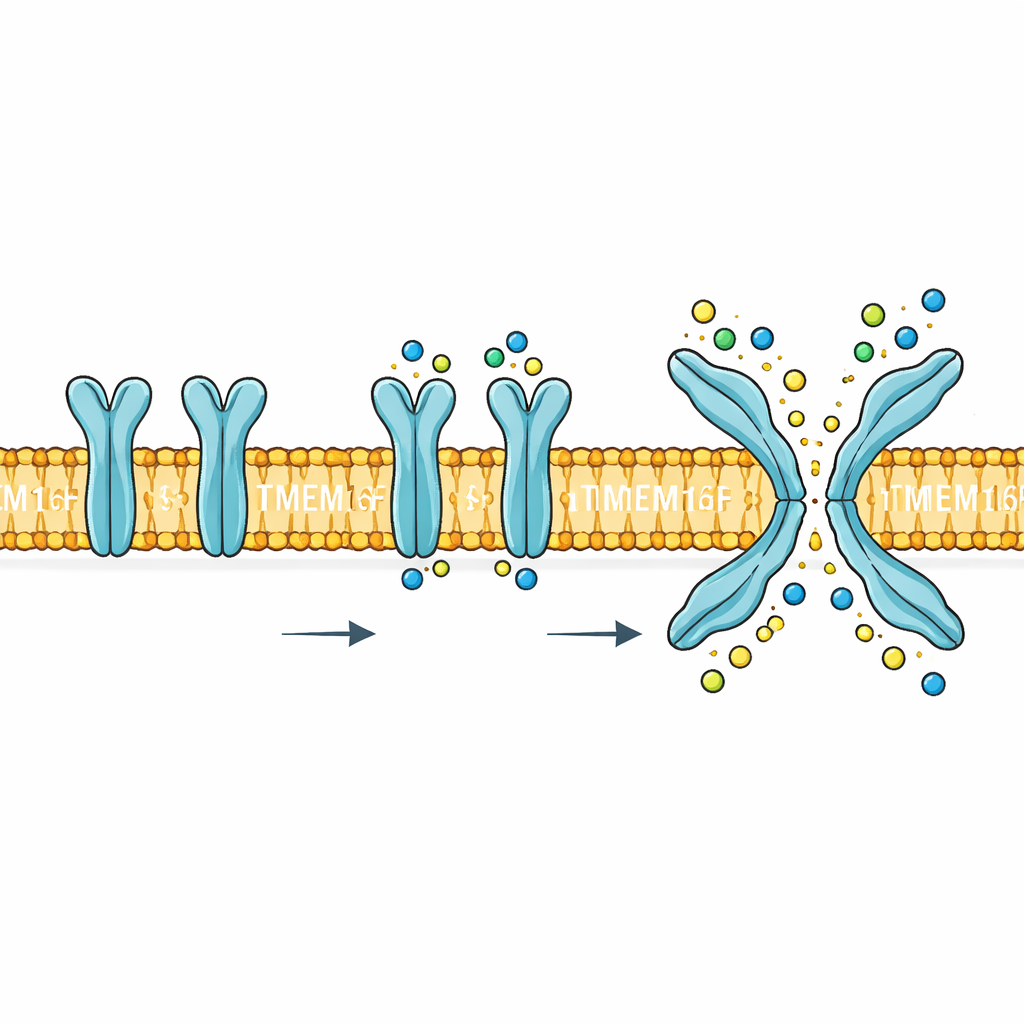
Um portão de dupla função na fronteira celular
O TMEM16F fica na membrana externa da célula e responde a aumentos de cálcio no interior celular. Quando ativado, ele desempenha duas funções muito diferentes. Primeiro, forma um caminho que permite que pequenas partículas carregadas como sódio, potássio e cloreto atravessem a membrana. Segundo, inverte certos lipídios, especialmente a fosfatidilserina, da face interna da membrana para a face externa. Essa inversão lipídica é um sinal biológico poderoso: ajuda plaquetas a formarem coágulos, marca células danificadas para serem removidas e pode ser explorada por vírus para entrar nas células. Mutações ou desregulação do TMEM16F estão associadas a problemas no sangue, nos ossos e no sistema nervoso, tornando seu mecanismo mais do que uma curiosidade — é um alvo potencial para fármacos.
Vendo a proteína em seu habitat nativo
Estudos estruturais anteriores examinaram o TMEM16F em ambientes artificiais como detergentes ou nanodiscos, e consistentemente o observaram em um estado que parecia fechado, mesmo quando o cálcio estava presente. Isso gerou um enigma: experimentos funcionais mostravam claramente que a proteína estava ativa, mas sua estrutura não parecia abrir uma rota para íons ou lipídios. Para resolver isso, os autores reconstituíram o TMEM16F de camundongo em pequenas bolhas de membrana livres (lipossomos) feitas de lipídios simples e bem definidos — o mesmo tipo de ambiente no qual podiam medir diretamente o movimento de íons e o embaralhamento de lipídios. Em seguida, usaram criomicroscopia eletrônica para capturar milhões de instantâneos da proteína e classificaram esses instantâneos em formas distintas que representam diferentes estados de atividade.
Como o cálcio remodela o portão
Na ausência de cálcio, o TMEM16F adotava duas formas inativas semelhantes nas quais um sulco chave através da proteína estava firmemente selado. Quando o cálcio foi adicionado, a proteína favoreceu uma forma convencional ligada ao cálcio, mas ainda fechada, e uma segunda forma, mais rara porém dramaticamente diferente. Nesse estado ativo, um segmento da proteína chamado TM4 deslizou junto a um segmento vizinho, TM6, criando um sulco em forma de X que atravessou a membrana. A parte central desse sulco formou um poro contínuo, delimitado pela proteína, largo o suficiente para íons parcialmente hidratados, enquanto as regiões mais próximas às superfícies da membrana abriram em vestíbulos mais amplos. Os pesquisadores confirmaram a importância dessa conformação ao introduzir mutações: aquelas que deslocaram a proteína para o estado em X facilitaram o embaralhamento, enquanto as que a prenderam na forma fechada quase aboliram a atividade.
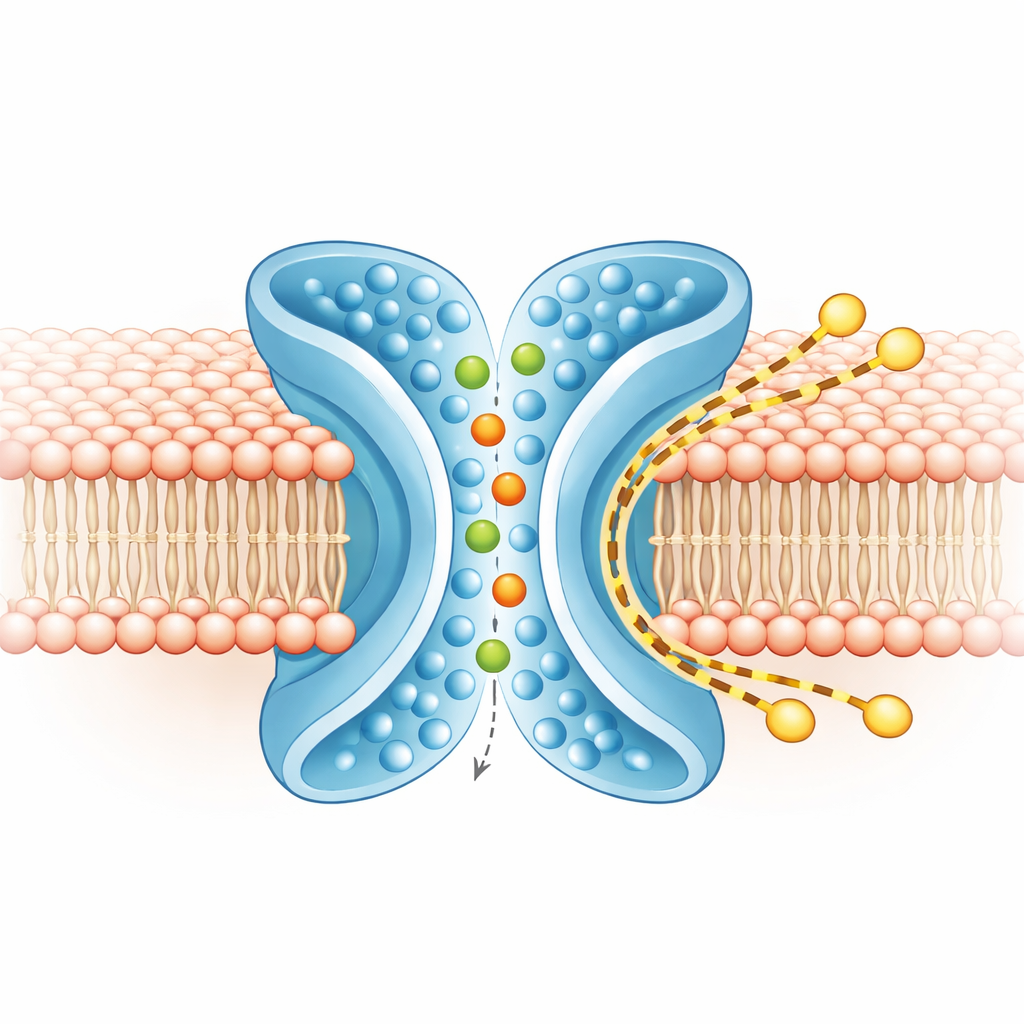
Pistas separadas para íons e lipídios
Para entender o que se move e por onde, a equipe executou extensas simulações computacionais do TMEM16F em uma membrana realista, tanto nas formas fechada quanto ativa. Na forma ativa em X, os íons serpentearam pelo poro central, entrando de ambos os lados e mantendo a maior parte de sua camada de água circundante, compatível com a preferência frouxa da proteína entre íons positivos e negativos. Ao mesmo tempo, a camada externa da membrana em torno de TM4 e TM6 afinou e dobrou. Simulações em nível coarse‑grained, rodadas por tempos mais longos, mostraram centenas de moléculas lipídicas cruzando de uma folha para a outra ao longo do exterior do sulco em X, em grande parte evitando o poro de íons. As rotas de íons e lipídios se sobrepunham minimamente, indicando que a proteína opera duas trilhas em grande parte independentes lado a lado: uma interna para íons e outra externa para lipídios.
Um controlador flexível ligado a sinais celulares
O estudo também revela como o domínio interno citosólico da proteína funciona como uma ligação mecânica que converte a ligação do cálcio nesses grandes movimentos. No estado de repouso, esse domínio forma uma estrutura compacta mantida por uma rede de “trancas” eletrostáticas entre aminoácidos específicos. A ligação do cálcio endireita o segmento TM6 e empurra esse domínio; a quebra dessas travas salinas permite que parte do domínio gire para cima e se prenda ao TM6. Esse movimento é transmitido à região TM4–TM5, fazendo com que o TM4 deslize e forme o sulco em X. Mutações que enfraquecem a trava aceleram o embaralhamento, enquanto aquelas que favorecem o estado fechado retardam ou bloqueiam a atividade.
O que isso significa para saúde e doença
Em termos práticos, este trabalho mostra que o TMEM16F é uma pequena máquina controlada por cálcio que pode simultaneamente abrir um canal interno para íons e moldar a membrana circundante para que lipídios deslizem através dela. Em vez de compartilharem um único caminho misto, íons e lipídios viajam majoritariamente por trilhas separadas moldadas pelo mesmo movimento da proteína. Ao revelar como a ligação do cálcio, os rearranjos internos e a curvatura da membrana cooperam, o estudo fornece um roteiro para entender doenças ligadas ao TMEM16F e para projetar fármacos que possam ajustar com precisão sua atividade na coagulação, reparo de membranas e infecções virais.
Citação: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Palavras-chave: TMEM16F, embaralhamento de lipídios, canais iônicos, membrana celular, sinalização por cálcio