Clear Sky Science · tr
TMEM16F skramblaz ve iyon kanalıın kalsiyuma bağımlı aktivasyonu
Bu küçük zar valfinin neden önemli olduğu
Her saniye, hücrelerimizin çevresindeki zarlar hayatta kalmamız için molekülleri sessizce yeniden düzenler. Bu dengenin göz ardı edilen oyuncularından biri TMEM16F adlı bir proteindir. Kanın pıhtılaşmasına yardımcı olur, yırtılmış zarları onarır, beyin bağışıklık hücrelerini yönlendirir ve hatta SARS‑CoV‑2 gibi virüsler tarafından hücreleri enfekte etmek için ele geçirilebilir. Yine de, şimdiye kadar bilim insanları bu proteinin nasıl açılıp kapandığını veya nasıl hem iyon kanalı hem de zarın iki yüzü arasında yağ moleküllerini çeviren bir lipid “skramblaz” olarak nasıl davranabildiğini anlamamıştı. Bu çalışma, yüksek çözünürlüklü görüntüleme ve bilgisayar simülasyonlarını kullanarak TMEM16F’nin çalışma hareketlerini eşi görülmemiş ayrıntıyla ortaya koyuyor.
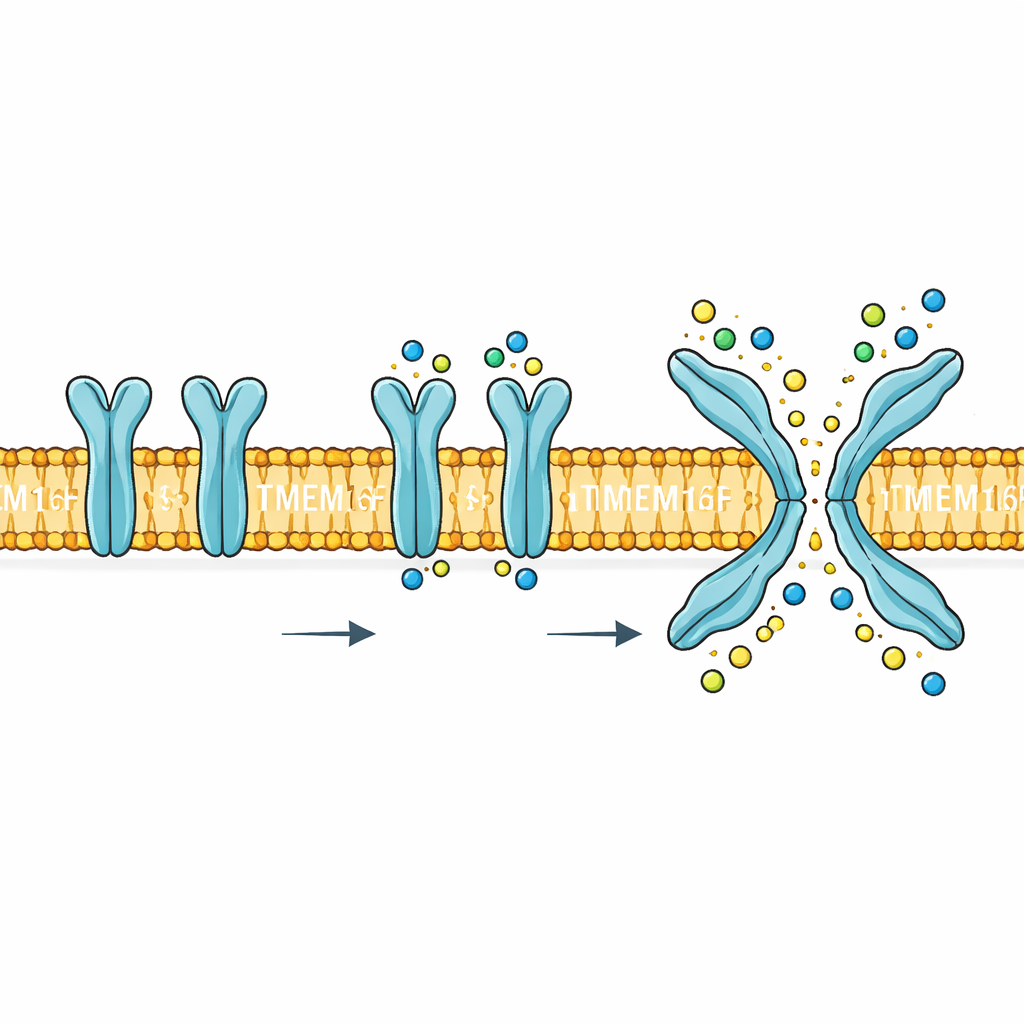
Hücre sınırında çift amaçlı bir kapı
TMEM16F hücrenin dış zarında konumlanır ve hücre içindeki kalsiyum artışlarına yanıt verir. Aktive olduğunda, iki çok farklı işi yapar. İlk olarak, sodyum, potasyum ve klorür gibi küçük yüklü parçacıkların zarı geçmesine izin veren bir yol oluşturur. İkinci olarak, özellikle fosfatidilserin olmak üzere belirli lipidleri zarın iç yüzeyinden dış yüzeyine çevirir. Bu lipid dönüşümü güçlü bir biyolojik işarettir: trombositlerin pıhtılaşmasına yardımcı olur, hasarlı hücreleri ortadan kaldırılmaları için işaretler ve virüslerin hücrelere girişini kolaylaştırmak üzere kullanılabilir. TMEM16F’deki mutasyonlar veya yanlış düzenleme kan, kemik ve sinir sistemi sorunlarıyla ilişkilendirilmiştir; dolayısıyla mekanizması yalnızca bir merak değil—potansiyel bir ilaç hedefidir.
Proteini doğal ortamında görmek
Önceki yapısal çalışmalar TMEM16F’yi deterjanlar veya nanodiskler gibi yapay ortamlarda inceledi ve kalsiyum olsa bile genellikle kapalı gibi görünen bir durumda tespit etti. Bu bir çelişki yarattı: fonksiyonel deneyler proteinin aktif olduğunu açıkça gösteriyordu, ancak yapısı iyonlar veya lipidler için bir yol açmıyor gibiydi. Bunu çözmek için yazarlar, fare TMEM16F’sini basit, iyi tanımlanmış lipidlerden yapılmış, serbest yüzen küçük zar kabarcıkları (liposome’lar) içine yeniden oluşturdular—iyon hareketini ve lipid karıştırmayı doğrudan ölçebildikleri aynı tür ortam. Ardından proteinlerin milyonlarca anlık görüntüsünü yakalamak için kriyo‑elektron mikroskobu kullandılar ve bunları farklı aktivite durumlarını temsil eden ayrı şekillere ayırdılar.
Kalsiyum kapıyı nasıl yeniden şekillendiriyor
Kalsiyum yokluğunda, TMEM16F anahtar bir oluğun sıkıca kapalı olduğu iki benzer, inaktif şekil benimsiyordu. Kalsiyum eklendiğinde, protein konvansiyonel kalsiyum bağlı ama hâlâ kapalı bir formu ve ikinci, daha nadir ama çarpıcı şekilde farklı bir formu tercih etti. Bu aktif durumda, TM4 adı verilen bir segment komşu TM6 segmentine karşı kayarak zar boyunca geçen X biçimli bir oluk oluşturdu. Bu oluğun merkezi kısmı, kısmen hidrate iyonlar için yeterince geniş, protein duvarlı sürekli bir gözenek oluştururken, zar yüzeylerine daha yakın bölgeler daha geniş vestibüller açtı. Araştırmacılar bu konformasyonun önemini mutasyonlar oluşturarak doğruladı: proteini X‑şeklindeki duruma kaydıran değişiklikler karıştırmayı kolaylaştırırken, onu kapalı formda sıkıştıranlar aktiviteyi neredeyse ortadan kaldırdı.
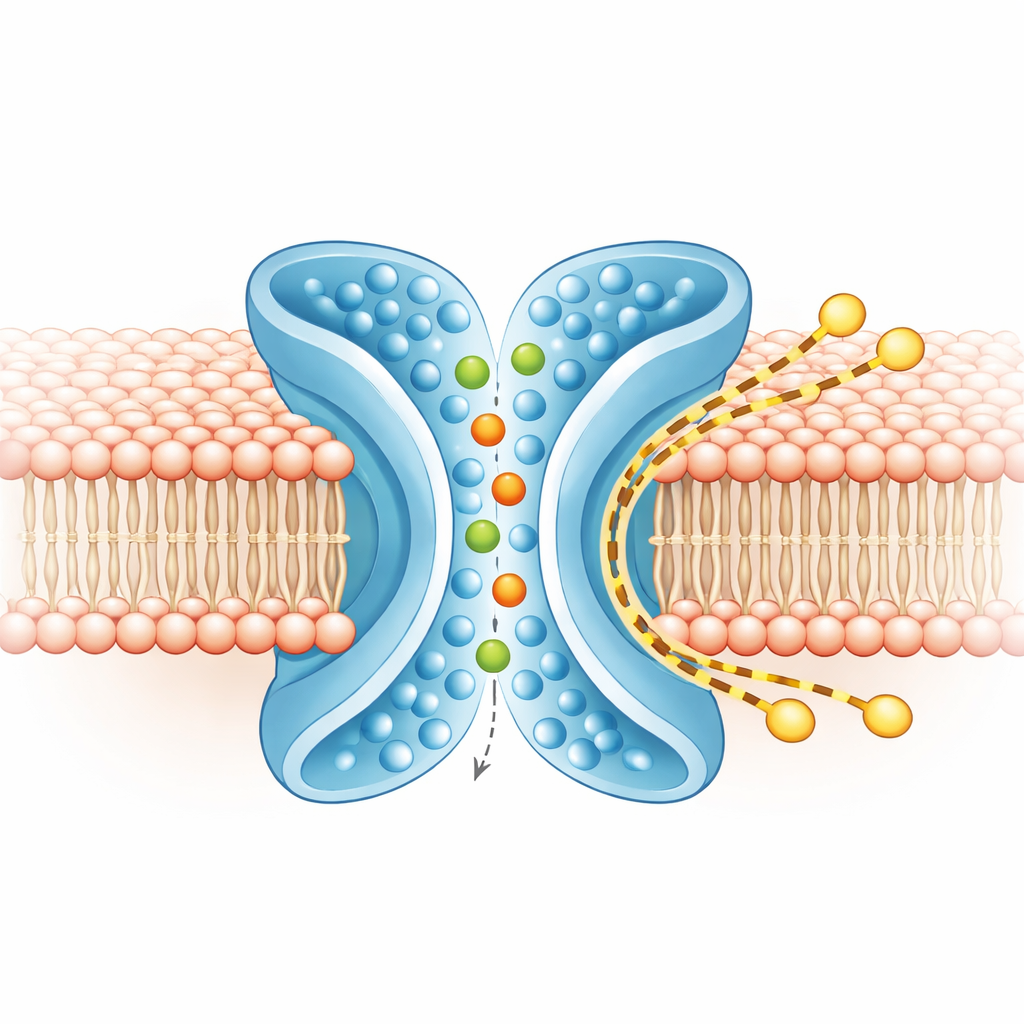
İyonlar ve lipidler için ayrı yollar
Hangi şeyin nerede hareket ettiğini anlamak için ekip, gerçekçi bir zarda hem kapalı hem de aktif şekillerde TMEM16F’nin geniş bilgisayar simülasyonlarını çalıştırdı. Aktif, X‑şeklindeki formda iyonlar merkezi gözenekten kıvrılarak geçiyor, her iki taraftan giriyor ve çevresindeki su kabuğunun çoğunu koruyordu; bu, proteinin pozitif ve negatif iyonlar arasında gevşek tercihini tutarlı kılıyordu. Aynı zamanda, TM4 ve TM6 çevresindeki zarın dış katmanı inceldi ve büküldü. Daha uzun zamanlarda çalıştırılan kaba taneli (coarse‑grained) simülasyonlar, X‑şekilli oluğun dışı boyunca yüzlerce lipid molekülünün bir yapraktan diğerine geçtiğini gösterdi; bu yol büyük ölçüde iyon gözenekten kaçınıyordu. İyonların ve lipidlerin rotaları yalnızca asgari düzeyde örtüştü; bu da proteinin yan yana iki büyük ölçüde bağımsız hattı çalıştırdığını gösteriyor: iyonlar için içsel bir hat ve lipidler için dışsal bir hat.
Hücre sinyallerine bağlı esnek bir kumanda
Çalışma ayrıca proteinin içsel, sitozolik domaininin kalsiyum bağlanmasını bu büyük hareketlere dönüştüren mekanik bir bağlantı gibi nasıl çalıştığını ortaya koyuyor. Dinlenme durumunda bu domain, belirli aminoasitler arasındaki elektrostatik “kilitler” ağıyla bir arada tutulan kompakt bir yapı oluşturur. Kalsiyum bağlanması TM6 segmentini düzleştirir ve bu domaini iter; tuz köprüsü kilitlerinin kırılması domainin bir kısmının yukarı doğru dönmesine ve TM6’ya tutunmasına izin verir. Bu hareket TM4–TM5 bölgesine iletilir, TM4’ün kaymasına ve X‑şekilli oluğun oluşmasına neden olur. Kilidi zayıflatan mutasyonlar karıştırmayı hızlandırırken, kapalı durumu destekleyenler bunu yavaşlatır veya engeller.
Sağlık ve hastalık için anlamı
Günlük terimlerle, bu çalışma TMEM16F’nin aynı anda iyonlar için içsel bir boruyu açabilen ve lipidlerin üzerinden kayabilmesi için çevreleyen zarı şekillendiren küçük, kalsiyum kontrollü bir makine olduğunu gösteriyor. Tek bir karışık yol paylaşmak yerine iyonlar ve lipidler çoğunlukla aynı protein hareketiyle şekillenen ayrı yollar üzerinde yol alır. Kalsiyum bağlanmasının, içsel yeniden düzenlemelerin ve zar bükülmesinin nasıl iş birliği yaptığını ortaya koyarak çalışma, TMEM16F ile ilişkili hastalıkları anlamak ve kan pıhtılaşması, zar onarımı ve viral enfeksiyonlarda aktivitesini ince ayarlayabilecek ilaçlar tasarlamak için bir şablon sağlıyor.
Atıf: Feng, Z., Alvarenga, O.E., Di Zanni, E. et al. Calcium dependent activation of the TMEM16F scramblase and ion channel. Nat Struct Mol Biol 33, 664–676 (2026). https://doi.org/10.1038/s41594-026-01789-5
Anahtar kelimeler: TMEM16F, lipid karıştırma, iyon kanalları, hücre zarı, kalsiyum sinyalleşmesi