Clear Sky Science · zh
在吞噬凋亡细胞过程中,Notch从接触位点被排斥限制了抗癌免疫
当清理队让抗癌战士沉默
我们的身体不断清除垂死细胞以维持组织的健康与平稳。但在肿瘤内部,这一相同的清理过程有时会适得其反,在我们最需要免疫系统作战的时候反而让它平静下来:在对抗癌症的过程中。本研究揭示了免疫细胞内一个隐藏的开关,决定细胞清理是会使免疫反应沉睡,还是帮助唤醒它去攻击肿瘤。
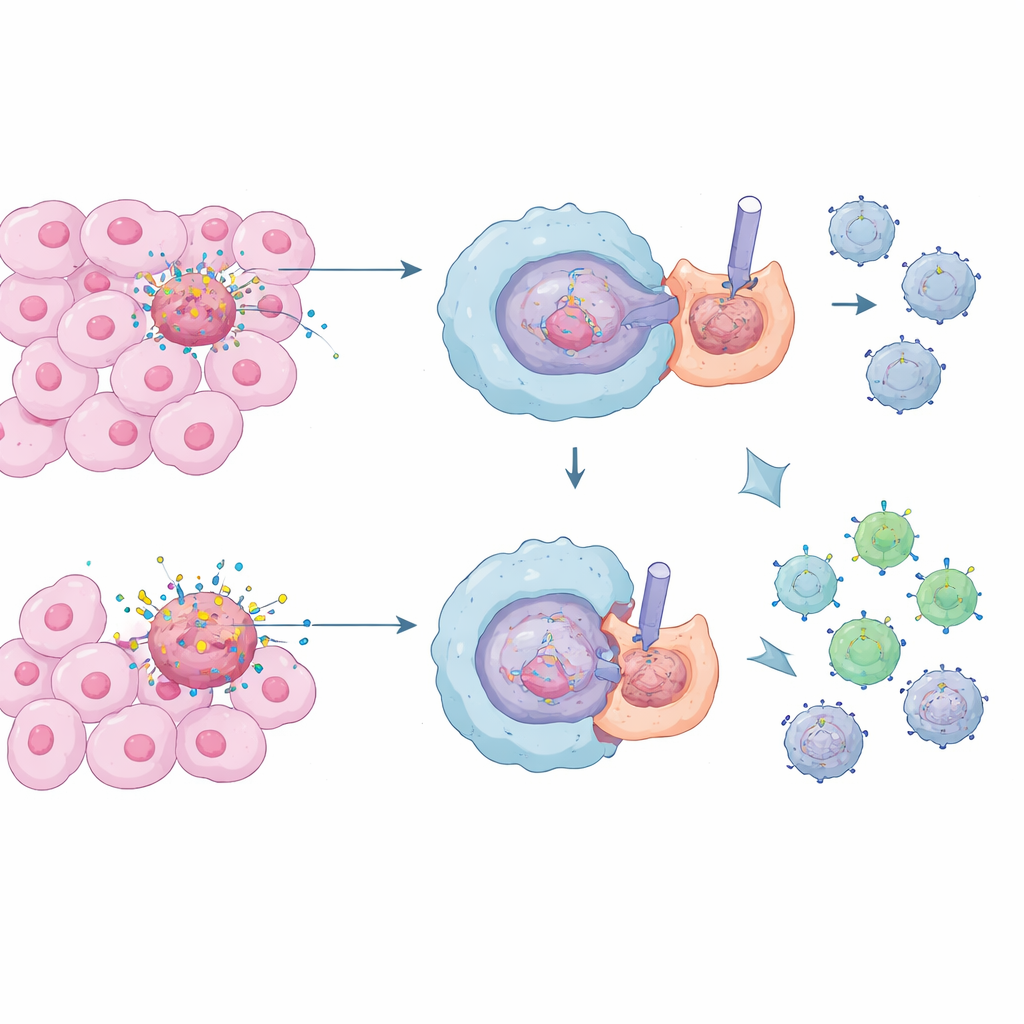
身体的清道夫及其无声工作
被称为巨噬细胞的特殊免疫细胞充当身体的清道夫,通过一种称为“吞噬凋亡细胞”(efferocytosis)的过程吞噬并消化死亡或即将死亡的细胞。在正常情况下,这一过程至关重要:它防止有毒细胞内容物泄漏并抑制炎症,从而保护我们免受慢性组织损伤和自身免疫疾病。在肿瘤内部,细胞持续大量死亡。默默清理这些尸体的巨噬细胞可能在肿瘤周围形成一个平静、抑制性的环境,使杀伤性T细胞更难识别和消灭恶性细胞。
巨噬细胞上的一个隐藏信号门
研究人员聚焦于一种称为Notch的通讯系统,它帮助细胞根据邻近细胞的信号决定行为。在巨噬细胞中,Notch活性倾向于将它们推向更具炎性和抗肿瘤的状态。令人惊讶的是,研究团队发现,当健康的巨噬细胞吞噬死细胞时,它们会在接触点主动关闭Notch信号。他们发现一个围绕Rubicon(RUBCN)分子的蛋白复合体与另一种酶VPS34协同,在巨噬细胞的外膜上建立了一个物理“屏障”。这个屏障由活化的整合素构成——这些抓握蛋白重排成一个紧密的环——物理地把体积较大的Notch受体从死细胞接触巨噬细胞的那一贴片上推开,使得Notch无法被开启。
打破屏障以增强免疫攻击
当科学家从巨噬细胞中移除Rubicon,或阻断下游酶磷脂酶D(PLD)时,这个整合素环便无法正常形成。没有了屏障,Notch受体可以移动到接触区并与死细胞表面的配对配体结合。在小鼠实验中,缺乏髓系细胞中Rubicon的动物,或接受PLD抑制药物处理的动物,其肿瘤内巨噬细胞显示出更强的Notch活性、更多的炎症相关基因程序,以及大量杀癌的CD8 T细胞和自然杀伤细胞浸润肿瘤。因此,肿瘤生长速度减慢。
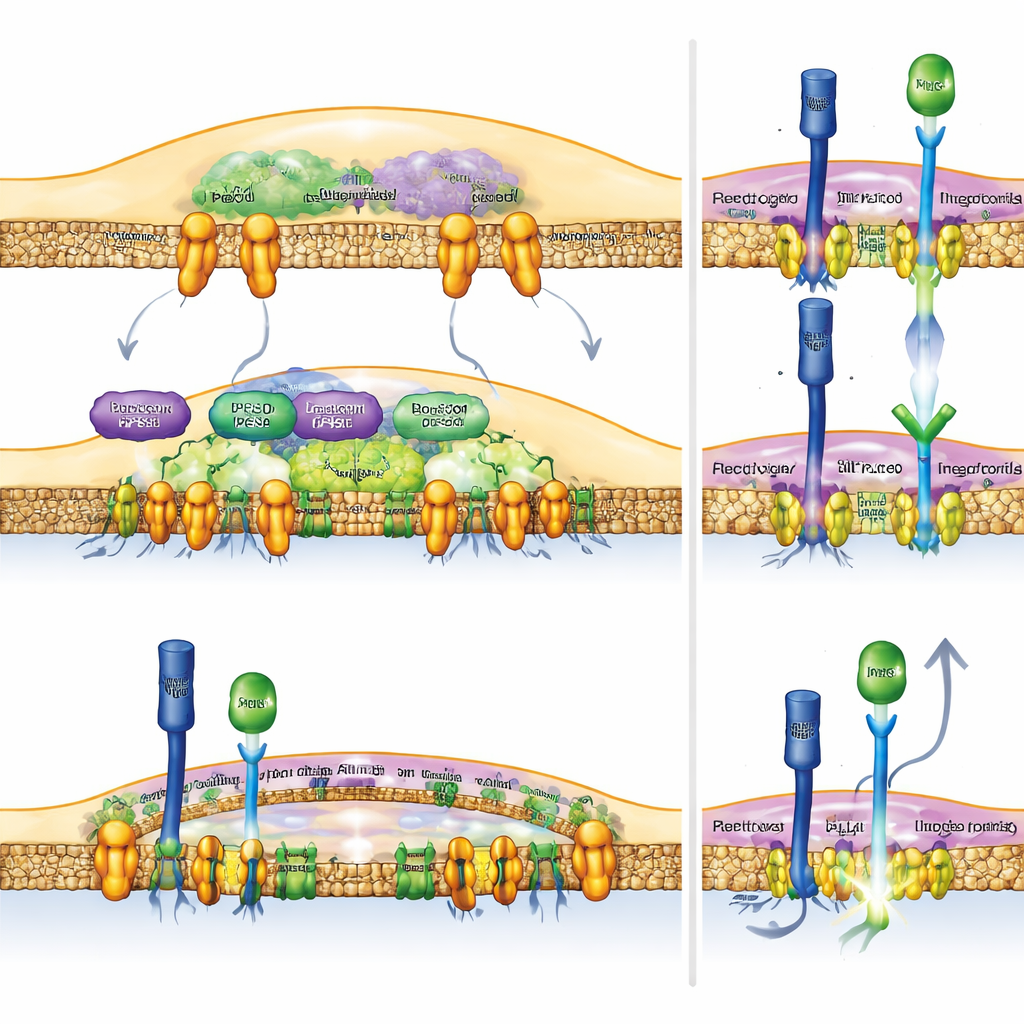
将Notch作为激发抗癌免疫的杠杆
为检验直接提高巨噬细胞中Notch是否足以帮助免疫系统,团队构建了髓系细胞持续产生活性Notch受体片段的小鼠。这些小鼠产生了更强的抗肿瘤反应:其肿瘤更小,肿瘤内的T细胞携带更多摧毁癌细胞所需的分子武器。重要的是,当研究者失活了RBPJ——Notch激活其靶基因所需的关键伙伴——Rubicon缺失或PLD抑制带来的益处便消失了。这表明这些干预的抗肿瘤效应依赖于巨噬细胞中完整的Notch信号,而非无关的附带效应。
来自人类肿瘤的线索与未来方向
在对数千例人类肿瘤数据的分析中,作者发现那些肿瘤表达高水平Notch激活配体但Rubicon水平较低的患者,通常比Rubicon水平高的患者存活更久。尽管这种分析不能证明因果关系,但这一发现与这样一个观点相符合:阻断肿瘤微环境中排斥Notch的屏障可以将平衡倾向于更有效的免疫监视。该研究提示,靶向Rubicon依赖的吞噬凋亡通路或PLD的药物,未来可能与现有免疫疗法联用,使巨噬细胞从沉默的垃圾收集者转变为抗癌的积极盟友。
这对患者意味着什么
简单来说,研究揭示了巨噬细胞携带一种内建门控机制,通常把一种关键的促免疫信号Notch隔离在它们吞噬死细胞的接触位点之外。这有助于保护健康组织免受不必要的炎症,但可能无意中屏蔽肿瘤。通过破坏这个门控——无论是通过基因改变还是药物治疗——研究人员可以让Notch信号通过,重新编程巨噬细胞以动员T细胞和其他防御者对抗癌症。尽管在这些发现转化为治疗方案之前仍需大量工作,但它们指向了一个新策略:除了直接增强T细胞外,我们或许还可以重构清理队,使其停止压制而开始放大体内的抗癌警报。
引用: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
关键词: 吞噬凋亡细胞(efferocytosis), Notch 信号, 巨噬细胞, 肿瘤微环境, 癌症免疫治疗