Clear Sky Science · it
Esclusione di Notch dal sito di contatto durante l’efferocitosi limita l’immunità anticancro
Quando le squadre di pulizia zittiscono i combattenti contro il cancro
I nostri corpi eliminano costantemente le cellule morenti per mantenere i tessuti sani e silenziosi. Ma all’interno dei tumori questo stesso processo di pulizia può ritorcersi contro, calmando il sistema immunitario proprio quando ne avremmo più bisogno: durante la lotta contro il cancro. Questo studio scopre un interruttore nascosto nelle cellule immunitarie che decide se la rimozione delle cellule farà assopire la risposta immunitaria oppure contribuirà a risvegliarla per attaccare i tumori.
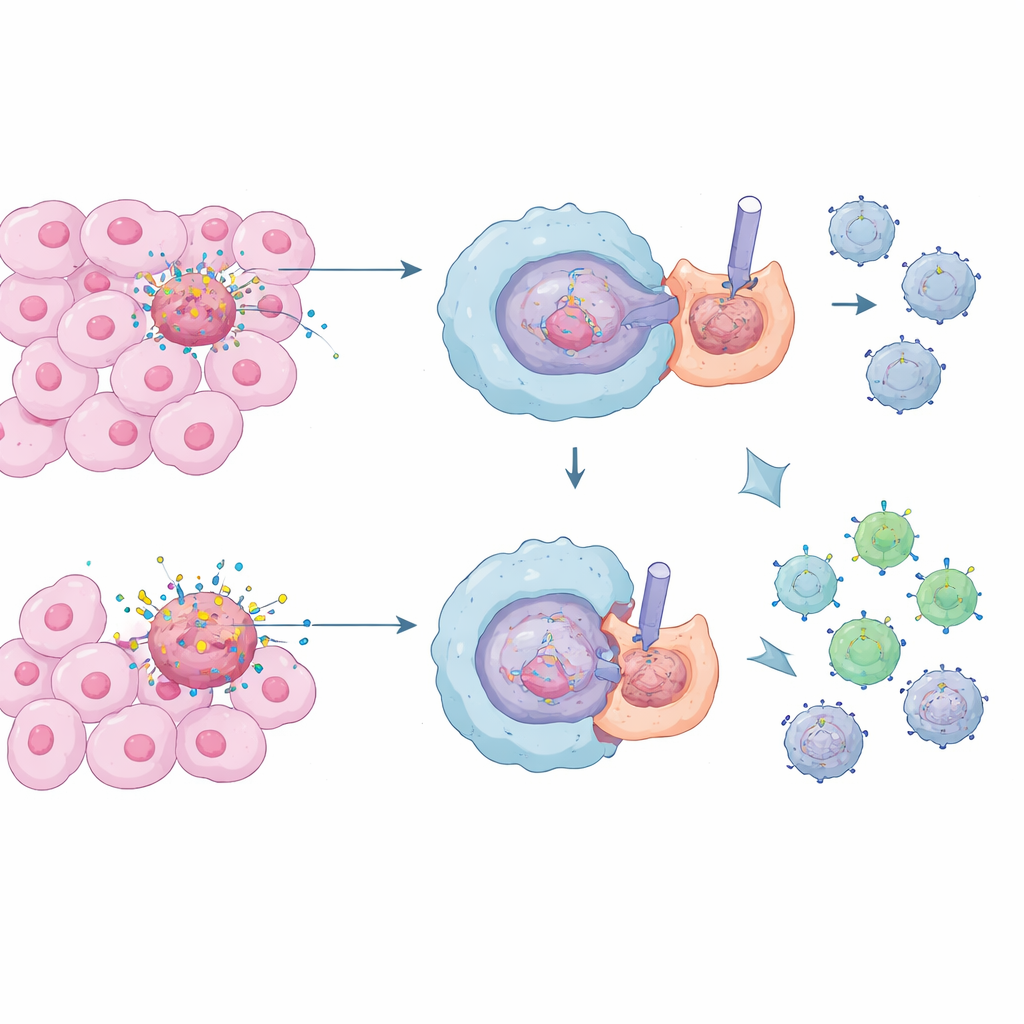
Gli spazzini del corpo e il loro lavoro silenzioso
Cellule immunitarie speciali chiamate macrofagi agiscono come gli spazzini del corpo, inghiottendo e digerendo cellule morte e morenti in un processo noto come efferocitosi. In condizioni normali questo è vitale: previene fuoriuscite di contenuti cellulari tossici e mantiene sotto controllo l’infiammazione, proteggendoci da danni tissutali cronici e malattie autoimmuni. Nei tumori, tuttavia, vi è una tempesta costante di morte cellulare. I macrofagi che puliscono in silenzio questi cadaveri possono finire per creare un quartiere calmo e soppressivo attorno al cancro, rendendo più difficile per le cellule T citotossiche riconoscere e distruggere le cellule maligne.
Un cancello segreto del segnale sui macrofagi
I ricercatori si sono concentrati su un sistema di comunicazione chiamato Notch, che aiuta le cellule a decidere come comportarsi in base ai segnali dei vicini. Nei macrofagi, l’attività di Notch tende a spingerli verso uno stato più infiammatorio e antitumorale. Sorprendentemente, il team ha scoperto che quando i macrofagi sani inglobano cellule morte, spengono attivamente la segnalazione Notch proprio nel punto di contatto. Hanno scoperto che un complesso proteico costruito attorno a una molecola chiamata Rubicon (RUBCN) si associa a un altro enzima, VPS34, per allestire una “barriera” fisica nella membrana esterna del macrofago. Questa barriera è costituita da integrine attivate—proteine di presa che si riorganizzano in un anello stretto—che spingono letteralmente i voluminisi recettori Notch lontano dalla zona di contatto con la cellula morta, impedendo così l’attivazione di Notch.
Rompere la barriera per potenziare l’attacco immunitario
Quando gli scienziati hanno rimosso Rubicon dai macrofagi, o hanno bloccato un enzima a valle chiamato fosfolipasi D (PLD), questo anello di integrine non si è più formato correttamente. Senza la barriera, i recettori Notch potevano spostarsi nella zona di contatto e interagire con i ligandi corrispondenti sulla superficie della cellula morta. Nei topi, i tumori che crescevano in animali privi di Rubicon nelle cellule mieloidi—or trattati con farmaci che inibiscono PLD—mostravano una maggiore attività di Notch all’interno dei macrofagi, programmi genici più infiammatori e un’ondata di cellule CD8 citotossiche e cellule NK infiltranti il tumore. Di conseguenza, i tumori crescevano più lentamente.
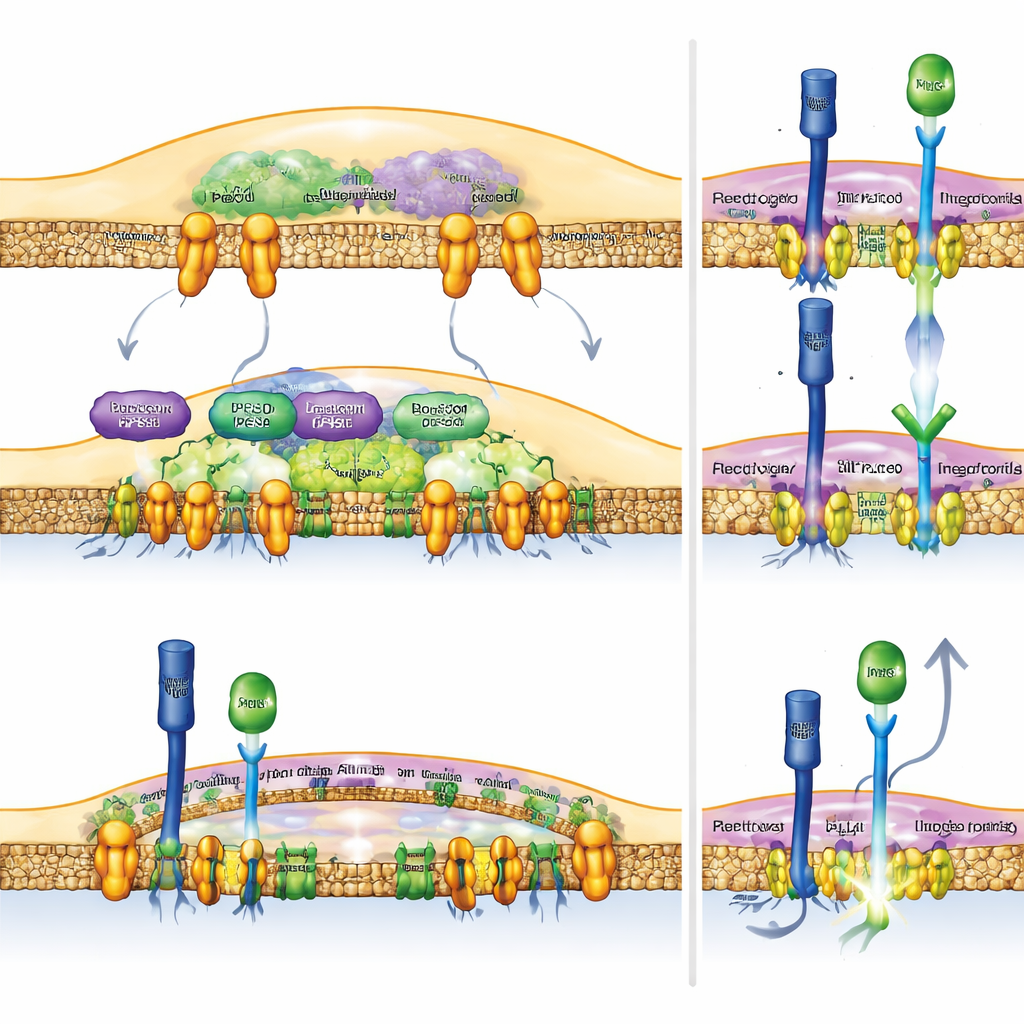
Notch come leva per l’immunità anticancro
Per verificare se l’aumento diretto di Notch nei macrofagi fosse sufficiente a favorire il sistema immunitario, il team ha ingegnerizzato topi i cui cellule mieloidi producono in modo continuo la parte attiva del recettore Notch. Questi topi hanno montato risposte antitumorali più potenti: i loro tumori erano più piccoli e le cellule T all’interno dei tumori avevano più degli strumenti molecolari necessari per distruggere le cellule cancerose. È importante sottolineare che quando i ricercatori hanno disattivato RBPJ—un partner chiave di cui Notch ha bisogno per attivare i suoi geni target—i benefici della perdita di Rubicon o dell’inibizione di PLD sono scomparsi. Questo dimostra che gli effetti antitumorali di queste interventi dipendono da una segnalazione Notch intatta nei macrofagi, piuttosto che da effetti collaterali non correlati.
Indizi dai tumori umani e direzioni future
Analizzando dati provenienti da migliaia di tumori umani, gli autori hanno trovato che i pazienti i cui tumori esprimevano alti livelli di ligandi che attivano Notch ma bassi livelli di Rubicon tendevano a sopravvivere più a lungo rispetto a quelli con alti livelli di Rubicon. Sebbene questa analisi non possa provare causa ed effetto, si allinea all’idea che bloccare la barriera che esclude Notch nel microambiente tumorale possa spostare l’equilibrio verso una sorveglianza immunitaria più efficace. Il lavoro suggerisce che farmaci che prendono di mira le vie di efferocitosi dipendenti da Rubicon o la PLD potrebbero un giorno essere combinati con immunoterapie esistenti per aiutare i macrofagi a trasformarsi da silenziosi spazzini in alleati attivi contro il cancro.
Cosa significa questo per i pazienti
In parole semplici, lo studio rivela che i macrofagi portano un cancello integrato che normalmente tiene lontano da siti in cui degradano cellule morte un segnale pro‑immunitario chiave, Notch. Questo protegge i tessuti sani da infiammazioni inutili ma può involontariamente proteggere i tumori. Disgregando il cancello—attraverso modifiche genetiche o trattamenti farmacologici—i ricercatori sono riusciti a far passare i segnali Notch, riprogrammando i macrofagi per richiamare le cellule T e altri difensori contro il cancro. Sebbene rimanga molto lavoro prima che queste intuizioni si traducano in terapie, indicano una nuova strategia: invece di limitarsi a stimolare più energicamente le cellule T, potremmo anche riprogettare le squadre di pulizia affinché smettano di attenuare e comincino ad amplificare l’allarme anticancro del corpo.
Citazione: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Parole chiave: efferocitosi, segnalazione Notch, macrofagi, microambiente tumorale, immunoterapia del cancro