Clear Sky Science · sv
Uteslutning av Notch från kontaktytan under efferocytos begränsar anticancer-immunitet
När städpatruller tystar cancerbekämpare
Våra kroppar rensar ständigt bort döende celler för att hålla vävnader friska och lugna. Men inne i tumörer kan denna samma rensningsprocess slå tillbaka genom att dämpa immunsystemet just när vi behöver det som mest: i kampen mot cancer. Denna studie avslöjar en dold avstängningsmekanism i immunceller som avgör om cellrensningen ska vagga immunsvaret till sömns eller hjälpa till att väcka det så att det angriper tumörer.
Kroppens städare och deras tysta arbete
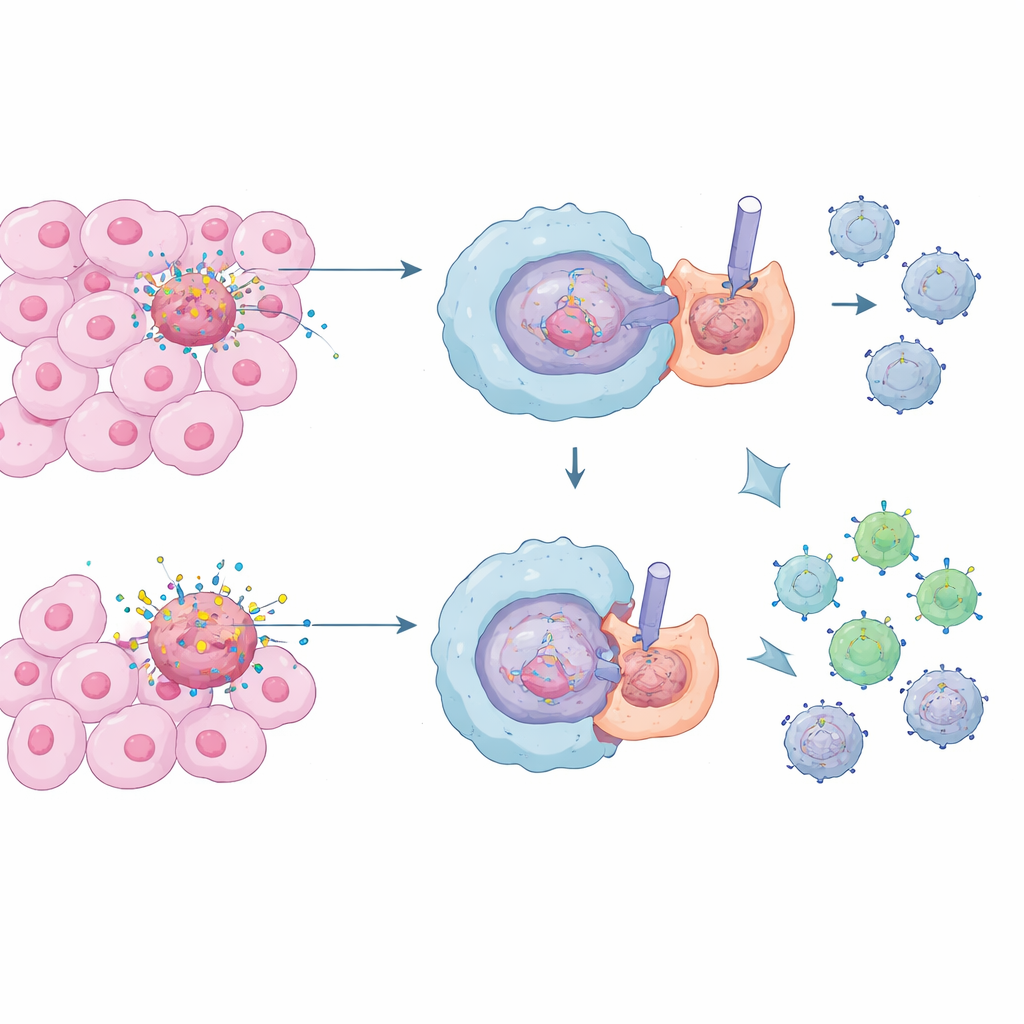
Särskilda immunceller kallade makrofager fungerar som kroppens städare, de slukar och bryter ner döda och döende celler i en process som kallas efferocytos. Under normala förhållanden är detta livsviktigt: det förhindrar utsläpp av toxiska cellinnehåll och håller inflammation i schack, vilket skyddar oss från kronisk vävnadsskada och autoimmuna sjukdomar. Inne i tumörer råder däremot en konstant storm av celldöd. Makrofager som tyst rensar upp dessa kadaver kan bidra till att skapa ett lugnt, dämpande grannskap runt cancern, vilket gör det svårare för mördarceller (T‑celler) att känna igen och förstöra maligna celler.
En dold signalport på makrofager
Forskarna fokuserade på ett kommunikationssystem kallat Notch, som hjälper celler att bestämma sitt beteende baserat på signaler från grannar. I makrofager tenderar Notch‑aktivitet att skjuta dem mot ett mer inflammatoriskt, tumörbekämpande tillstånd. Överraskande nog fann teamet att när friska makrofager omsluter döda celler så stänger de aktivt av Notch‑signaleringen just vid kontaktpunkten. De upptäckte att ett proteincomplex byggt kring ett molekylärt nav kallat Rubicon (RUBCN) samarbetar med ett annat enzym, VPS34, för att skapa en fysisk ”barriär” i makrofagens yttre membran. Denna barriär består av aktiverade integriner — greppande proteiner som omorganiseras till en tät ring — som bokstavligen skjuter de otympliga Notch‑receptorerna bort från det placket där den döda cellen träffar makrofagen, så att Notch inte kan slås på.
Bryta barriären för att förstärka immunangreppet
När forskarna tog bort Rubicon från makrofager eller blockerade ett downstream‑enzym kallat fosfolipas D (PLD), bildades inte längre denna integrinring på rätt sätt. Utan barriären kunde Notch‑receptorerna röra sig in i kontaktzonen och binda sina matchande ligander på den döda cellens yta. I möss visade tumörer som växte i djur utan Rubicon i myeloida celler — eller som behandlats med PLD‑blockerande läkemedel — starkare Notch‑aktivitet i makrofagerna, mer inflammatoriska genprogram och en våg av cancer‑dödande CD8‑T‑celler och naturliga mördarceller som trängde in i tumörerna. Följaktligen växte tumörerna långsammare.
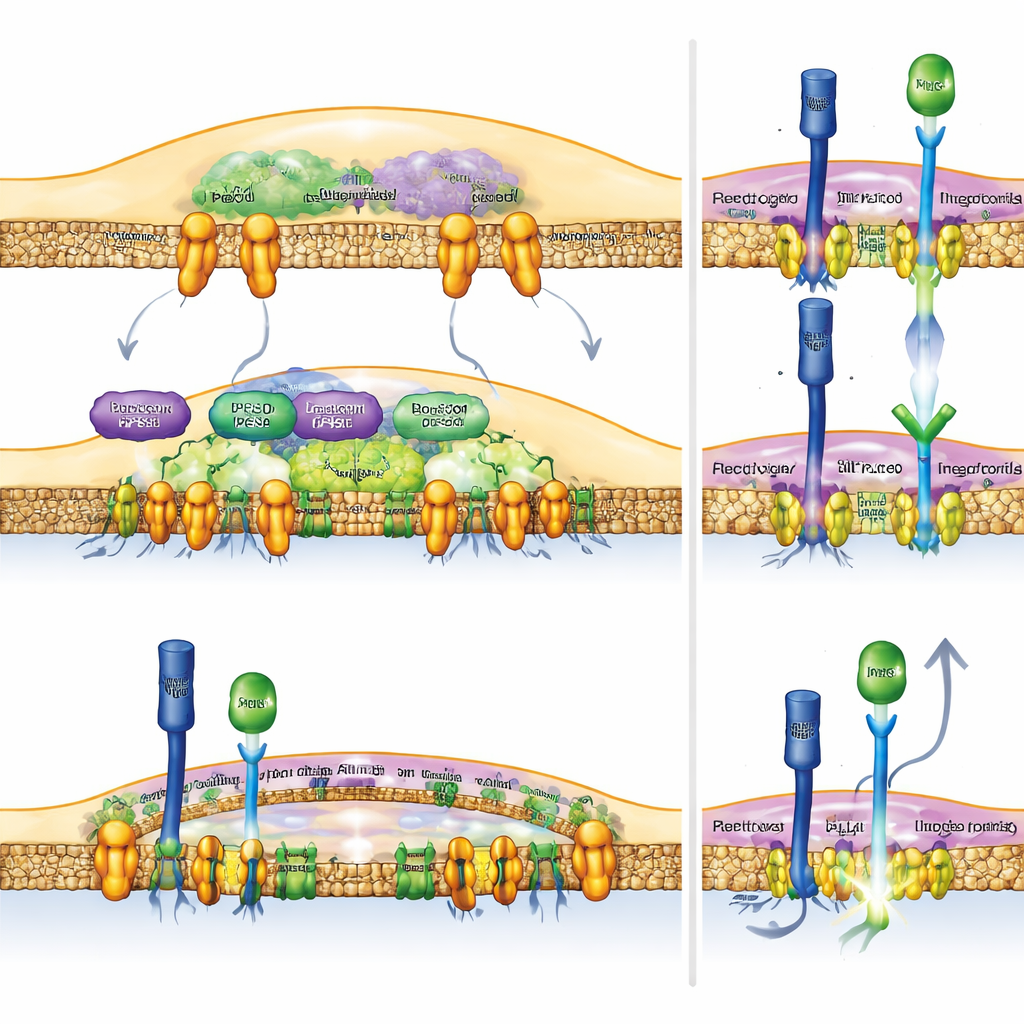
Notch som hävstång för cancerimmunitet
För att testa om en direkt uppreglering av Notch i makrofager räckte för att hjälpa immunsystemet, konstruerade teamet möss vars myeloida celler kontinuerligt producerar den aktiva delen av Notch‑receptorn. Dessa möss monterade kraftfullare antitumörsvar: deras tumörer var mindre, och T‑cellerna inne i tumörerna bar mer av de molekylära vapen som krävs för att förstöra cancerceller. Viktigt är att när forskarna inaktiverade RBPJ — en nyckelpartner som Notch behöver för att slå på sina målgener — försvann fördelarna av Rubicon‑bortfallet eller PLD‑inhiberingen. Detta visar att de antitumöreffekter som observeras beror på intakt Notch‑signalering i makrofager snarare än på orelaterade sidoeffekter.
Ledtrådar från mänskliga tumörer och framtida inriktningar
När författarna tittade på data från tusentals mänskliga tumörer fann de att patienter vars cancer uttryckte höga nivåer av Notch‑aktiverande ligander men låga nivåer av Rubicon tenderade att överleva längre än de med höga Rubicon‑nivåer. Även om denna analys inte kan bevisa orsak och verkan, stämmer den överens med idén att blockering av den Notch‑uteslutande barriären i tumörmikromiljön kan förskjuta balansen mot effektivare immunövervakning. Arbetet tyder på att läkemedel som riktar in sig på Rubicon‑beroende efferocytosvägar eller PLD en dag skulle kunna kombineras med befintliga immunoterapier för att få makrofager att byta från tysta sophämtare till aktiva allierade mot cancer.
Vad detta betyder för patienter
Enkelt uttryckt visar studien att makrofager bär på en inbyggd grind som normalt håller en viktig pro‑immun signal, Notch, borta från de platser där de tuggar upp döda celler. Detta skyddar friska vävnader från onödig inflammation men kan oavsiktligt skydda tumörer. Genom att störa grinden — genom genetiska förändringar eller läkemedelsbehandling — kunde forskarna släppa igenom Notch‑signaler, omprogrammera makrofager och få dem att mobilisera T‑celler och andra försvarare mot cancer. Även om mycket arbete återstår innan dessa insikter kan omsättas i behandlingar, pekar de mot en ny strategi: istället för att enbart pressa T‑celler hårdare kan vi också omkoppla städpatrullerna så att de slutar dämpa och börjar förstärka kroppens egna anticancer‑larm.
Citering: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Nyckelord: efferocytos, Notch‑signalering, makrofager, tumörmikromiljö, cancerimmunoterapi