Clear Sky Science · pt
Exclusão do Notch do local de contato durante a efferocitose limita a imunidade anticâncer
Quando as Equipes de Limpeza Silenciam os Combatentes do Câncer
Nossos corpos constantemente removem células em morte para manter os tecidos saudáveis e tranquilos. Mas dentro dos tumores, esse mesmo processo de limpeza pode se voltar contra nós ao acalmar o sistema imunológico justamente quando mais precisamos dele: durante a luta contra o câncer. Este estudo revela um interruptor oculto dentro de células imunes que decide se a remoção de células fará a resposta imune adormecer ou a ajudará a despertar para atacar tumores.
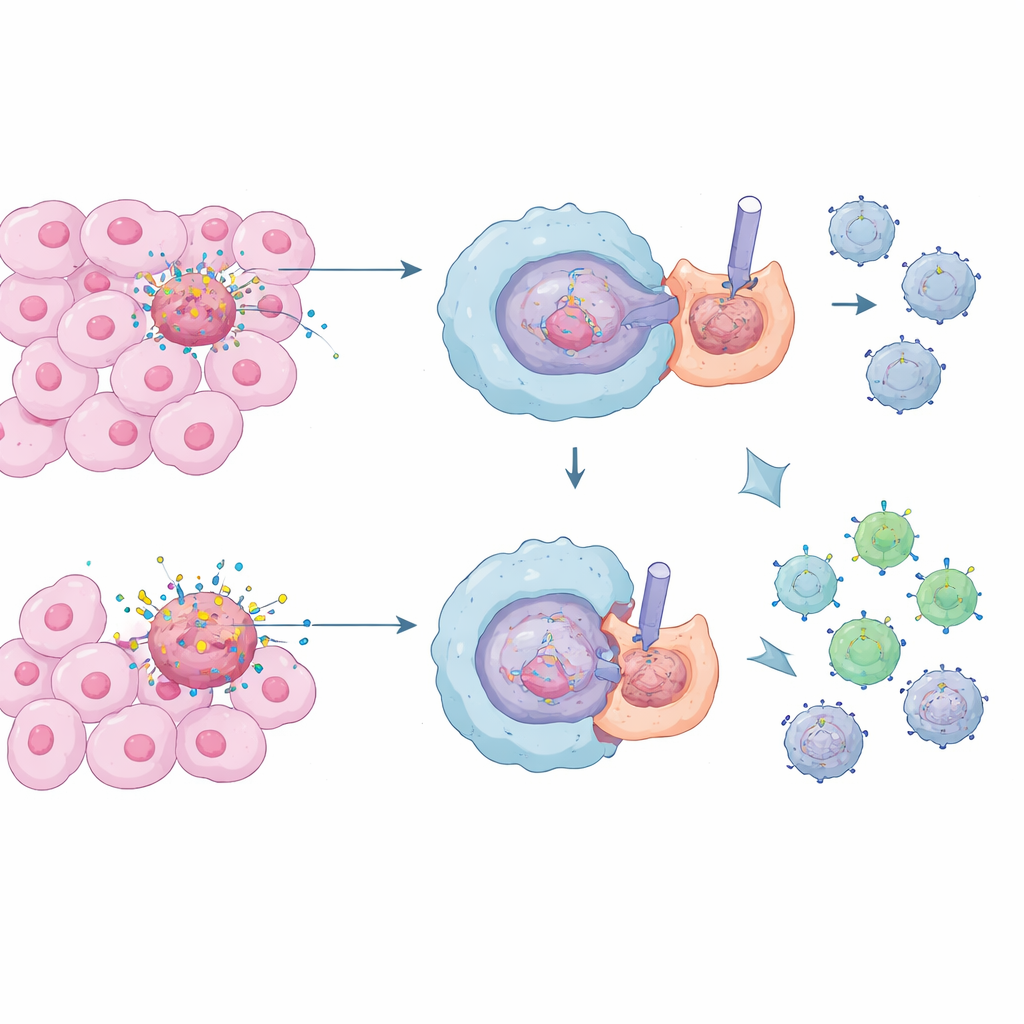
Os Faxineiros do Corpo e Seu Trabalho Silencioso
Células imunes especiais chamadas macrófagos atuam como faxineiros do corpo, engolindo e digerindo células mortas e moribundas em um processo conhecido como efferocitose. Em condições normais isso é vital: evita o vazamento de conteúdos celulares tóxicos e mantém a inflamação sob controle, protegendo-nos de danos crônicos ao tecido e de doenças autoimunes. No interior dos tumores, porém, há uma tempestade constante de morte celular. Macrófagos que silenciosamente limpam esses cadáveres podem acabar criando um ambiente calmo e supressivo ao redor do câncer, tornando mais difícil para células T assassinas reconhecerem e destruírem células malignas.
Um Portão de Sinalização Oculto nos Macrófagos
Os pesquisadores focaram em um sistema de comunicação chamado Notch, que ajuda as células a decidir como se comportar com base em sinais de suas vizinhas. Nos macrófagos, a atividade de Notch tende a direcioná‑los a um estado mais inflamatório e combativo contra tumores. Surpreendentemente, a equipe descobriu que, quando macrófagos saudáveis engolem células mortas, eles desligam ativamente a sinalização Notch exatamente no ponto de contato. Eles encontraram que um complexo proteico centrado em uma molécula chamada Rubicon (RUBCN) se associa a outra enzima, VPS34, para montar uma “barreira” física na membrana externa do macrófago. Essa barreira é formada por integrinas ativadas—proteínas de aderência que se reorganizam em um anel apertado—literalmente empurrando os volumosos receptores Notch para longe da região onde a célula morta toca o macrófago, impedindo que o Notch seja ativado.
Quebrando a Barreira para Potencializar o Ataque Imune
Quando os cientistas removeram Rubicon dos macrófagos, ou bloquearam uma enzima a jusante chamada fosfolipase D (PLD), esse anel de integrinas deixou de se formar corretamente. Sem a barreira, os receptores Notch puderam mover‑se para a zona de contato e engajar seus ligantes correspondentes na superfície da célula morta. Em camundongos, tumores que cresceram em animais sem Rubicon nas células mieloides—ou tratados com drogas que bloqueiam PLD—mostraram maior atividade de Notch dentro dos macrófagos, programas gênicos mais inflamatórios e uma onda de células CD8 T citotóxicas e células natural killer infiltrando os tumores. Como resultado, os tumores cresceram mais lentamente.
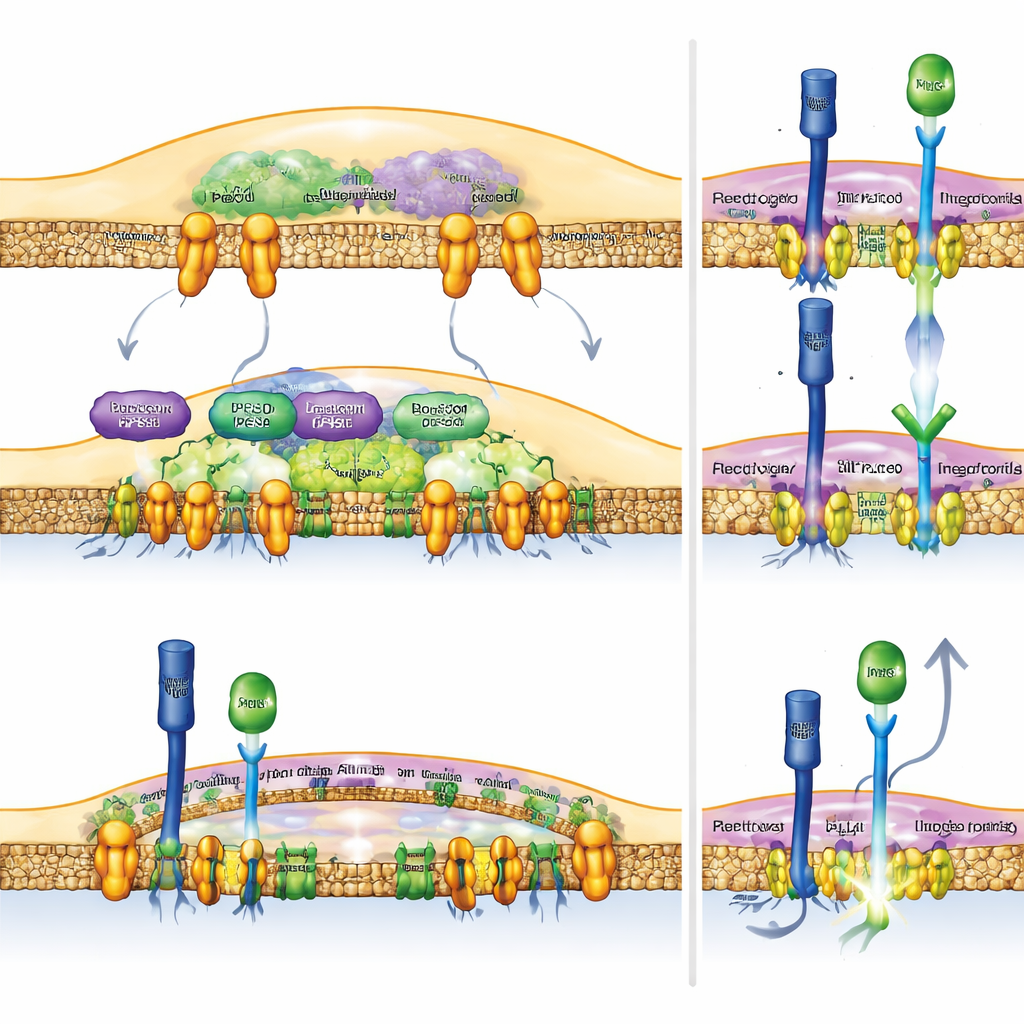
Notch como Alavanca para a Imunidade contra o Câncer
Para testar se aumentar diretamente o Notch nos macrófagos é suficiente para ajudar o sistema imune, a equipe engenheirou camundongos cujas células mieloides produzem continuamente a parte ativa do receptor Notch. Esses camundongos montaram respostas antitumorais mais potentes: seus tumores eram menores, e as células T dentro dos tumores exibiam mais das armas moleculares necessárias para destruir células cancerosas. Importante: quando os pesquisadores desativaram RBPJ—um parceiro-chave que o Notch precisa para ativar seus genes-alvo—os benefícios da perda de Rubicon ou da inibição de PLD desapareceram. Isso mostra que os efeitos antitumorais dessas intervenções dependem da sinalização Notch intacta nos macrófagos, em vez de efeitos colaterais não relacionados.
Pistas de Tumores Humanos e Direções Futuras
Ao analisar dados de milhares de tumores humanos, os autores descobriram que pacientes cujos cânceres expressavam altos níveis de ligantes ativadores de Notch, mas baixos níveis de Rubicon, tendiam a sobreviver mais tempo do que aqueles com níveis altos de Rubicon. Embora essa análise não prove causa e efeito, ela se alinha à ideia de que bloquear a barreira que exclui Notch no microambiente tumoral pode inclinar a balança em favor de uma vigilância imune mais eficaz. O trabalho sugere que drogas direcionadas às vias de efferocitose dependentes de Rubicon ou à PLD possam, um dia, ser combinadas com imunoterapias existentes para ajudar os macrófagos a mudar de coletores silenciosos de lixo para aliados ativos contra o câncer.
O Que Isso Significa para Pacientes
Em termos simples, o estudo revela que os macrófagos carregam um portão embutido que normalmente mantém um sinal pró-imune chave, o Notch, afastado dos locais onde eles degradam células mortas. Isso protege tecidos saudáveis de inflamação desnecessária, mas pode involuntariamente proteger tumores. Ao desabilitar esse portão—por alterações genéticas ou tratamento farmacológico—os pesquisadores puderam permitir a passagem dos sinais Notch, reprogramando macrófagos para reunir células T e outros defensores contra o câncer. Embora ainda haja muito trabalho antes que essas descobertas se traduzam em terapias, elas apontam para uma nova estratégia: em vez de apenas estimular mais as células T, também podemos reconfigurar as equipes de limpeza para que parem de abafar e comecem a amplificar o alarme anticâncer do próprio corpo.
Citação: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Palavras-chave: efferocitose, sinalização Notch, macrófagos, microambiente tumoral, imunoterapia contra o câncer