Clear Sky Science · ar
استبعاد نوتش من موقع التماس أثناء الالتقام الخلوي يقيّد المناعة المضادة للسرطان
عندما تُسكت فرق التنظيف مقاتلي السرطان
جسمنا يزيل باستمرار الخلايا المحتضرة للحفاظ على الأنسجة صحية وهادئة. لكن داخل الأورام، يمكن أن تنقلب هذه العملية نفسها ضدنا من خلال تهدئة جهاز المناعة في اللحظة التي نحتاجه فيها أكثر: أثناء القتال ضد السرطان. تكشف هذه الدراسة عن مفتاح مخفي داخل الخلايا المناعية يقرّر ما إذا كان تنظيف الخلايا سيهدي الاستجابة المناعية أم يساعد في إيقاظها للهجوم على الأورام.
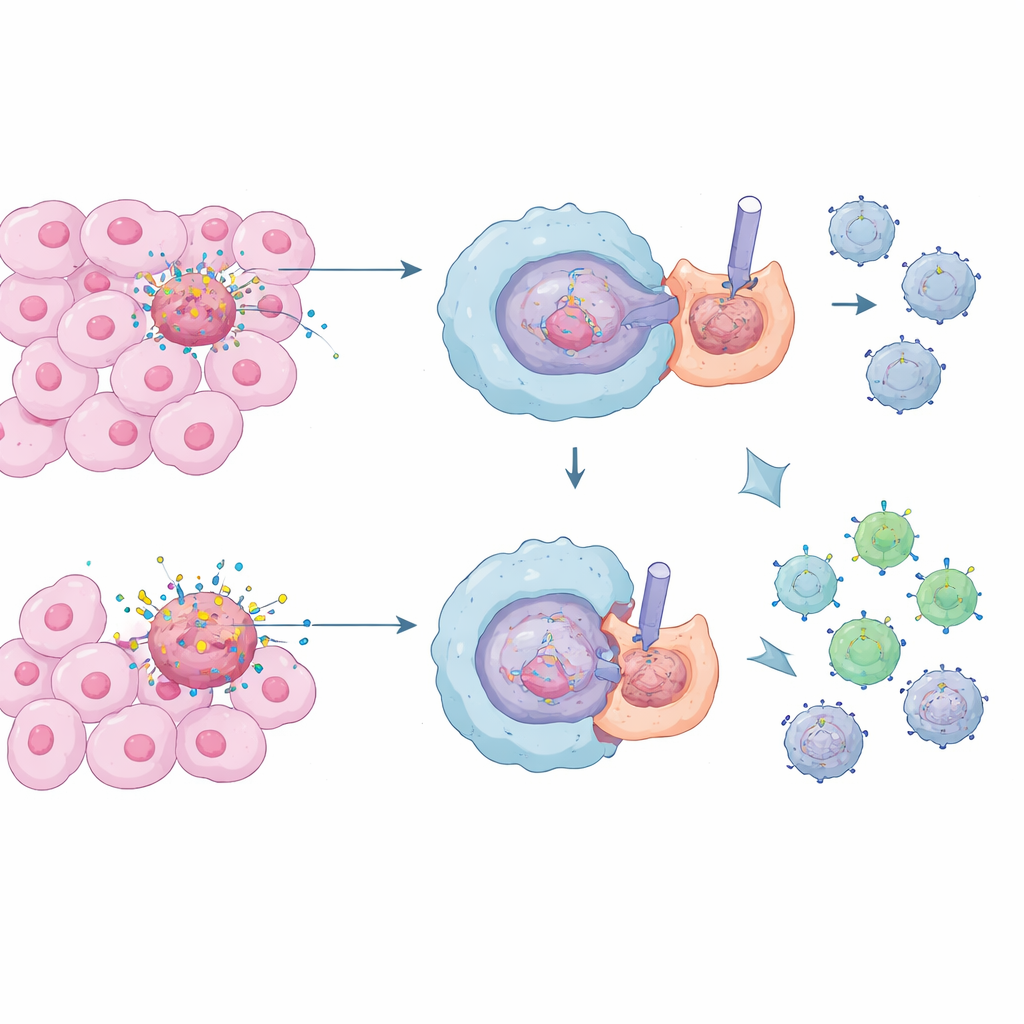
عمال النظافة في الجسم وعملهم الهادئ
تعمل خلايا مناعية متخصصة تسمى البلعميات كعمال نظافة في الجسم، حيث تبتلع وتهضم الخلايا الميتة والمحتضرة في عملية تُعرف بالالتقام الخلوي. تحت الظروف الطبيعية هذه العملية حيوية: فهي تمنع تسرب محتويات خلوية سامة وتبقي الالتهاب تحت السيطرة، مما يحمي من تلف أنسجي مزمن ومرض مناعي ذاتي. داخل الأورام، هناك، مع ذلك، عاصفة مستمرة من موت الخلايا. قد يؤدي اختفاء البلعميات التي تنظف هذه الجثث بهدوء إلى خلق حي هادئ وكابح حول السرطان، مما يصعّب على خلايا تي القاتلة التعرف على الخلايا الخبيثة وتدميرها.
بوابة إشارة مخفية على البلعميات
ركز الباحثون على نظام تواصل يُدعى نوتش، الذي يساعد الخلايا في تقرير سلوكها بناءً على إشارات الجيران. في البلعميات، تميل نشاطات نوتش إلى دفعها نحو حالة أكثر التهابية ومكافحة للأورام. على نحو مفاجئ، وجد الفريق أنه عندما تبتلع البلعميات السليمة الخلايا الميتة، فإنها تطفئ نشاط نوتش بنشاط عند نقطة الاتصال مباشرة. اكتشفوا أن مركبًا بروتينيًا مبنيًا حول جزيء يُدعى روبكون (RUBCN) يتعاون مع إنزيم آخر، VPS34، لتأسيس "حاجز" في غشاء البلعمة الخارجي. يتكون هذا الحاجز من إنتغرينات مُفعّلة—بروتينات تمسك وتُعاد ترتيبها إلى حلقة محكمة—تدفع حرفيًا مستقبلات نوتش الضخمة بعيدًا عن الرقعة التي يلمس فيها الخلية الميتة سطح البلعمة، بحيث لا يمكن تفعيل نوتش.
اختراق الحاجز لتعزيز الهجوم المناعي
عندما أزال العلماء روبكون من البلعميات، أو حجبوا إنزيمًا أسفلًا يُدعى فسفوليباز D (PLD)، لم تعد حلقة الإنتغرين تتكوّن بشكل صحيح. بدون الحاجز، أمكن لمستقبلات نوتش الانتقال إلى منطقة الاتصال والتفاعل مع مثائلها من اللُجَينات على سطح الخلية الميتة. في الفئران، أظهرت الأورام التي نمت في حيوانات فقدت روبكون في الخلايا النخاعية—أو التي عولجت بأدوية تحجب PLD—نشاط نوتش أقوى داخل البلعميات، وبرامج جينية التهابية أكثر، وتدفقًا لخلايا CD8 القاتلة للخلايا والطبيعية القاتلة التي اخترقت الأورام. ونتيجة لذلك، نمت الأورام بوتيرة أبطأ.
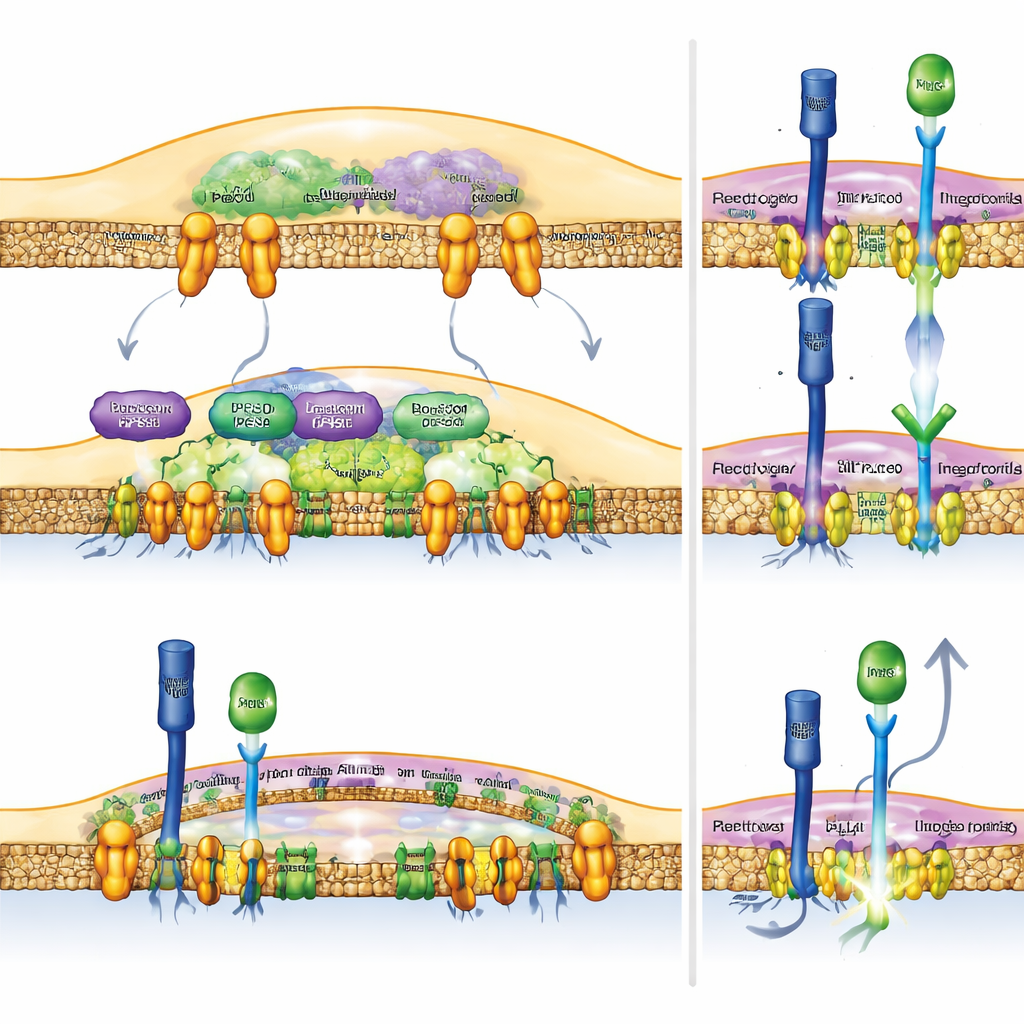
نوتش كرافعة للمناعة المضادة للسرطان
لاختبار ما إذا كان رفع نشاط نوتش مباشرة في البلعميات كافٍ لمساعدة جهاز المناعة، صمّم الفريق فئرانًا خلاياها النخاعية تنتج باستمرار الجزء النشط من مستقبل نوتش. أظهرت هذه الفئران استجابات مضادة للأورام أقوى: كانت أورامها أصغر، وحملت خلايا تي داخل الأورام أدوات جزيئية أكبر لتدمير الخلايا السرطانية. والمهم، أنه عندما أعاق الباحثون RBPJ—الشريك الأساسي الذي يحتاجه نوتش لتشغيل جيناته المستهدفة—اختفت فوائد فقدان روبكون أو تثبيط PLD. وهذا يدل على أن التأثيرات المضادة للأورام لهذه التدخّلات تعتمد على إشارة نوتش السليمة داخل البلعميات، لا على آثار جانبية غير ذات صلة.
دلائل من الأورام البشرية والاتجاهات المستقبلية
عند النظر إلى بيانات آلاف الأورام البشرية، وجد المؤلفون أن المرضى الذين عبرت سرطاناتهم عن مستويات عالية من لُجَينات تنشيط نوتش لكن مستويات منخفضة من روبكون كانوا يميلون إلى البقاء على قيد الحياة لفترة أطول من أولئك ذوي المستويات العالية من روبكون. بينما لا يمكن لهذا التحليل إثبات السببية، فإنه يتوافق مع الفكرة القائلة بأن حجب الحاجز المستبعد لنوتش في البيئة الدقيقة للورم يمكن أن يميل التوازن نحو مراقبة مناعية أكثر فعالية. تشير هذه الدراسة إلى أن أدوية تستهدف مسارات الالتقام الخلوي المعتمدة على روبكون أو PLD قد تُدمج يومًا ما مع العلاجات المناعية الموجودة لمساعدة البلعميات على التحول من جامعي نفايات هادئين إلى حلفاء نشطين ضد السرطان.
ما الذي يعنيه هذا للمرضى
ببساطة، تكشف الدراسة أن البلعميات تحمل بوابة مدمجة تحافظ عادةً على إبعاد إشارة مناعية رئيسية، نوتش، عن مواقع تمزيق الخلايا الميتة. هذا يحمي الأنسجة السليمة من الالتهاب غير الضروري لكنه قد يغطّي الأورام عن غير قصد. من خلال تعطيل البوابة—عن طريق تغييرات جينية أو علاج دوائي—مكن الباحثون مرور إشارات نوتش، فأعادوا برمجة البلعميات لحشد خلايا تي ومدافعين آخرين ضد السرطان. على الرغم من أن الكثير من العمل لا يزال مطلوبًا قبل أن تترجم هذه الأفكار إلى علاجات، إلا أنها تشير إلى استراتيجية جديدة: بدلاً من دفع خلايا تي فقط بقوة أكبر، قد نعيد أيضًا توصيل فرق التنظيف حتى تتوقف عن كتم الإنذار المناعي وتبدأ في تضخيمه.
الاستشهاد: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
الكلمات المفتاحية: الالتقام الخلوي, إشارة نوتش, البلعميات, البيئة الدقيقة للورم, العلاج المناعي للسرطان