Clear Sky Science · es
Exclusión de Notch del sitio de contacto durante la efervocitosis restringe la inmunidad anticancerígena
Cuando los equipos de limpieza silencian a los combatientes contra el cáncer
Nuestros cuerpos eliminan constantemente células moribundas para mantener los tejidos sanos y tranquilos. Pero dentro de los tumores, este mismo proceso de limpieza puede volverse contraproducente al calmar el sistema inmunitario justo cuando más lo necesitamos: durante la lucha contra el cáncer. Este estudio descubre un interruptor oculto dentro de las células inmunitarias que decide si la limpieza celular adormecerá la respuesta inmune o la despertará para atacar los tumores.
Los conserjes del cuerpo y su trabajo silencioso
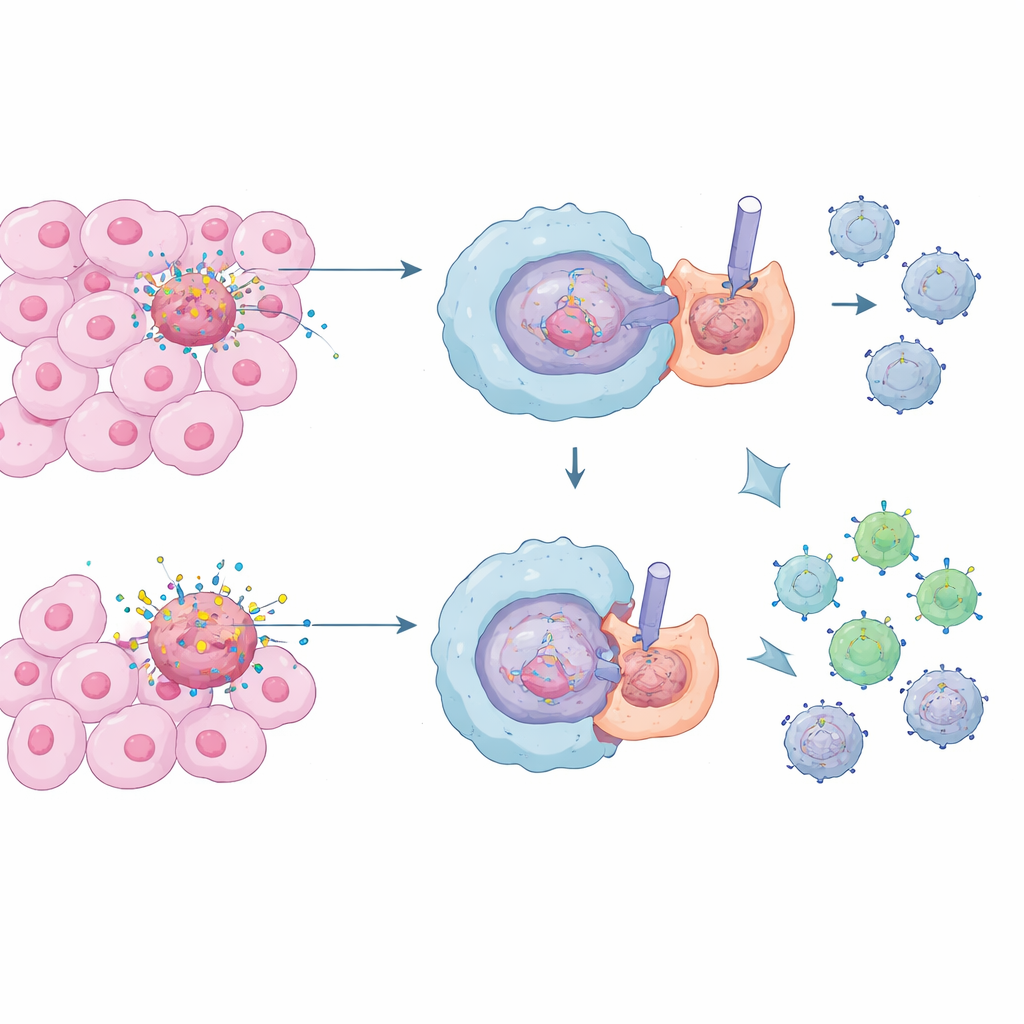
Células inmunitarias especializadas llamadas macrófagos actúan como los conserjes del cuerpo, engullendo y digiriendo células muertas y moribundas en un proceso conocido como eferocitosis. En condiciones normales esto es vital: evita la liberación de contenidos celulares tóxicos y mantiene la inflamación bajo control, protegiéndonos del daño tisular crónico y de las enfermedades autoinmunes. Sin embargo, dentro de los tumores hay una tormenta constante de muerte celular. Los macrófagos que eliminan silenciosamente estos restos pueden acabar creando un vecindario calmado y supresor alrededor del cáncer, lo que dificulta que las células T asesinas reconozcan y destruyan células malignas.
Una compuerta de señal oculta en los macrófagos
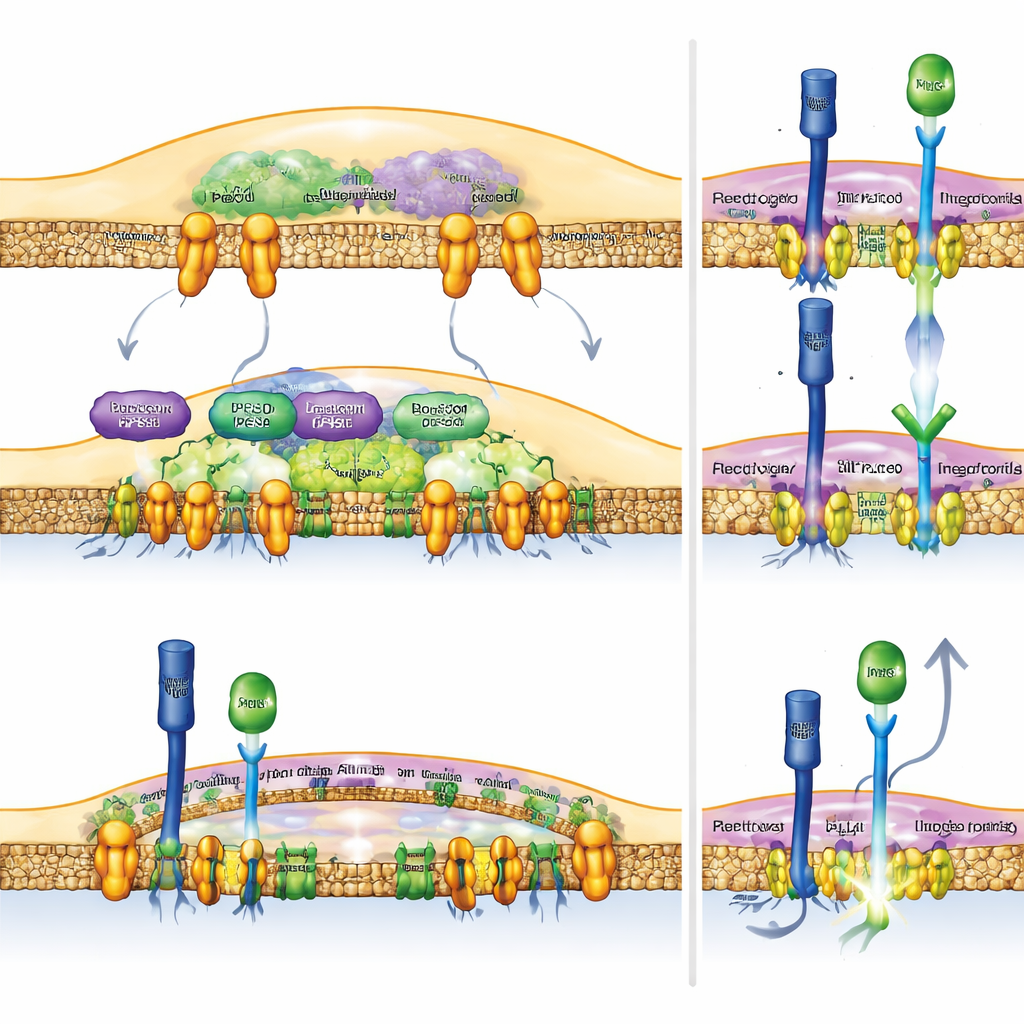
Los investigadores se centraron en un sistema de comunicación llamado Notch, que ayuda a las células a decidir cómo comportarse en función de las señales de sus vecinas. En los macrófagos, la actividad de Notch tiende a empujarlos hacia un estado más inflamatorio y combativo contra el tumor. Sorprendentemente, el equipo encontró que cuando los macrófagos sanos engullen células muertas, apagan activamente la señalización Notch justo en el punto de contacto. Descubrieron que un complejo proteico centrado en una molécula llamada Rubicon (RUBCN) se asocia con otra enzima, VPS34, para montar una “barrera” física en la membrana externa del macrófago. Esta barrera está formada por integrinas activadas—proteínas de agarre que se reorganizan en un anillo apretado—que literalmente empujan los voluminosos receptores Notch fuera del parche donde la célula muerta toca al macrófago, de modo que Notch no puede activarse.
Romper la barrera para potenciar el ataque inmune
Cuando los científicos eliminaron Rubicon de los macrófagos o bloquearon una enzima descendente llamada fosfolipasa D (PLD), este anillo de integrinas dejó de formarse correctamente. Sin la barrera, los receptores Notch pudieron desplazarse hacia la zona de contacto y ligarse con sus ligandos en la superficie de la célula muerta. En ratones, los tumores que crecieron en animales que carecían de Rubicon en células mieloides—o que fueron tratados con fármacos que bloquean PLD—mostraron mayor actividad de Notch dentro de los macrófagos, programas génicos más inflamatorios y una oleada de células CD8 T citotóxicas y células asesinas naturales infiltrando los tumores. Como resultado, los tumores crecieron más despacio.
Notch como palanca para la inmunidad contra el cáncer
Para probar si aumentar directamente Notch en los macrófagos es suficiente para ayudar al sistema inmunitario, el equipo diseñó ratones cuyas células mieloides producen de forma continua la parte activa del receptor Notch. Estos ratones montaron respuestas antitumorales más potentes: sus tumores fueron más pequeños y las células T dentro de los tumores portaban más de las armas moleculares necesarias para destruir las células cancerosas. Es importante que, cuando los investigadores inactivaron RBPJ—un socio clave que Notch necesita para activar sus genes diana—los beneficios de la pérdida de Rubicon o de la inhibición de PLD desaparecieron. Esto muestra que los efectos antitumorales de estas intervenciones dependen de una señalización Notch intacta en los macrófagos, y no de efectos secundarios no relacionados.
Pistas desde tumores humanos y direcciones futuras
Al analizar datos de miles de tumores humanos, los autores hallaron que los pacientes cuyos cánceres expresaban altos niveles de ligandos que activan Notch pero bajos niveles de Rubicon tendían a sobrevivir más que aquellos con niveles altos de Rubicon. Aunque este análisis no puede probar causalidad, concuerda con la idea de que bloquear la barrera que excluye a Notch en el microambiente tumoral puede inclinar la balanza hacia una vigilancia inmune más eficaz. El trabajo sugiere que fármacos dirigidos a las vías de eferocitosis dependientes de Rubicon o a PLD podrían algún día combinarse con inmunoterapias existentes para ayudar a que los macrófagos pasen de ser recolectores silenciosos de desechos a aliados activos contra el cáncer.
Qué significa esto para los pacientes
En pocas palabras, el estudio revela que los macrófagos llevan una compuerta incorporada que normalmente mantiene una señal proinmune clave, Notch, alejada de los sitios donde devoran células muertas. Esto protege los tejidos sanos de inflamación innecesaria pero puede, involuntariamente, proteger a los tumores. Al interrumpir la compuerta—mediante cambios genéticos o tratamiento farmacológico—los investigadores pudieron dejar pasar las señales Notch, reprogramando a los macrófagos para movilizar a las células T y a otros defensores contra el cáncer. Aunque queda mucho trabajo antes de que estos hallazgos se traduzcan en terapias, señalan una nueva estrategia: en lugar de limitarse a estimular más a las células T, también podríamos reconectar a los equipos de limpieza para que dejen de amortiguar y empiecen a amplificar la propia alarma anticancerígena del organismo.
Cita: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Palabras clave: eferocitosis, señalización Notch, macrófagos, microambiente tumoral, inmunoterapia contra el cáncer