Clear Sky Science · nl
Uitsluiting van Notch van de contactplaats tijdens efferocytose beperkt antikanker‑immuniteit
Wanneer opruimploegen kankervechters tot zwijgen brengen
Ons lichaam ruimt voortdurend stervende cellen op om weefsels gezond en kalm te houden. Maar in tumoren kan ditzelfde schoonmaakproces averechts werken door het immuunsysteem te sussen op het moment dat we het juist het meest nodig hebben: tijdens de strijd tegen kanker. Deze studie onthult een verborgen schakelaar in immuuncellen die bepaalt of het opruimen de immuunrespons in slaap sust of juist helpt wakker te maken om tumoren aan te vallen.
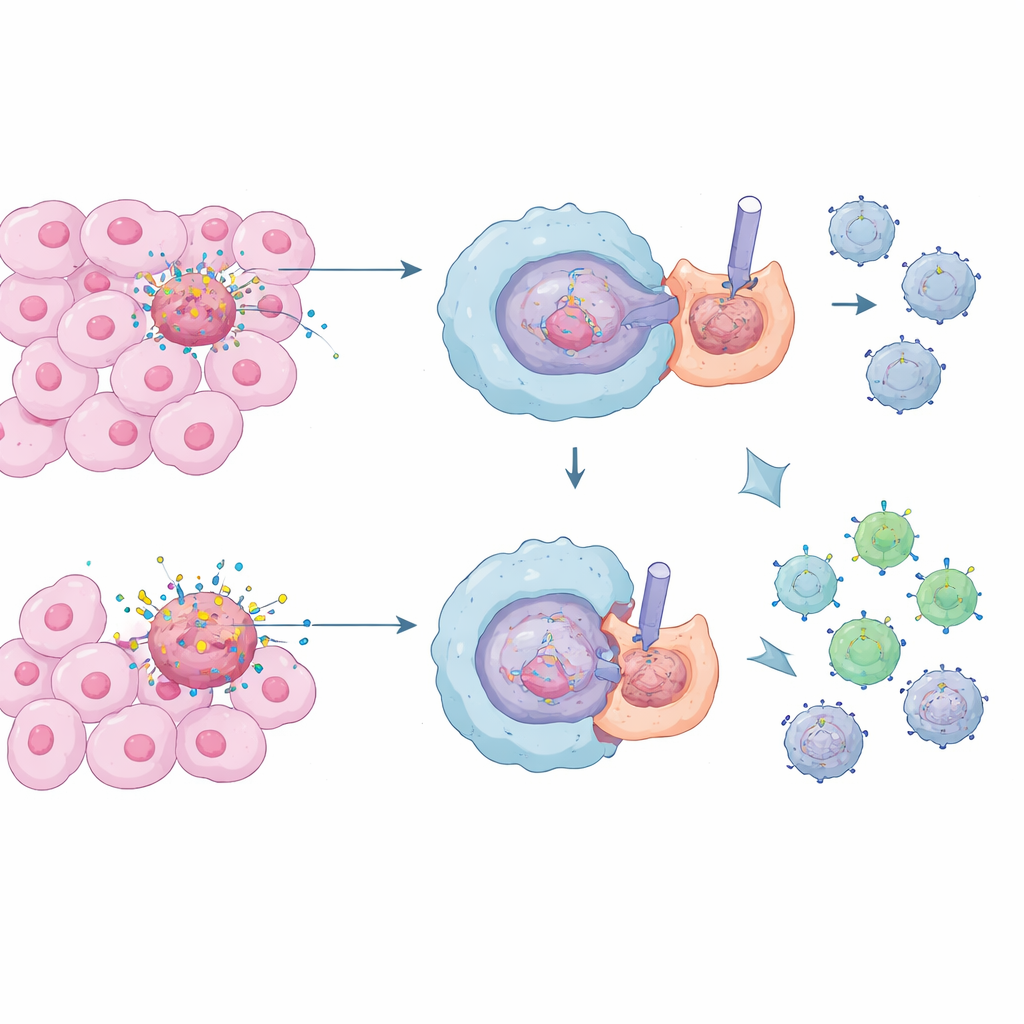
De schoonmakers van het lichaam en hun stille werk
Speciale immuuncellen, macrofagen, functioneren als de schoonmakers van het lichaam: ze verslinden en verteren dode en stervende cellen in een proces dat bekendstaat als efferocytose. Onder normale omstandigheden is dit essentieel: het voorkomt dat toxische celinhoud vrijkomt en houdt ontsteking onder controle, waardoor we beschermd blijven tegen chronische weefselschade en auto‑immuunziekten. In tumoren is er echter een constante storm van celdood. Macrofagen die deze lijken stilletjes opruimen, kunnen een kalme, onderdrukkende omgeving rond de kanker creëren, waardoor het moeilijker wordt voor cytotoxische T‑cellen om kwaadaardige cellen te herkennen en te vernietigen.
Een verborgen signaalpoort op macrofagen
De onderzoekers richtten zich op een communicatiesysteem genaamd Notch, dat cellen helpt te beslissen hoe ze zich moeten gedragen op basis van signalen van hun buren. In macrofagen neigt Notch‑activiteit ertoe ze naar een meer ontstekingsbevorderende, tumorbestrijdende staat te duwen. Tot hun verbazing vonden de onderzoekers dat wanneer gezonde macrofagen dode cellen insluiten, ze actief de Notch‑signalering uitschakelen precies op het contactpunt. Ze ontdekten dat een eiwitcomplex rond een molecuul genaamd Rubicon (RUBCN) samenwerkt met een ander enzym, VPS34, om een fysieke “barrière” in het buitenmembraan van de macrofaag op te zetten. Deze barrière bestaat uit geactiveerde integrines—grepen die zich herschikken tot een strakke ring—die de omvangrijke Notch‑receptoren letterlijk wegedrukt houden van het gebied waar de dode cel de macrofaag raakt, zodat Notch niet kan worden geactiveerd.
De barrière doorbreken om de immuungevecht te versterken
Toen de wetenschappers Rubicon uit macrofagen verwijderden, of een downstream enzym genaamd fosfolipase D (PLD) blokkeerden, vormde deze integrinering zich niet langer goed. Zonder de barrière konden Notch‑receptoren het contactgebied binnen bewegen en hun overeenkomstige liganden op het oppervlak van de dode cel binden. Bij muizen vertoonden tumoren die groeiden in dieren zonder Rubicon in myeloïde cellen—or die werden behandeld met PLD‑blokkers—sterkere Notch‑activiteit in macrofagen, meer ontstekingsgerichte genprogramma’s en een toestroom van kankerdodende CD8‑T‑cellen en natural killer‑cellen in de tumoren. Als gevolg daarvan groeiden tumoren langzamer.
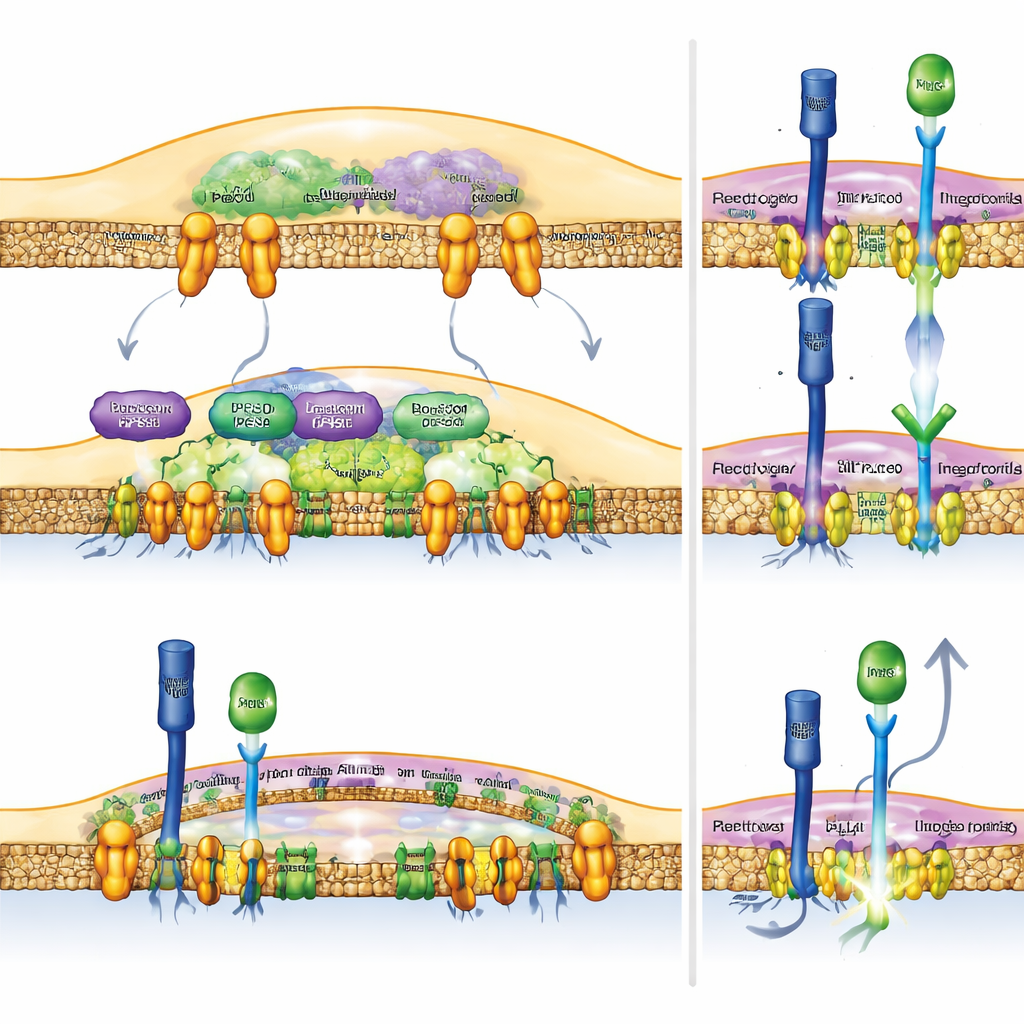
Notch als hefboom voor kankerimmuniteit
Om te testen of directe verhoging van Notch in macrofagen voldoende is om het immuunsysteem te helpen, maakten de onderzoekers muizen waarvan de myeloïde cellen continu het actieve deel van de Notch‑receptor produceren. Deze muizen ontwikkelden krachtigere antitumorresponsen: hun tumoren waren kleiner en T‑cellen in de tumoren droegen meer van de moleculaire wapens die nodig zijn om kankercellen te vernietigen. Belangrijk is dat toen de onderzoekers RBPJ—een sleutelpartner die Notch nodig heeft om zijn doelgenen aan te zetten—uitschakelden, de voordelen van Rubicon‑verlies of PLD‑remming verdwenen. Dit toont aan dat de antitumor‑effecten van deze ingrepen afhankelijk zijn van intacte Notch‑signalering in macrofagen, en niet van niet‑gerelateerde bijwerkingen.
Aanwijzingen uit menselijke tumoren en toekomstige richtingen
Bij analyse van gegevens uit duizenden menselijke tumoren vonden de auteurs dat patiënten wiens kankers hoge niveaus van Notch‑activerende liganden maar lage niveaus van Rubicon tot expressie brachten, geneigd waren langer te overleven dan degenen met hoge Rubicon‑niveaus. Hoewel deze analyse geen oorzaak‑gevolg kan aantonen, past het bij het idee dat het blokkeren van de Notch‑uitsluitende barrière in de tumormicro‑omgeving het evenwicht kan verschuiven naar effectievere immuurbewaking. Het werk suggereert dat geneesmiddelen die Rubicon‑afhankelijke efferocytosepaden of PLD targeten, mogelijk op termijn gecombineerd kunnen worden met bestaande immunotherapieën om macrofagen te laten omschakelen van stille opruimers naar actieve bondgenoten tegen kanker.
Wat dit betekent voor patiënten
Kort gezegd onthult de studie dat macrofagen een ingebouwde poort dragen die normaal een sleutelpro‑immuunsignaal, Notch, uit de weg houdt op plaatsen waar ze dode cellen verteren. Dit beschermt gezonde weefsels tegen onnodige ontsteking maar kan onbedoeld tumoren afschermen. Door de poort te verstoren—door genetische veranderingen of medicamenteuze behandeling—konen de onderzoekers Notch‑signalen doorlaten en macrofagen herprogrammeren om T‑cellen en andere verdedigers tegen kanker bijeen te brengen. Hoewel er nog veel werk nodig is voordat deze inzichten in therapieën worden omgezet, wijzen ze op een nieuwe strategie: in plaats van alleen T‑cellen harder aan te jagen, zouden we ook de opruimploegen kunnen herbedraden zodat ze ophouden te dempen en beginnen te versterken wat het lichaam al als antikankeralarm heeft.
Bronvermelding: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Trefwoorden: efferocytose, Notch‑signalering, macrofagen, tumormicro‑omgeving, kankerimmunotherapie