Clear Sky Science · fr
Exclusion de Notch du site de contact pendant l'efférocytose limite l'immunité anticancéreuse
Quand les équipes de nettoyage font taire les combattants du cancer
Notre organisme élimine en permanence les cellules en train de mourir pour maintenir les tissus sains et calmes. Mais dans les tumeurs, ce même processus de nettoyage peut se retourner contre nous en apaisant le système immunitaire au moment où nous en avons le plus besoin : lors d'une lutte contre le cancer. Cette étude met au jour un interrupteur caché au sein des cellules immunitaires qui décide si le nettoyage endormira la réponse immunitaire ou l'aidera à se réveiller pour attaquer les tumeurs.
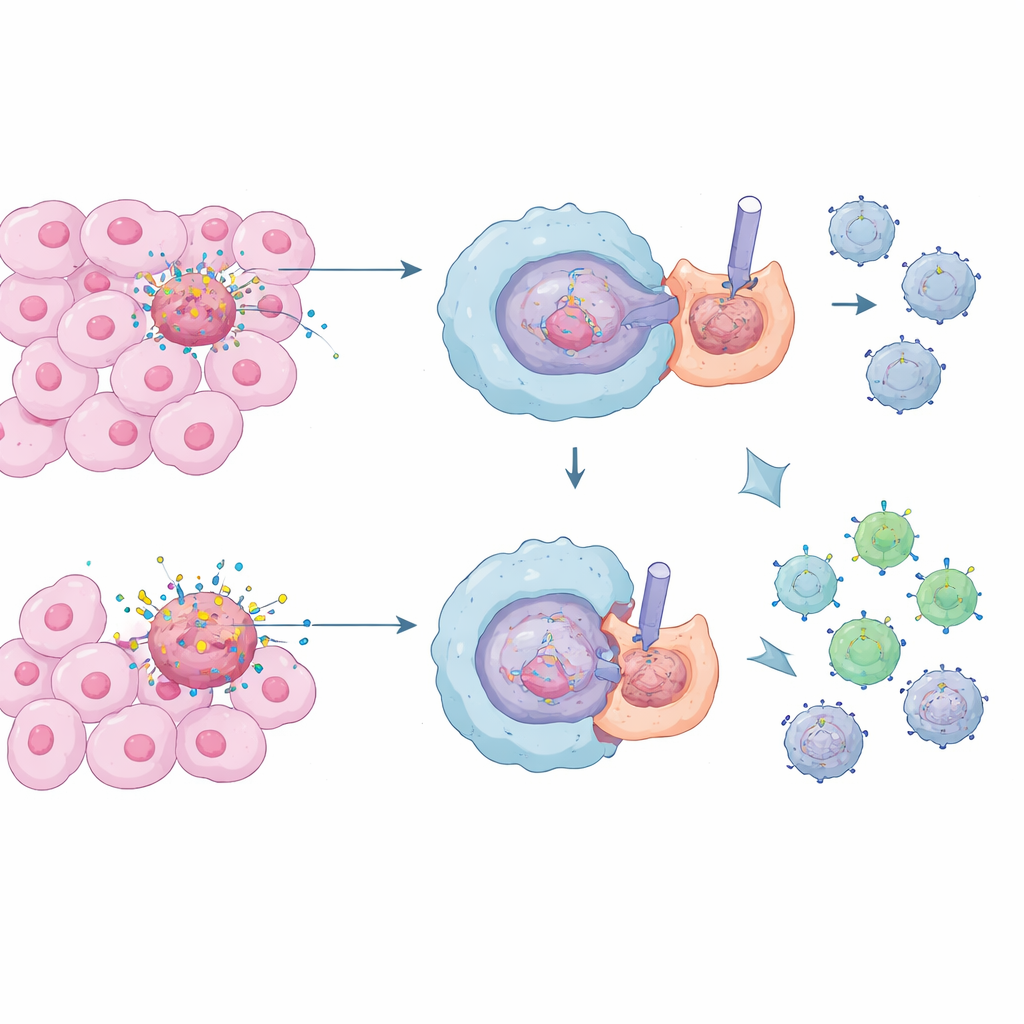
Les nettoyeurs du corps et leur travail silencieux
Des cellules immunitaires spécialisées appelées macrophages jouent le rôle de nettoyeurs du corps, en avalant et digérant les cellules mortes et mourantes dans un processus connu sous le nom d'efférocytose. Dans des conditions normales, c'est vital : cela empêche la dispersion de contenus cellulaires toxiques et maintient l'inflammation sous contrôle, nous protégeant des dommages tissulaires chroniques et des maladies auto-immunes. À l'intérieur des tumeurs, toutefois, il y a une tempête constante de mort cellulaire. Les macrophages qui débarrassent silencieusement ces cadavres peuvent finir par créer autour du cancer un voisinage calme et suppressif, rendant plus difficile pour les lymphocytes T tueurs de reconnaître et détruire les cellules malignes.
Une barrière de signalisation cachée sur les macrophages
Les chercheurs se sont concentrés sur un système de communication nommé Notch, qui aide les cellules à décider comment se comporter en fonction des signaux de leurs voisines. Chez les macrophages, l'activité de Notch tend à les pousser vers un état plus inflammatoire et anti‑tumoral. De façon surprenante, l'équipe a découvert que lorsque des macrophages sains engloutissent des cellules mortes, ils coupent activement la signalisation Notch précisément au point de contact. Ils ont montré qu'un complexe protéique centré sur une molécule appelée Rubicon (RUBCN) s'associe à une autre enzyme, VPS34, pour établir une « barrière » physique dans la membrane externe du macrophage. Cette barrière est constituée d'intégrines activées — protéines d'adhérence qui se réarrangent en un anneau serré — repoussant littéralement les volumineux récepteurs Notch loin de la zone où la cellule morte touche le macrophage, empêchant ainsi l'activation de Notch.
Briser la barrière pour renforcer l'attaque immunitaire
Lorsque les scientifiques ont supprimé Rubicon dans les macrophages, ou bloqué une enzyme en aval appelée phospholipase D (PLD), cet anneau d'intégrines ne s'est plus formé correctement. Sans la barrière, les récepteurs Notch pouvaient se déplacer dans la zone de contact et engager leurs ligands correspondants à la surface de la cellule morte. Chez la souris, les tumeurs développées chez des animaux dépourvus de Rubicon dans les cellules myéloïdes — ou traités par des médicaments inhibant la PLD — présentaient une activité Notch renforcée dans les macrophages, des programmes géniques plus inflammatoires et une infiltration accrue de cellules CD8 tueuses et de cellules NK dans les tumeurs. Par conséquent, la croissance tumorale était ralentie.
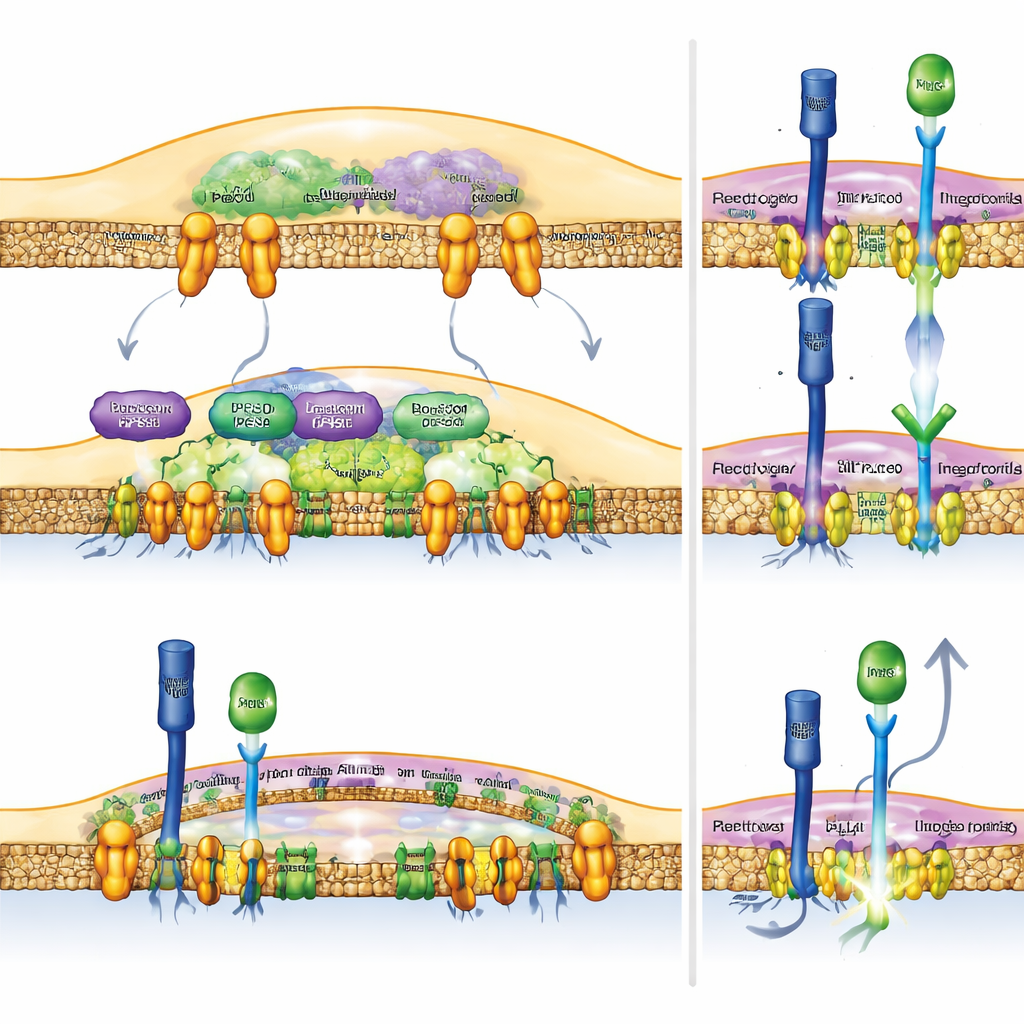
Notch comme levier de l'immunité anticancéreuse
Pour vérifier si l'activation directe de Notch dans les macrophages suffisait à aider le système immunitaire, l'équipe a conçu des souris dont les cellules myéloïdes produisent en continu la partie active du récepteur Notch. Ces animaux ont déclenché des réponses antitumorales plus puissantes : leurs tumeurs étaient plus petites et les lymphocytes T à l'intérieur des tumeurs portaient davantage d'armes moléculaires nécessaires pour détruire les cellules cancéreuses. De manière importante, lorsque les chercheurs ont désactivé RBPJ — un partenaire clé dont Notch a besoin pour activer ses gènes cibles — les bénéfices de la perte de Rubicon ou de l'inhibition de la PLD ont disparu. Cela montre que les effets antitumoraux de ces interventions dépendent d'une signalisation Notch intacte dans les macrophages, et non d'effets secondaires non liés.
Indices provenant de tumeurs humaines et pistes d'avenir
En analysant des données de milliers de tumeurs humaines, les auteurs ont constaté que les patients dont les cancers exprimaient des niveaux élevés de ligands activant Notch mais de faibles niveaux de Rubicon avaient tendance à survivre plus longtemps que ceux présentant des niveaux élevés de Rubicon. Bien que cette analyse ne puisse pas établir de relation de cause à effet, elle concorde avec l'idée que bloquer la barrière d'exclusion de Notch dans le microenvironnement tumoral peut basculer l'équilibre en faveur d'une surveillance immunitaire plus efficace. Ces travaux suggèrent que des médicaments ciblant les voies d'efférocytose dépendantes de Rubicon ou la PLD pourraient un jour être combinés aux immunothérapies existantes pour aider les macrophages à passer du statut de simples éboueurs silencieux à celui d'alliés actifs contre le cancer.
Ce que cela signifie pour les patients
En termes simples, l'étude révèle que les macrophages possèdent une porte intérieure qui garde normalement un signal pro‑immunitaire clé, Notch, éloigné des sites où ils dégradent les cellules mortes. Cela protège les tissus sains d'une inflammation inutile mais peut involontairement abriter les tumeurs. En perturbant cette porte — par des modifications génétiques ou un traitement médicamenteux — les chercheurs ont pu laisser passer les signaux Notch, reprogrammant les macrophages pour mobiliser les lymphocytes T et d'autres défenseurs contre le cancer. Bien qu'il reste beaucoup de travail avant que ces découvertes ne se traduisent en traitements, elles ouvrent une nouvelle stratégie : plutôt que de stimuler uniquement les lymphocytes T, on pourrait aussi reconfigurer les équipes de nettoyage pour qu'elles cessent d'étouffer et commencent à amplifier l'alarme anticancéreuse de l'organisme.
Citation: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Mots-clés: efférocytose, signalisation Notch, macrophages, microenvironnement tumoral, immunothérapie anticancéreuse