Clear Sky Science · tr
Efferositoz sırasında temas bölgesinden Notch’un dışlanması, antikanser bağışıklığını kısıtlar
Temizlik Ekibi Kanser Dövüşçülerini Susturduğunda
Vücudumuz dokuları sağlıklı ve sakin tutmak için sürekli olarak ölen hücreleri temizliyor. Ancak tümörlerde bu aynı temizlik süreci, kanserle savaşmak istediğimiz anda bağışıklık sistemini yatıştırarak ters tepki verebilir. Bu çalışma, hücre temizliğinin bağışıklık yanıtını uykuya mı yatıracağı yoksa tümörlere saldırmak için uyandırıp uyandıramayacağına karar veren bağışıklık hücreleri içindeki gizli bir anahtarı ortaya koyuyor.
Vücudun Hizmetçileri ve Onların Sessiz Çalışması
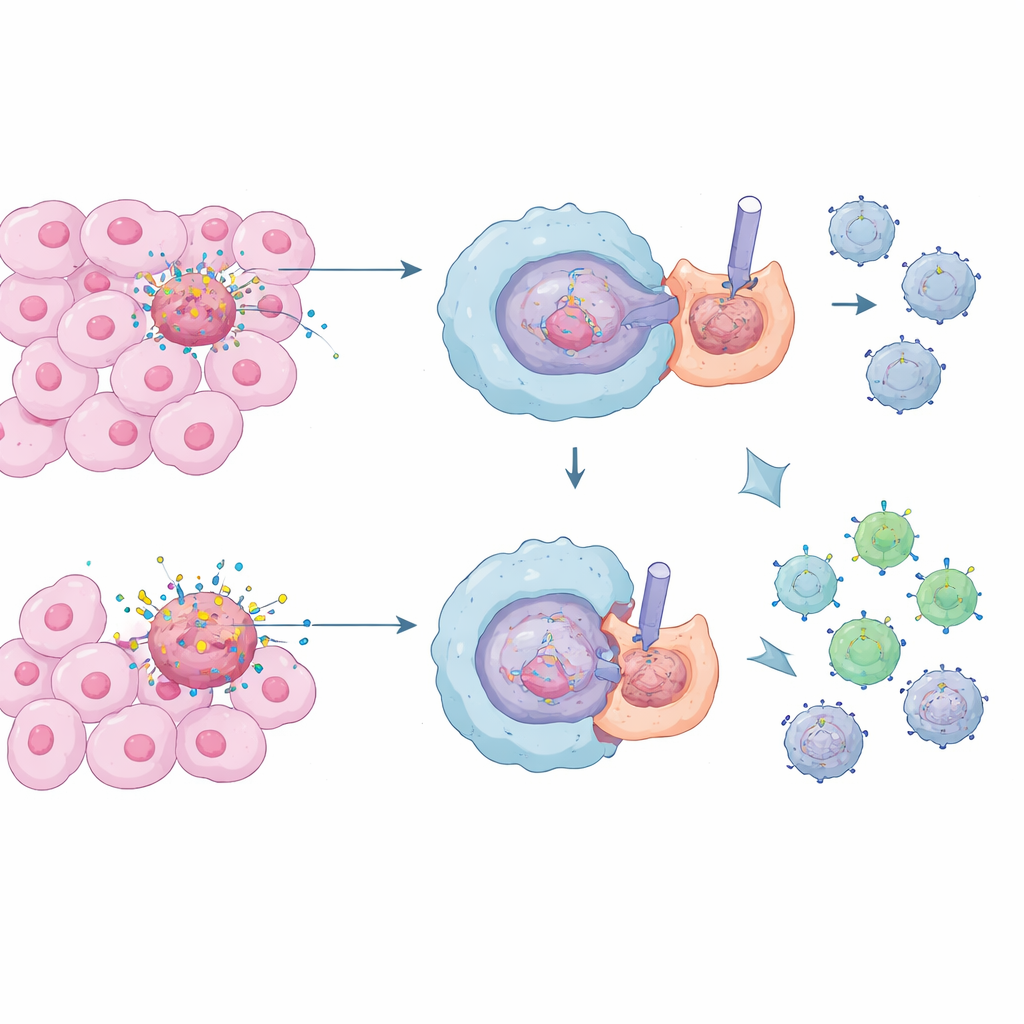
Makrofaj adı verilen özel bağışıklık hücreleri, efferositoz olarak bilinen bir süreçte ölü ve ölmekte olan hücreleri yutarak ve sindirerek vücudun hizmetçileri gibi davranır. Normal koşullarda bu çok önemlidir: toksik hücre içeriklerinin sızmasını önler ve iltihabı kontrol altında tutarak kronik doku hasarı ve otoimmün hastalıklardan korur. Ancak tümörlerin içinde sürekli bir hücre ölümü fırtınası vardır. Bu cesetleri sessizce temizleyen makrofajlar, kanserin etrafında sakin ve baskılayıcı bir ortam yaratarak öldürücü T hücrelerinin kötü huylu hücreleri tanıyıp yok etmesini zorlaştırabilir.
Makrofajlarda Gizli Bir Sinyal Kapısı
Araştırmacılar, hücrelerin komşularından gelen sinyallere göre davranışlarını belirlemesine yardımcı olan Notch adlı bir iletişim sistemine odaklandı. Makrofajlarda Notch etkinliği genellikle onları daha iltihaplı, tümörle savaşan bir duruma iter. İlginç bir şekilde ekip, sağlıklı makrofajlar ölü hücreleri yuttuklarında, temas noktasında Notch sinyalleşmesini aktif olarak kapattıklarını buldu. RUBCN adlı bir molekül etrafında kurulan bir protein kompleksinin, VPS34 adlı başka bir enzimle iş birliği yaparak makrofajın dış zarında fiziksel bir “engel” oluşturduğunu keşfettiler. Bu engel, sıkı bir halka şeklinde yeniden düzenlenen aktifleşmiş integrinlerden—tutunma proteinlerinden—oluşuyor ve ölü hücrenin makrofaja temas ettiği yamadaki büyük Notch reseptörlerini kelimenin tam anlamıyla uzaklaştırarak Notch’un etkinleştirilememesini sağlıyor.
Engeli Kırarak Bağışıklık Saldırısını Güçlendirmek
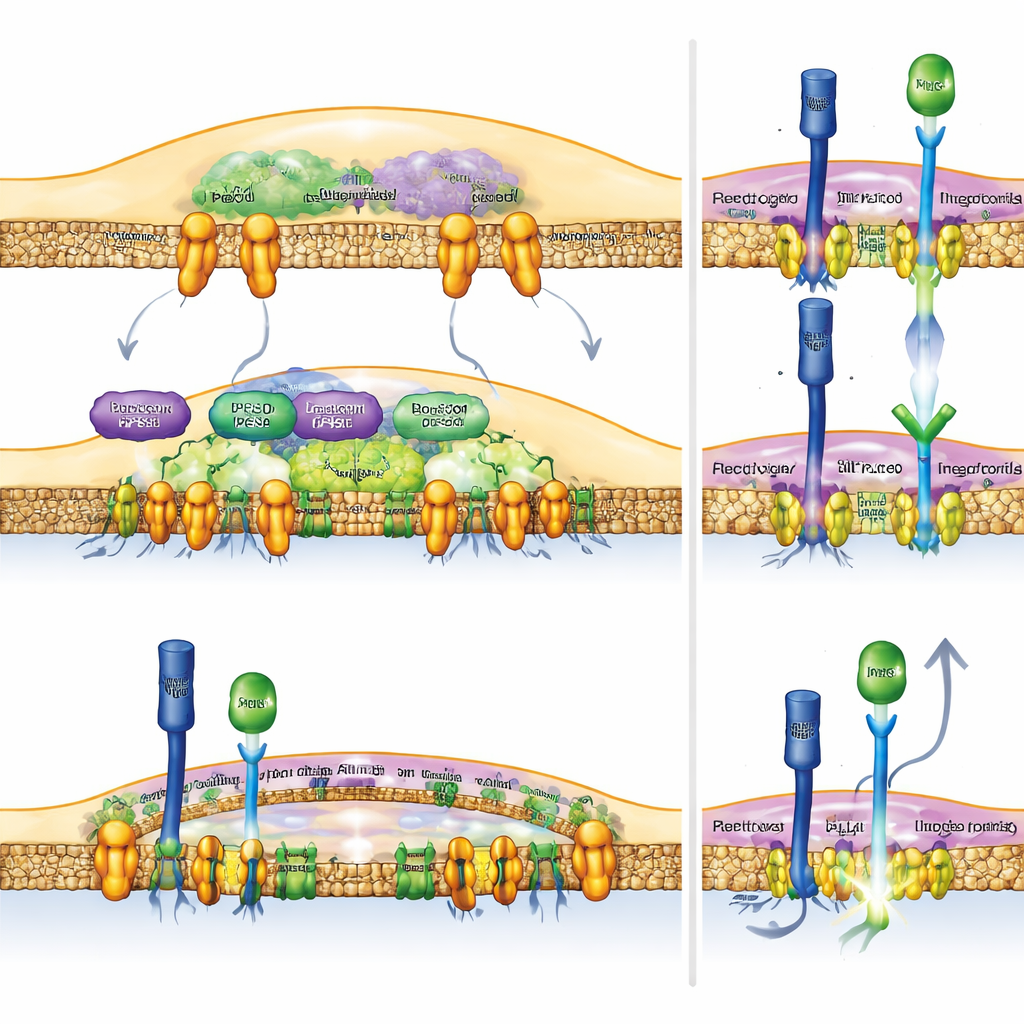
Araştırmacılar Rubicon’u makrofajlardan kaldırdıklarında veya aşağı akıştaki bir enzim olan fosfolipaz D’yi (PLD) engellediklerinde, bu integrin halkası düzgün oluşmadı. Engel olmadan Notch reseptörleri temas bölgesine hareket edebildi ve ölü hücre yüzeyindeki eşleşen ligandlarla etkileşime girebildi. Farelerde, miyeloid hücrelerinde Rubicon eksikliği olan veya PLD’yi engelleyen ilaçlarla tedavi edilen hayvanlarda büyüyen tümörler, makrofajlarda daha güçlü Notch etkinliği, daha iltihaplı gen programları ve tümörlere infiltre olan kanser öldürücü CD8 T hücreleri ile doğal öldürücü hücrelerde bir artış gösterdi. Sonuç olarak tümörler daha yavaş büyüdü.
Kanser Bağışıklığı İçin Bir Kaldıraç Olarak Notch
Notch’u doğrudan makrofajlarda artırmanın bağışıklık sistemine yardımcı olup olmayacağını test etmek için ekip, miyeloid hücreleri sürekli Notch reseptörünün aktif kısmını üreten fareler geliştirdi. Bu fareler daha güçlü antitumor yanıtlar gösterdi: tümörleri daha küçüktü ve tümör içindeki T hücreleri kanser hücrelerini yok etmek için gereken moleküler silahlardan daha fazlasını taşıyordu. Önemli olarak, araştırmacılar Notch’un hedef genlerini açmak için gerekli kilit bir ortak olan RBPJ’yi devre dışı bıraktıklarında, Rubicon kaybı veya PLD inhibisyonunun faydaları ortadan kalktı. Bu, bu müdahalelerin antitumor etkilerinin makrofajlardaki sağlam Notch sinyalleşmesine dayandığını, ilgisiz yan etkilere bağlı olmadığını gösteriyor.
İnsan Tümörlerinden İpuçları ve Gelecek Yönelimleri
Binlerce insan tümöründen elde edilen verileri inceleyen yazarlar, Notch’u aktive eden ligandları yüksek, Rubicon seviyeleri düşük olan kanserlere sahip hastaların Rubicon seviyesi yüksek olanlara göre daha uzun yaşama eğiliminde olduğunu buldu. Bu analiz nedenselliği kanıtlayamazken, tümör mikroçevresinde Notch’u dışlayan bariyeri engellemenin daha etkili immün gözetim lehine dengeyi değiştirebileceği fikriyle uyumlu. Çalışma, Rubicon bağımlı efferositoz yollarını veya PLD’yi hedef alan ilaçların bir gün mevcut immünoterapilerle birleştirilerek makrofajların sessiz çöp toplayıcılardan kansere karşı aktif müttefiklere dönüşmesine yardımcı olabileceğini öne sürüyor.
Bu Hastalar İçin Ne Anlama Geliyor
Basitçe söylemek gerekirse, çalışma makrofajların normalde ölü hücreleri çiğnedikleri yerlere anahtar pro-bağışıklık sinyali Notch’u uzak tutan yerleşik bir kapıya sahip olduğunu ortaya koyuyor. Bu, sağlıklı dokuları gereksiz iltihaptan korur ama istemeden tümörleri koruyabilir. Araştırmacılar kapıyı—genetik değişiklikler veya ilaç tedavisiyle—bozduklarında Notch sinyallerinin geçmesine izin vererek makrofajları T hücrelerini ve diğer savunucuları kanserle savaşmaya çağıracak şekilde yeniden programlayabildiler. Bu içgörülerin tedavilere dönüşmesi için daha yapılacak çok iş olsa da, bunlar yeni bir stratejiye işaret ediyor: yalnızca T hücrelerini daha fazla zorlamak yerine, temizlik ekiplerini yeniden kablolayarak onların susturmaktan vazgeçip vücudun kendi antikanser alarmını güçlendirmesini sağlayabiliriz.
Atıf: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Anahtar kelimeler: efferositoz, Notch sinyalleşmesi, makrofajlar, tümör mikroçevresi, kanser immünoterapisi