Clear Sky Science · pl
Wyłączenie Notch w miejscu kontaktu podczas efefrocytozy ogranicza odporność przeciwnowotworową
Kiedy ekipy sprzątające uciszają wojowników przeciw nowotworom
Nasze ciało nieustannie usuwa obumierające komórki, żeby tkanki pozostały zdrowe i spokojne. Jednak w obrębie guzów ten sam proces sprzątania może działać przeciwko nam, wyciszając układ odpornościowy właśnie wtedy, gdy jest on najbardziej potrzebny — podczas walki z rakiem. Badanie to ujawnia ukryty przełącznik w komórkach odpornościowych, który decyduje, czy sprzątanie uśpi reakcję immunologiczną, czy pomoże ją obudzić do ataku na nowotwór.
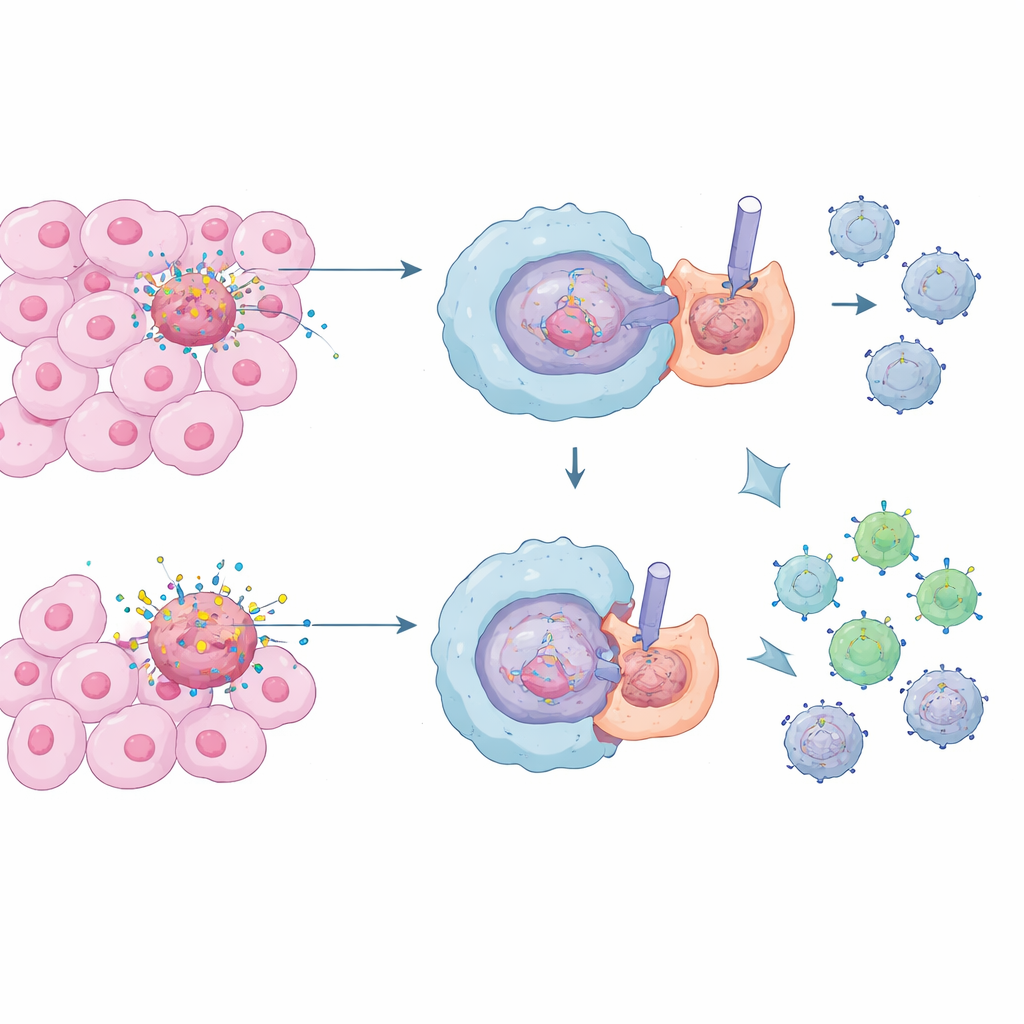
Gospodarze ciała i ich cicha praca
Specjalne komórki odpornościowe zwane makrofagami pełnią rolę sprzątaczy organizmu, pochłaniając i trawiąc martwe oraz umierające komórki w procesie znanym jako efferocytoza. W normalnych warunkach jest to niezbędne: zapobiega uwolnieniu toksycznych treści komórkowych i utrzymuje stan zapalny pod kontrolą, chroniąc nas przed przewlekłym uszkodzeniem tkanek i chorobami autoimmunologicznymi. W guzach natomiast stale zachodzi intensywne obumieranie komórek. Makrofagi, które spokojnie usuwają te szczątki, mogą niechcący tworzyć wokół nowotworu strefę spokoju i tłumienia, utrudniając komórkom zabójczym T rozpoznanie i zniszczenie komórek nowotworowych.
Ukryte bramki sygnałowe na makrofagach
Naukowcy skupili się na systemie komunikacji zwanym Notch, który pomaga komórkom decydować o zachowaniu na podstawie sygnałów od sąsiadów. W makrofagach aktywność Notch zazwyczaj skłania je ku bardziej zapalnemu, przeciwnowotworowemu stanowi. Ku zaskoczeniu zespołu, okazało się, że kiedy zdrowe makrofagi pochłaniają martwe komórki, aktywnie wyłączają sygnalizację Notch właśnie w miejscu kontaktu. Odkryli, że kompleks białkowy zbudowany wokół cząsteczki Rubicon (RUBCN) współpracuje z enzymem VPS34, tworząc fizyczną „barierę” w zewnętrznej błonie makrofaga. Bariera ta powstaje z aktywowanych integryn — białek chwytających, które reorganizują się w ciasny pierścień — dosłownie odsuwając masywne receptory Notch od fragmentu błony, gdzie martwa komórka styka się z makrofagiem, uniemożliwiając w ten sposób uruchomienie Notch.
Przełamanie bariery by wzmocnić atak immunologiczny
Gdy naukowcy usunęli Rubicon z makrofagów lub zablokowali enzym znajdujący się w szlaku, fosfolipazę D (PLD), pierścień integryn przestał prawidłowo się formować. Bez bariery receptory Notch mogły przesunąć się w strefę kontaktu i aktywować swoje dopasowane ligandy na powierzchni martwej komórki. U myszy guzy rozwijające się u zwierząt pozbawionych Rubicon w komórkach mieloidalnych — lub u zwierząt leczonych lekami blokującymi PLD — wykazywały silniejszą aktywność Notch w makrofagach, bardziej zapalne programy genowe oraz napływ komórek CD8 zabijających komórki nowotworowe i komórek NK do guzów. W efekcie guzy rosły wolniej.
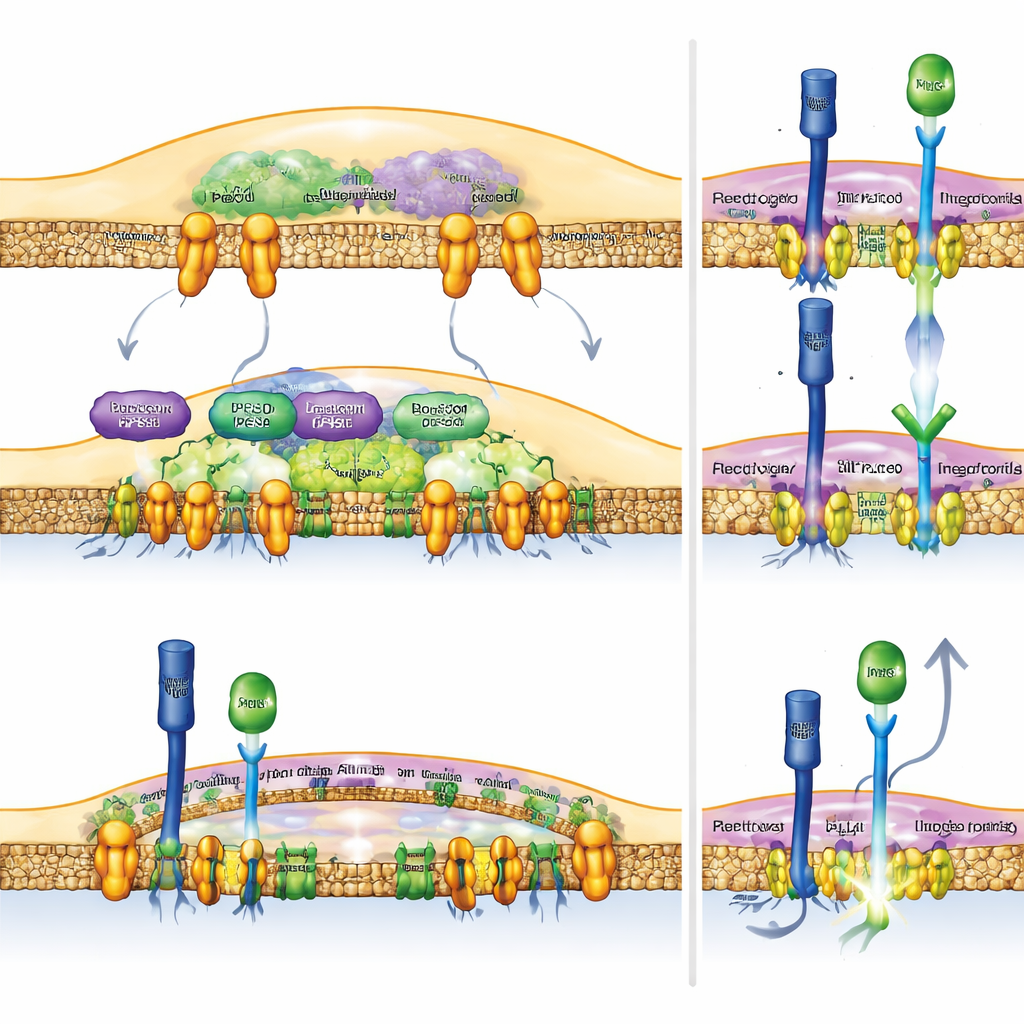
Notch jako dźwignia dla odporności przeciwnowotworowej
Aby sprawdzić, czy bezpośrednie wzmocnienie Notch w makrofagach wystarcza, by wspomóc układ odpornościowy, zespół genetycznie zmodyfikował myszy tak, by ich komórki mieloidalne stale produkowały aktywną część receptora Notch. Te myszy wykazywały silniejsze odpowiedzi przeciwnowotworowe: ich guzy były mniejsze, a komórki T w obrębie guzów nosiły więcej cząsteczek pozwalających niszczyć komórki nowotworowe. Co ważne, gdy badacze wyłączyli RBPJ — kluczowego partnera potrzebnego Notch do uruchamiania genów docelowych — korzyści wynikające z utraty Rubicon lub zahamowania PLD znikały. Pokazuje to, że przeciwnowotworowe efekty tych interwencji zależą od nienaruszonej sygnalizacji Notch w makrofagach, a nie od niezwiązanych skutków ubocznych.
Wskaźniki z ludzkich nowotworów i kierunki na przyszłość
Analiza danych z tysięcy ludzkich nowotworów wykazała, że pacjenci, których guzy wykazywały wysokie poziomy ligandów aktywujących Notch przy jednocześnie niskich poziomach Rubicon, częściej przeżywali dłużej niż ci z wysokim poziomem Rubicon. Choć ta analiza nie dowodzi przyczynowości, zgadza się z ideą, że zablokowanie bariery wykluczającej Notch w mikrośrodowisku guza może przesunąć równowagę na korzyść skuteczniejszego nadzoru immunologicznego. Wyniki sugerują, że leki celujące w szlaki efferocytozy zależne od Rubicon lub w PLD mogłyby w przyszłości być łączone z istniejącymi immunoterapiami, aby pomóc makrofagom przekształcić się z cichych zbieraczy odpadów w aktywnych sojuszników przeciw nowotworowi.
Co to oznacza dla pacjentów
Mówiąc prosto, badanie ujawnia, że makrofagi mają wbudowaną bramkę, która normalnie trzyma kluczowy, proimmunologiczny sygnał Notch z dala od miejsc, gdzie rozkładają martwe komórki. Chroni to zdrowe tkanki przed niepotrzebnym stanem zapalnym, ale może niezamierzenie osłaniać guzy. Poprzez zaburzenie tej bramki — przez zmiany genetyczne lub leczenie lekami — badacze mogli dopuścić sygnały Notch do działania, przeprogramowując makrofagi tak, by mobilizowały komórki T i innych obrońców przeciw rakowi. Choć wciąż potrzeba wielu badań, zanim te odkrycia przełożą się na terapie, wskazują one na nową strategię: zamiast tylko wzmacniać komórki T, możemy także przeokreślić ekipy sprzątające, by przestały tłumić, a zaczęły wzmacniać własny alarm przeciwnowotworowy organizmu.
Cytowanie: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Słowa kluczowe: efefrocytoza, sygnalizacja Notch, makrofagi, mikrośrodowisko guza, immunoterapia przeciwnowotworowa