Clear Sky Science · de
Ausschluss von Notch an der Kontaktstelle während der Efferocytose begrenzt die krebsabwehrende Immunität
Wenn die Aufräumtrupps die Krebsbekämpfer zum Schweigen bringen
Unser Körper beseitigt ständig sterbende Zellen, um Gewebe gesund und ruhig zu halten. Innerhalb von Tumoren kann derselbe Reinigungsprozess jedoch nach hinten losgehen, weil er das Immunsystem beruhigt – gerade dann, wenn wir es am dringendsten brauchen: im Kampf gegen Krebs. Die Studie enthüllt einen verborgenen Schalter in Immunzellen, der entscheidet, ob das Aufräumen die Immunantwort in den Schlaf wiegt oder sie weckt, damit sie Tumore angreift.
Die Hausmeister des Körpers und ihre stille Arbeit
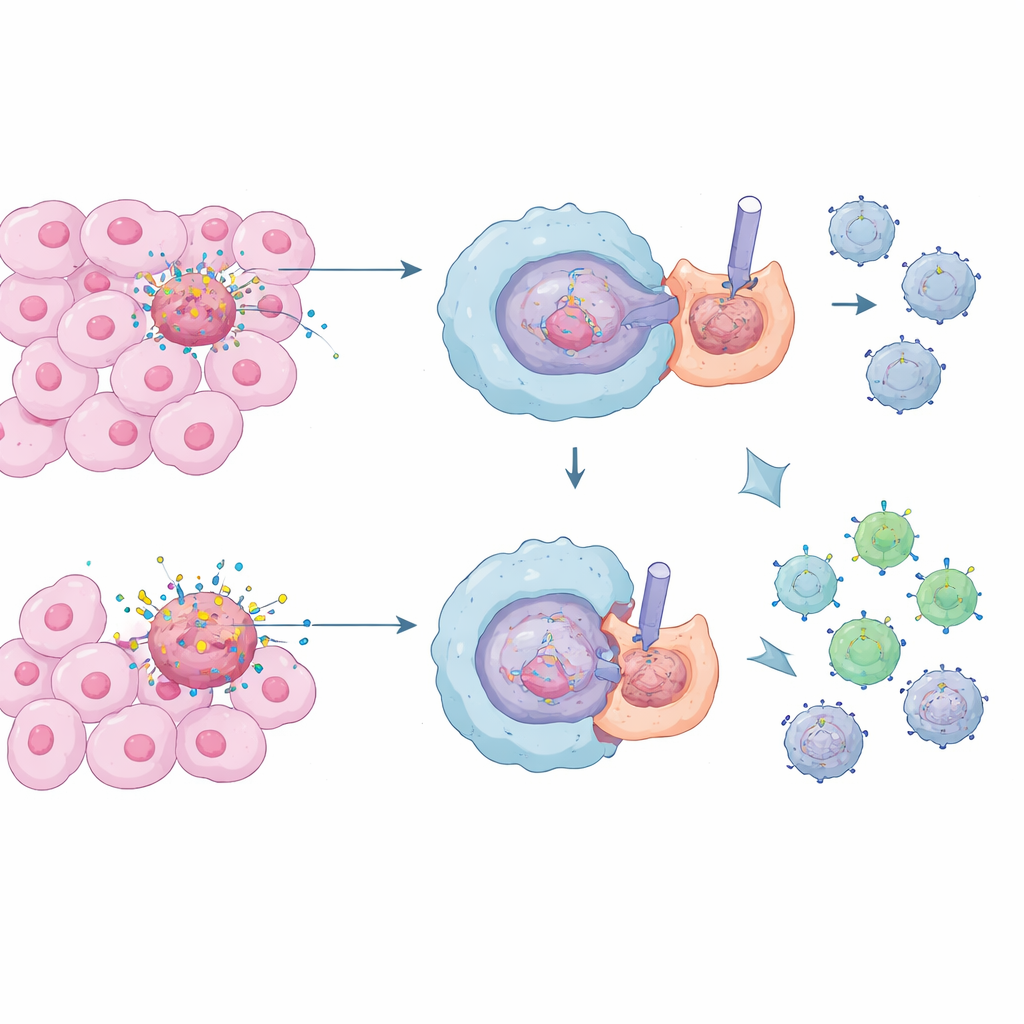
Spezielle Immunzellen, Makrophagen genannt, fungieren als Hausmeister des Körpers: sie verschlingen und verdauen tote und sterbende Zellen in einem Prozess, der als Efferocytose bekannt ist. Unter normalen Bedingungen ist das lebenswichtig: Es verhindert das Austreten toxischer Zellinhalte und hält Entzündungen in Schach, was uns vor chronischen Gewebeschäden und Autoimmunerkrankungen schützt. In Tumoren herrscht hingegen ein ständiger Sturm des Zelltods. Makrophagen, die diese Körperchen still beseitigen, können eine ruhige, unterdrückende Nachbarschaft um den Krebs herum schaffen und es so den zytotoxischen T‑Zellen erschweren, bösartige Zellen zu erkennen und zu zerstören.
Ein verborgener Signalriegel auf Makrophagen
Die Forschenden konzentrierten sich auf ein Kommunikationssystem namens Notch, das Zellen dabei hilft, ihr Verhalten anhand von Signalen der Nachbarn zu bestimmen. In Makrophagen tendiert Notch‑Aktivität dazu, sie in einen entzündlicheren, tumorfighterischen Zustand zu treiben. Überraschenderweise stellten die Autorinnen und Autoren fest, dass gesunde Makrophagen beim Verschlingen toter Zellen die Notch‑Signalübertragung genau an der Kontaktstelle aktiv herunterfahren. Sie entdeckten, dass ein Proteinkomplex um ein Molekül namens Rubicon (RUBCN) zusammen mit einer weiteren Enzymkomponente, VPS34, eine physische „Barriere“ in der äußeren Membran des Makrophagen aufbaut. Diese Barriere besteht aus aktivierten Integrinen – greifenden Proteinen, die sich zu einem engen Ring umformen – und schieben die sperrigen Notch‑Rezeptoren förmlich von der Stelle weg, an der die tote Zelle den Makrophagen berührt, sodass Notch dort nicht aktiviert werden kann.
Die Barriere durchbrechen, um die Immunangriffe zu verstärken
Wenn die Forschenden Rubicon aus Makrophagen entfernten oder ein nachgeschaltetes Enzym namens Phospholipase D (PLD) blockierten, bildete sich dieser Integrinring nicht mehr richtig. Ohne die Barriere konnten Notch‑Rezeptoren in die Kontaktzone wandern und mit passenden Liganden auf der Oberfläche der toten Zelle interagieren. In Mäusen zeigten Tumore, die in Tieren wuchsen, denen Rubicon in myeloiden Zellen fehlte – oder die mit PLD‑hemmenden Medikamenten behandelt wurden –, eine stärkere Notch‑Aktivität in Makrophagen, expressionell verstärkte entzündliche Programme und einen Zustrom krebsabtötender CD8‑T‑Zellen und natürlicher Killerzellen in die Tumoren. Infolgedessen wuchsen die Tumore langsamer.
Notch als Hebel für die Krebsimmunität
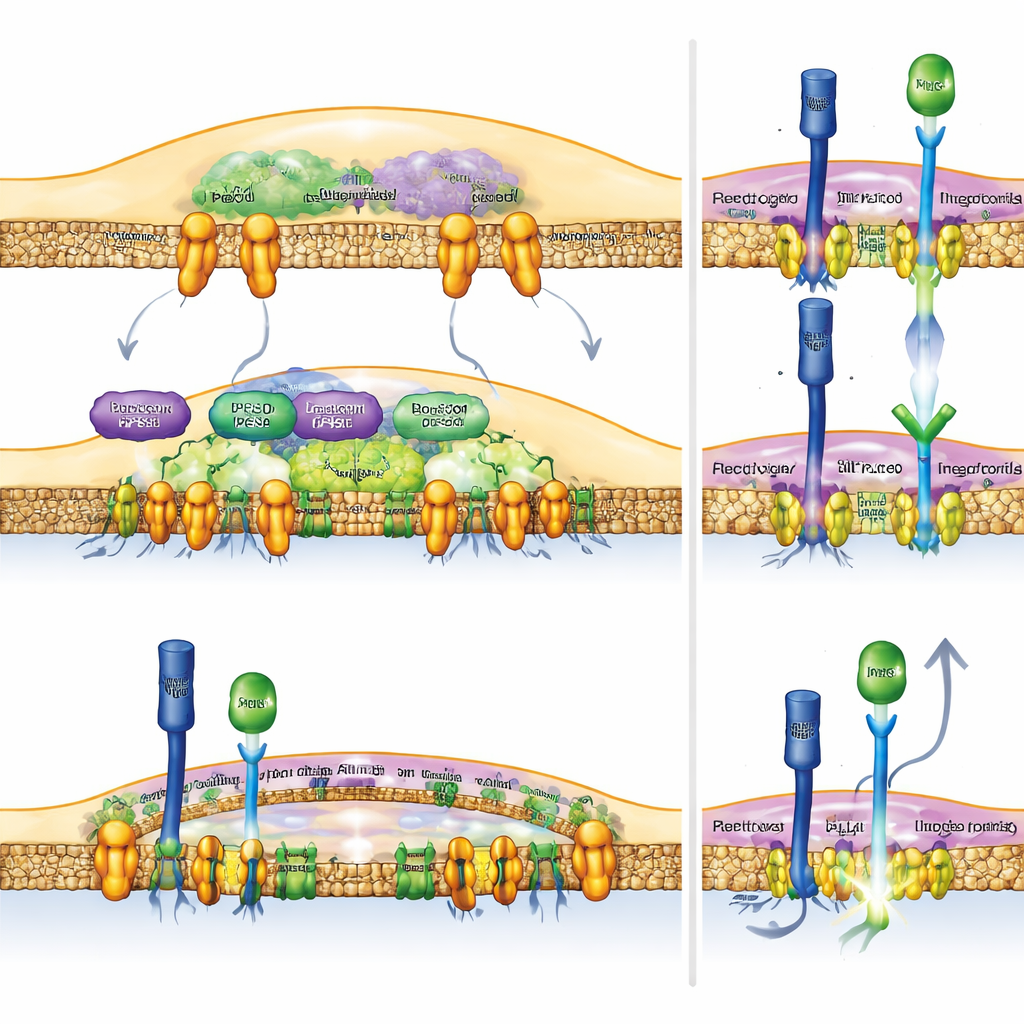
Um zu prüfen, ob eine direkte Erhöhung von Notch in Makrophagen ausreicht, das Immunsystem zu unterstützen, erzeugte das Team Mäuse, deren myeloide Zellen dauerhaft den aktiven Teil des Notch‑Rezeptors produzieren. Diese Mäuse entwickelten stärkere antitumorale Antworten: Ihre Tumore waren kleiner und die T‑Zellen innerhalb der Tumore trugen mehr der molekularen Waffen, die nötig sind, um Krebszellen zu zerstören. Wichtig ist, dass die Vorteile durch Verlust von Rubicon oder PLD‑Hemmung verschwanden, wenn die Forschenden RBPJ deaktivierten – einen Schlüsselfaktor, den Notch braucht, um seine Zielgene anzuschalten. Das zeigt, dass die antitumoralen Effekte dieser Eingriffe von intaktem Notch‑Signaling in Makrophagen abhängen und nicht von unzusammenhängenden Nebeneffekten.
Hinweise aus menschlichen Tumoren und Ausblick
Beim Blick auf Daten aus Tausenden menschlicher Tumore fanden die Autorinnen und Autoren, dass Patientinnen und Patienten, deren Tumore hohe Mengen an Notch‑aktivierenden Liganden, aber niedrige Rubicon‑Spiegel aufwiesen, tendenziell länger überlebten als solche mit hohen Rubicon‑Werten. Während diese Analyse keinen ursächlichen Zusammenhang beweisen kann, passt sie zu der Idee, dass das Blockieren der Notch‑ausschließenden Barriere in der Tumormikroumgebung das Gleichgewicht zugunsten einer effektiveren immunologischen Überwachung verschieben kann. Die Arbeit legt nahe, dass Medikamente, die Rubicon‑abhängige Efferocytose‑Wege oder PLD anvisieren, eines Tages mit bestehenden Immuntherapien kombiniert werden könnten, um Makrophagen von stillen Müllsammlern in aktive Verbündete gegen Krebs zu verwandeln.
Was dies für Patientinnen und Patienten bedeutet
Kurz gesagt zeigt die Studie, dass Makrophagen ein eingebautes Tor tragen, das normalerweise ein wichtiges pro‑immunes Signal, Notch, von den Stellen fernhält, an denen sie tote Zellen abarbeiten. Das schützt gesunde Gewebe vor unnötiger Entzündung, kann aber unbeabsichtigt Tumore abschirmen. Durch das Stören dieses Tores – durch genetische Veränderungen oder medikamentöse Behandlung – konnten die Forschenden Notch‑Signale durchlassen und Makrophagen so umprogrammieren, dass sie T‑Zellen und andere Abwehrkräfte gegen Krebs mobilisieren. Obwohl noch viel Arbeit nötig ist, bevor sich diese Erkenntnisse in Therapien übersetzen lassen, deuten sie auf eine neue Strategie: Anstatt ausschließlich die T‑Zellen stärker zu treiben, könnte man auch die Aufräumtrupps so umgestalten, dass sie das körpereigene Krebsalarm‑System nicht mehr dämpfen, sondern verstärken.
Zitation: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Schlüsselwörter: Efferocytose, Notch-Signaling, Makrophagen, Tumormikroumgebung, Krebsimmuntherapie