Clear Sky Science · ru
Исключение Notch из зоны контакта во время эффероцитоза ограничивает противораковый иммунитет
Когда уборщики отключают борцов с раком
Наш организм постоянно очищает умирающие клетки, чтобы ткани оставались здоровыми и спокойными. Но в опухолях тот же процесс уборки может работать против нас, успокаивая иммунную систему именно тогда, когда это наименее желанно — во время борьбы с раком. В этом исследовании обнаружен скрытый переключатель в иммунных клетках, который решает, приведёт ли очистка клеток к усыплению иммунного ответа или, наоборот, к его пробуждению для атаки на опухоль.
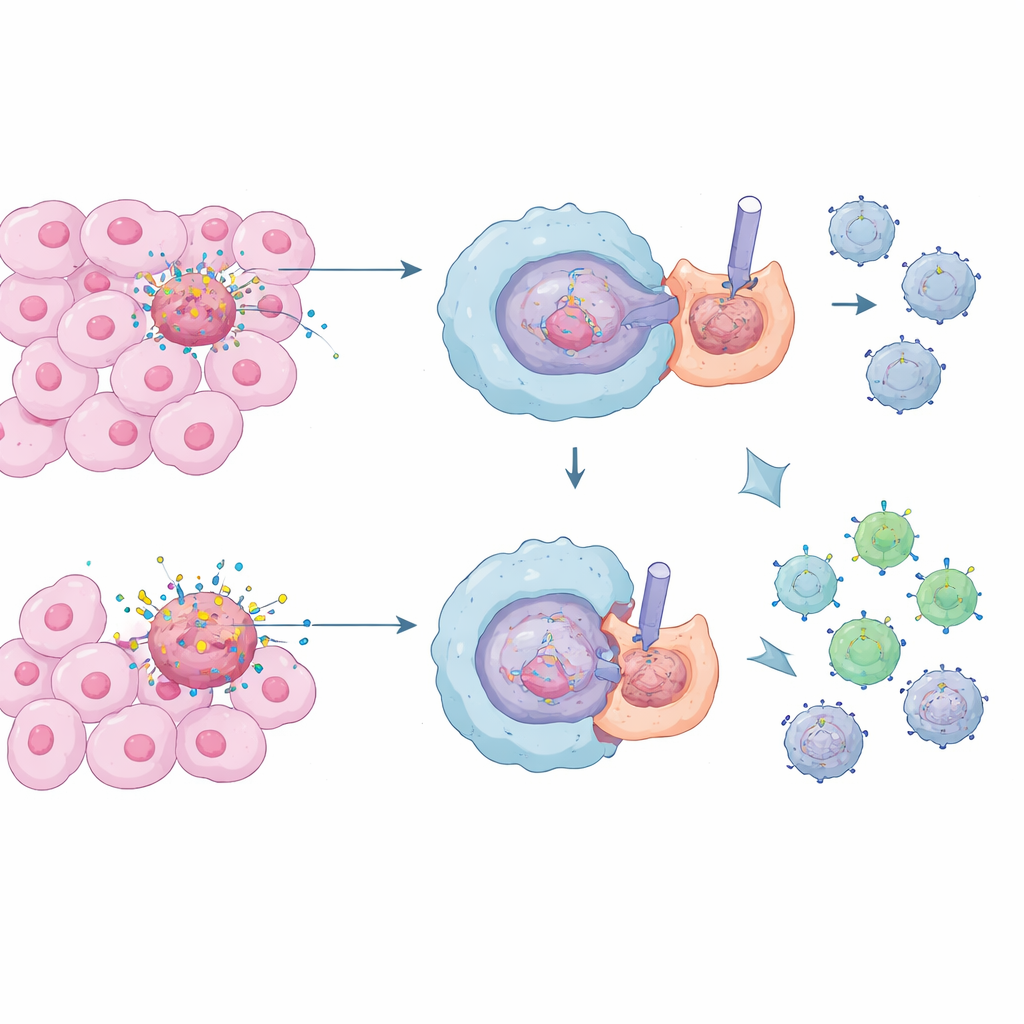
Телесные дворники и их тихая работа
Специальные иммунные клетки, называемые макрофагами, действуют как дворники организма: они поглощают и переваривают мёртвые и умирающие клетки в процессе, известном как эффероцитоз. В норме это жизненно важно: предотвращается попадание токсического содержимого клеток и удерживается воспаление под контролем, что защищает от хронического повреждения тканей и аутоиммунных заболеваний. В опухолях же постоянно идёт шквал клеточной гибели. Макрофаги, которые тихо убирают эти трупики, могут формировать вокруг рака спокойную, супрессивную среду, делая труднее для «киллерных» Т‑клеток распознать и уничтожить злостные клетки.
Скрытый шлюз сигнализации на макрофагах
Исследователи сосредоточились на системе коммуникации под названием Notch, которая помогает клеткам решать, как себя вести, в зависимости от сигналов соседей. В макрофагах активность Notch склоняет их к более провоспалительному, антипухолевому состоянию. Удивительно, но команда обнаружила, что когда здоровые макрофаги поглощают мёртвые клетки, они активно выключают Notch‑сигнал именно в точке контакта. Они установили, что белковый комплекс вокруг молекулы Rubicon (RUBCN) в сотрудничестве с ферментом VPS34 создаёт физический «барьер» в наружной мембране макрофага. Этот барьер формируется из активированных интегринов — «хватательных» белков, которые перестраиваются в плотное кольцо и буквально отталкивают массивные рецепторы Notch от участка, где мёртвая клетка соприкасается с макрофагом, мешая включению Notch.
Разрушение барьера для усиления иммунной атаки
Когда учёные удаляли Rubicon из макрофагов или блокировали более низкоуровневый фермент фосфолипазу D (PLD), это интегриновое кольцо переставало правильно формироваться. Без барьера рецепторы Notch могли перемещаться в зону контакта и взаимодействовать со своими лигандами на поверхности мёртвой клетки. У мышей опухоли, растущие в животных с отсутствием Rubicon в миелоидных клетках или у тех, кого лечили препаратами, блокирующими PLD, показали усиленную активность Notch в макрофагах, включение провоспалительных генетических программ и приток CD8‑Т‑клеток и естественных киллеров в опухоли. В результате опухоли росли медленнее.
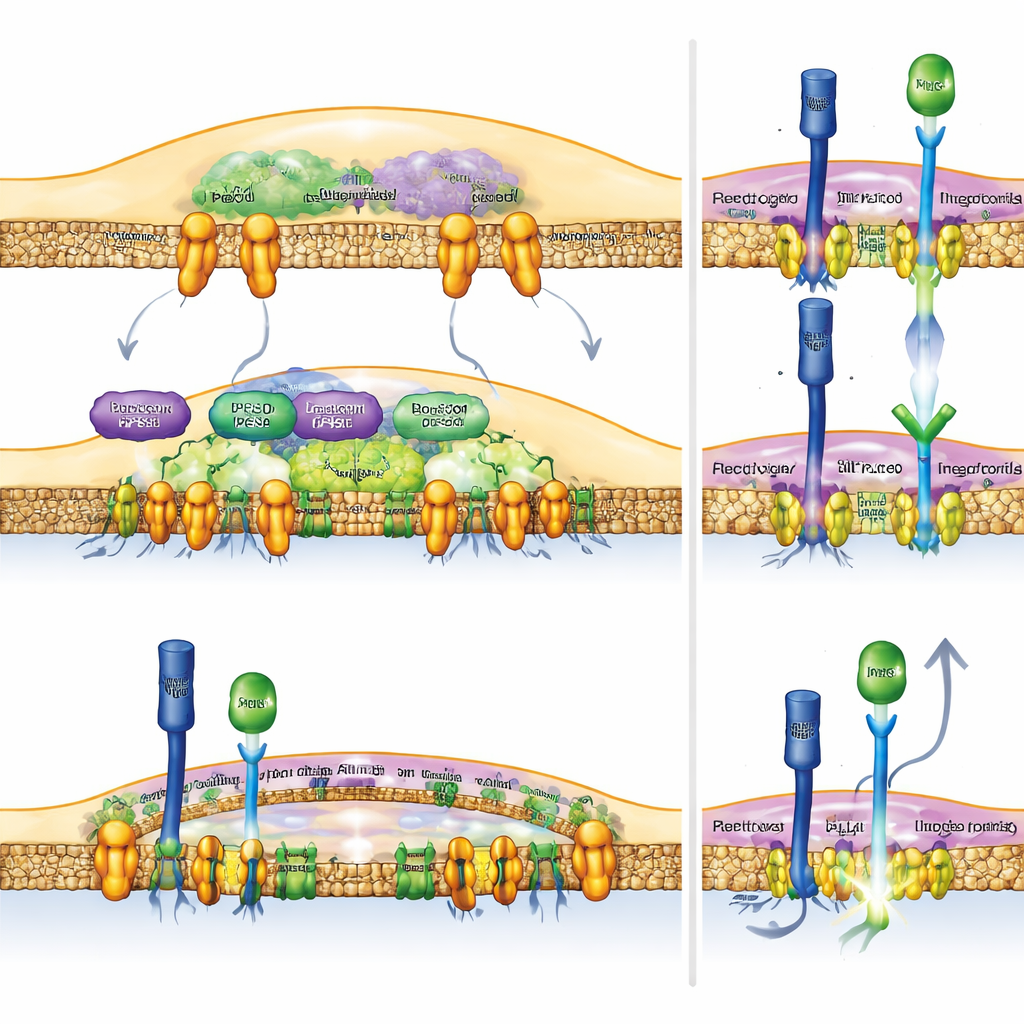
Notch как рычаг противоракового иммунитета
Чтобы проверить, достаточно ли простого усиления Notch в макрофагах для помощи иммунной системе, команда создала мышей, чьи миелоидные клетки постоянно продуцировали активную часть рецептора Notch. Эти мыши развили более мощные антитуморные ответы: их опухоли были меньших размеров, а Т‑клетки внутри опухолей несли больше молекулярного «оружия», необходимого для разрушения раковых клеток. Важно, что когда исследователи выключали RBPJ — ключевого партнёра, необходимого Notch для включения целевых генов — преимущества от потери Rubicon или ингибирования PLD исчезали. Это показывает, что антитуморные эффекты этих вмешательств зависят от целостной Notch‑сигнализации в макрофагах, а не от сопутствующих побочных эффектов.
Улики из опухолей человека и направления дальнейшей работы
Анализируя данные тысяч человеческих опухолей, авторы обнаружили, что пациенты, у которых опухоли экспрессировали высокие уровни лигандов, активирующих Notch, но низкие уровни Rubicon, как правило, жили дольше, чем те, у кого был высокий уровень Rubicon. Хотя этот анализ сам по себе не доказывает причинно‑следственную связь, он согласуется с идеей, что блокирование барьера, исключающего Notch в микроокружении опухоли, может склонить баланс в сторону более эффективного иммунного надзора. Работа указывает на то, что препараты, нацеленные на пути эффероцитоза, зависящие от Rubicon, или на PLD, могли бы в будущем сочетаться с уже существующими иммунотерапиями, чтобы превратить макрофагов из тихих сборщиков мусора в активных союзников против рака.
Что это значит для пациентов
Проще говоря, исследование показывает, что макрофаги несут встроенный «затвор», который обычно удерживает ключевой провоспалительный сигнал Notch подальше от мест, где они пережёвывают мёртвые клетки. Это защищает здоровые ткани от ненужного воспаления, но может непреднамеренно защищать опухоли. При нарушении этого затвора — генетически или с помощью лекарств — исследователи могли пропустить сигналы Notch, перепрограммировать макрофаги и мобилизовать Т‑клетки и других защитников против рака. Несмотря на то что до превращения этих открытий в терапию ещё далеко, они указывают на новую стратегию: вместо того чтобы только усиленно стимулировать Т‑клетки, можно также перенастроить «уборочные бригады», чтобы они перестали заглушать и начали усиливать собственную противораковую сигнализацию организма.
Цитирование: Li, Z., Xu, B., Sharma, P. et al. Exclusion of Notch from the contact site during efferocytosis restricts anticancer immunity. Nat Immunol 27, 750–761 (2026). https://doi.org/10.1038/s41590-026-02452-3
Ключевые слова: эффероцитоз, Notch-сигнализация, макрофаги, опухолевый микроклимат, раковая иммунотерапия