Clear Sky Science · zh
异源寡聚驱动真核细胞过氧化物还原酶的结构可塑性
为保护细胞而自我重塑的蛋白质
在每个细胞内部,都在与可能损伤 DNA、蛋白质和脂质的活性氧分子进行一场无声的斗争。一类称为过氧化物还原酶(peroxiredoxin,Prx)的酶担当前线防御,解毒这些活性物质并帮助细胞感知氧化水平的变化。多年来,科学家普遍认为每种过氧化物还原酶以由相同构件组成的均一簇体单独工作。本研究颠覆了这一观点,表明许多过氧化物还原酶实际上会与密切相关的同源体混合配对,形成具有可变形状和稳定性的杂合装配体,这些变化可能微调细胞应对压力的方式。
为什么蛋白质协作很重要
过氧化物还原酶是从酵母到人类与植物等多种生物中含量最高的蛋白质之一。它们清除过氧化氢——代谢的反应性副产物,同时也充当分子伴护蛋白,帮助其他蛋白维持构象。教科书中的经典图景显示这些酶要么组装成一对(二聚体),要么形成十个单元的环状结构(十聚体),而且通常被认为是由单一同系型构成。然而,许多细胞在同一细胞区室中携带两种几乎相同的过氧化物还原酶同系型。作者提出了一个简单却根本性的问题:这些同系型真会互不相融,还是会组装成具有新特性的混合复合体?
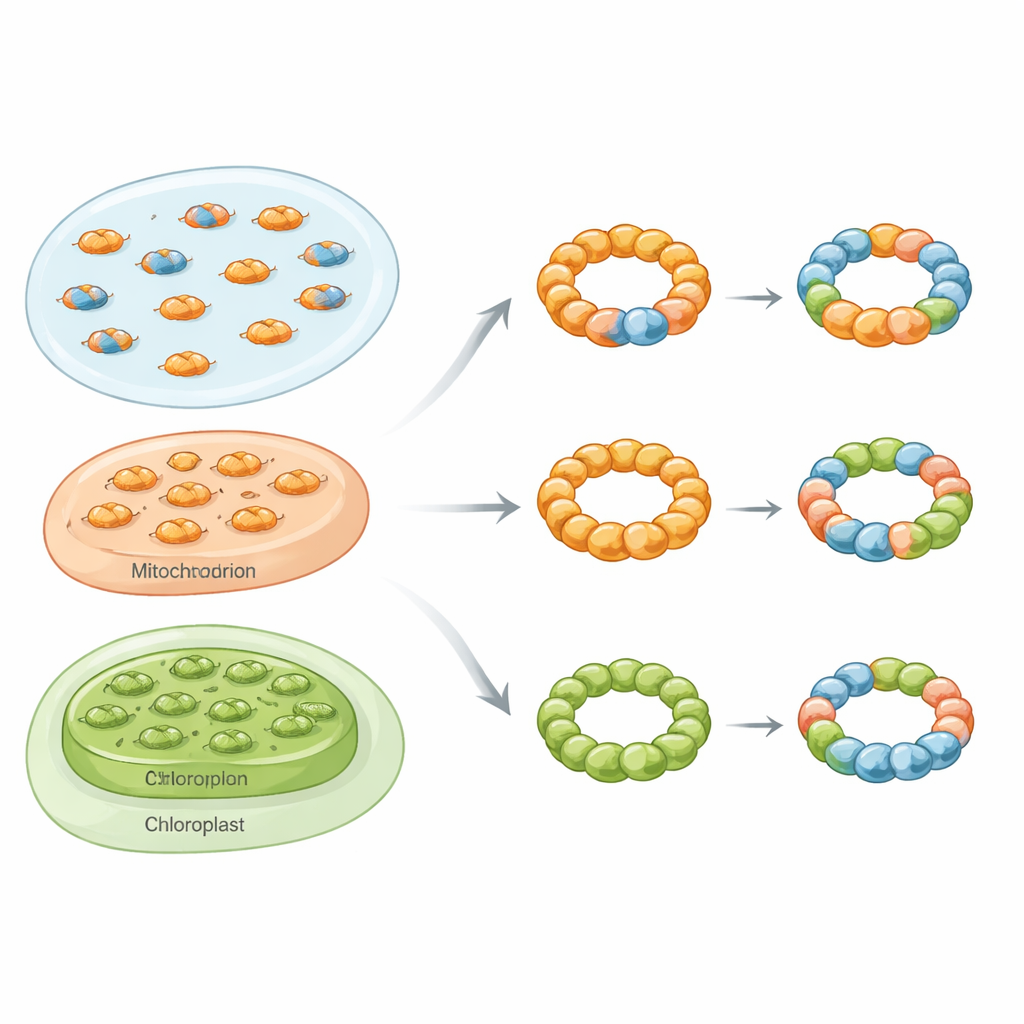
跨生物界的混合环体
研究者使用生化纯化、本征质量光度法、本征电镜和活细胞荧光测定等工具,证明了混合或异源寡聚的过氧化物还原酶复合体并非罕见现象。在面包酵母中,他们关注两种胞质同系型 Tsa1 和 Tsa2。当这两种蛋白在细菌中共同表达时,它们既能形成混合二聚体,也能形成混合十聚体,呈现出不同的亚基比例谱。在电子显微镜下,这些组装体呈现出典型的环状颗粒,证实了 Tsa1 与 Tsa2 可以共享相同的结构支架,而不是只形成各自独立的环。
酵母细胞中的应激触发重塑
为了检验这种混合在活细胞中是否有意义,团队用荧光传感器标记 Tsa1 和 Tsa2 并追踪它们在酵母中的行为。在正常生长条件下,Tsa1 丰富而 Tsa2 稀少,且 Tsa1 主要以较小的形态存在。当细胞暴露于过氧化氢时,Tsa2 的表达迅速上升,本征凝胶上出现对应较大环状组装体的明确条带。有趣的是,即便仅在 Tsa1 环中引入一到两个 Tsa2 单元,也足以在加温时稳定十聚体结构,防止其解体。酶动力学分析显示,这些杂合环体仍保持完全活性,反应速率与纯同系型相近,但更不容易被过氧化而失活。
调节蛋白功能的一种广泛策略
故事并不限于酵母。在人类肾细胞中,作者通过离子交换色谱分离了两种紧密相关的过氧化物还原酶 PRDX1 与 PRDX2。在缺失其中一种同系型的细胞中,剩余蛋白各自作为不同物种洗脱;而在正常细胞中,这两种同系型在共同的洗脱范围内共同出现,支持存在混合复合体的结论。在工程化酵母中表达人类、植物和寄生虫的过氧化物还原酶的类似试验显示,来自这些生物的同系型都能形成功能性的杂合体。在植物叶绿体酶和导致利什曼病的寄生虫中,引入更偏好十聚体的同系型可以将更倾向二聚体的伙伴拉入更大的环体,或根据主导亚基的不同反向破坏环体稳定性。对1500 多个真核基因组的生物信息学分析显示,超过80% 的物种很可能在同一区室中存在多种 Prx1 型过氧化物还原酶,表明这种混合更可能是常态而非例外。
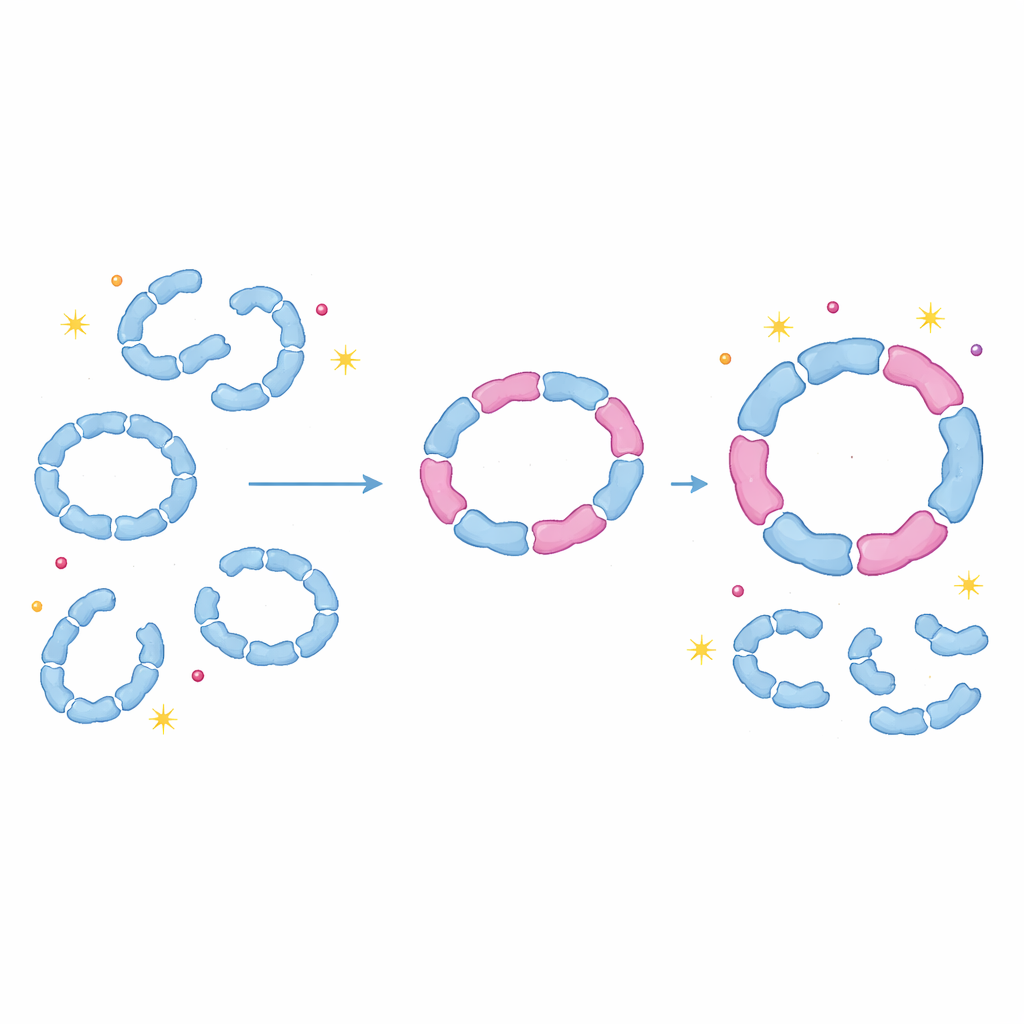
作为可调减震器的蛋白质
通过证明过氧化物还原酶常规地构建混合环体和二聚体,这项工作挑战了长期以来每种同系型仅作为纯装配体功能的假设。相反,细胞似乎利用异源寡聚作为一种灵活手段,来调整这些环体的稳定性、对损伤的敏感性以及在解毒与伴护功能之间切换的时机。比如在氧化应激期间,某一同系型表达量的微小变化就能通过同时重塑大量混合复合体而在系统中产生连锁效应。对非专业读者而言,关键信息是:蛋白质复合体的行为不像僵硬的乐高模型,更像可调的减震器——通过替换不同但兼容的部件,细胞能够微妙地调控其对氧化应激的防护,这对衰老、癌症、感染以及其他氧化还原平衡失衡相关的病理具有重要影响。
引用: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
关键词: 过氧化物还原酶, 氧化应激, 蛋白复合体, 氧化还原信号传导, 细胞适应