Clear Sky Science · pt
Hetero-oligomerização impulsiona a plasticidade estrutural de peroxiredoxinas eucarióticas
Proteínas que se remodelam para proteger nossas células
Dentro de cada célula, trava-se uma batalha silenciosa contra moléculas reativas de oxigênio que podem danificar DNA, proteínas e lipídios. Uma família de enzimas chamadas peroxiredoxinas atua como linha de frente dessa defesa, detoxificando essas espécies reativas e ajudando as células a perceber variações nos níveis de oxidação. Por anos, os cientistas supuseram que cada peroxiredoxina funcionava isoladamente em aglomerados uniformes compostos por blocos idênticos. Este estudo derruba essa visão ao mostrar que muitas peroxiredoxinas, na verdade, combinam-se com parentes estreitamente relacionados, formando montagens híbridas que alteram forma e estabilidade de maneiras que podem ajustar finamente como as células lidam com o estresse.
Por que o trabalho conjunto de proteínas importa
As peroxiredoxinas estão entre as proteínas mais abundantes em organismos que vão da levedura a plantas e humanos. Elas removem peróxido de hidrogênio, um subproduto reativo do metabolismo, e também atuam como chaperonas moleculares que ajudam outras proteínas a manter sua conformação. A imagem clássica dos livros mostra essas enzimas montando-se em pares (dímeros) ou em anéis em forma de rosquinha de dez unidades (decâmeros), mas sempre construídos a partir de uma única isoforma por vez. No entanto, muitas células abrigam duas versões quase gêmeas da mesma peroxiredoxina no mesmo compartimento. Os autores colocaram uma pergunta simples, porém fundamental: essas isoformas realmente permanecem separadas, ou elas se montam em complexos mistos com propriedades novas?
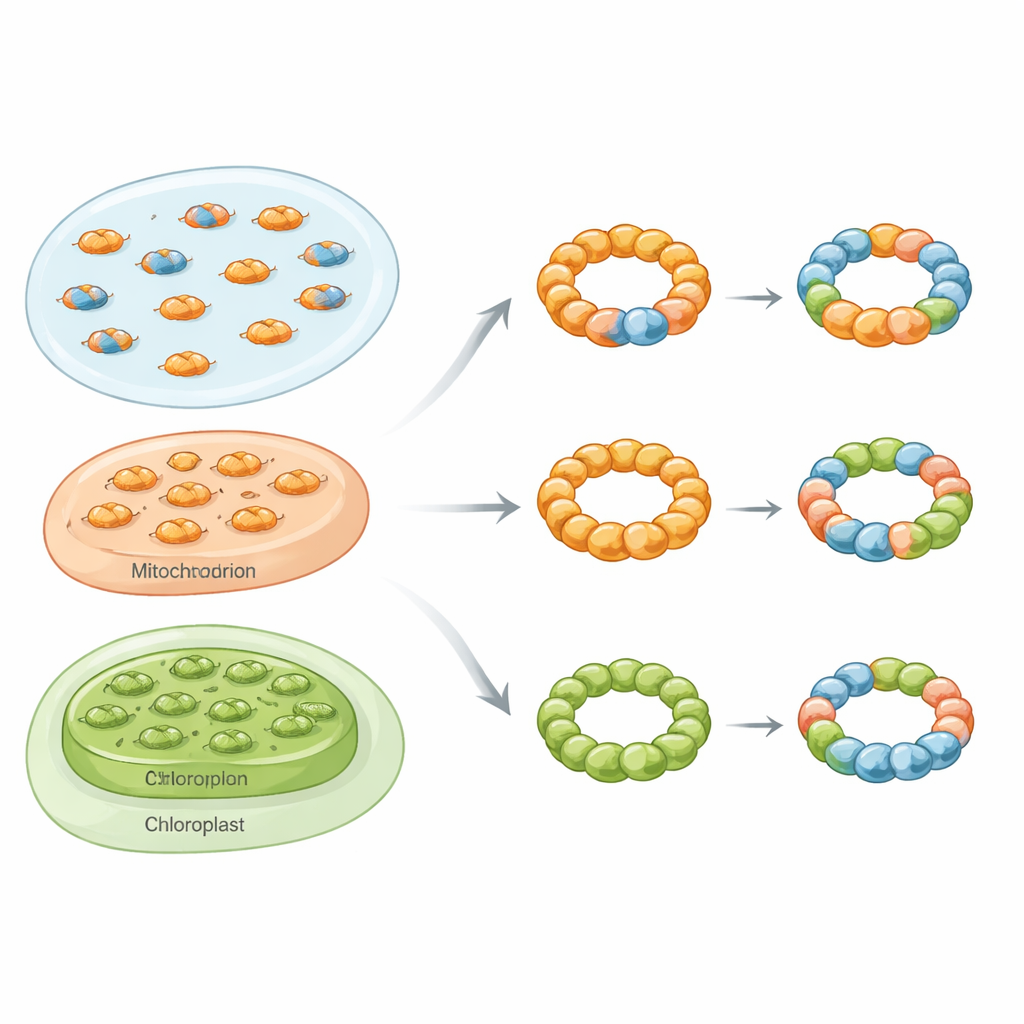
Anéis mistos através dos reinos da vida
Usando um conjunto de técnicas que incluiu purificação bioquímica, fotometria de massa nativa, microscopia eletrônica e ensaios de fluorescência em células vivas, os pesquisadores mostram que complexos hetero‑oligoméricos de peroxiredoxina não são curiosidades raras. Na levedura de padeiro, eles se concentraram em duas isoformas citosólicas chamadas Tsa1 e Tsa2. Quando as duas proteínas foram produzidas juntas em bactérias, formaram tanto dímeros mistos quanto decâmeros mistos com um espectro de proporções entre subunidades. Ao microscópio eletrônico, essas montagens apareciam como partículas características em forma de anel, confirmando que Tsa1 e Tsa2 podem compartilhar o mesmo arcabouço estrutural em vez de formar apenas anéis separados.
Remodelação desencadeada por estresse em células de levedura
Para testar se essa mistura importa dentro de células vivas, a equipe marcou Tsa1 e Tsa2 com um sensor fluorescente e acompanhou seu comportamento na levedura. Em condições normais de crescimento, Tsa1 é abundante enquanto Tsa2 é escassa, e Tsa1 permanece majoritariamente em formas menores. Quando as células foram expostas ao peróxido de hidrogênio, a produção de Tsa2 disparou, e faixas claras correspondendo a montagens maiores em forma de anel apareceram em géis nativos. Intrigantemente, mesmo a incorporação de apenas uma ou duas unidades de Tsa2 em um anel de Tsa1 foi suficiente para estabilizar a estrutura de dez unidades contra a dissociação quando aquecida. Cinéticas enzimáticas mostraram que esses anéis híbridos permaneceram totalmente ativos, com taxas de reação semelhantes às formas puras, porém com menor tendência a se hiperóxidar e inativar.
Uma estratégia difundida para ajustar a função proteica
A história não parou na levedura. Em células renais humanas, os autores separaram duas peroxiredoxinas intimamente relacionadas, PRDX1 e PRDX2, por cromatografia de troca iônica. Em células que careciam de uma isoforma, cada proteína remanescente eluía como uma espécie distinta. Em células normais, entretanto, ambas as isoformas coeluíam em uma faixa compartilhada, consistente com a presença de complexos mistos. Testes semelhantes em leveduras engenheiradas para produzir peroxiredoxinas humanas, de plantas e de parasitas mostraram que pares de todos esses organismos podiam formar híbridos funcionais. Em enzimas do cloroplasto vegetal e em um parasita que causa leishmaniose, introduzir uma isoforma mais inclinada ao decâmero podia puxar uma parceira mais dímerica para anéis maiores, ou inversamente desestabilizar anéis dependendo de qual subunidade predominasse. Análises bioinformáticas de mais de 1.500 genomas eucarióticos revelaram que mais de 80% das espécies provavelmente abrigam múltiplas peroxiredoxinas do tipo Prx1 no mesmo compartimento, sugerindo que tal mistura é a regra e não a exceção.
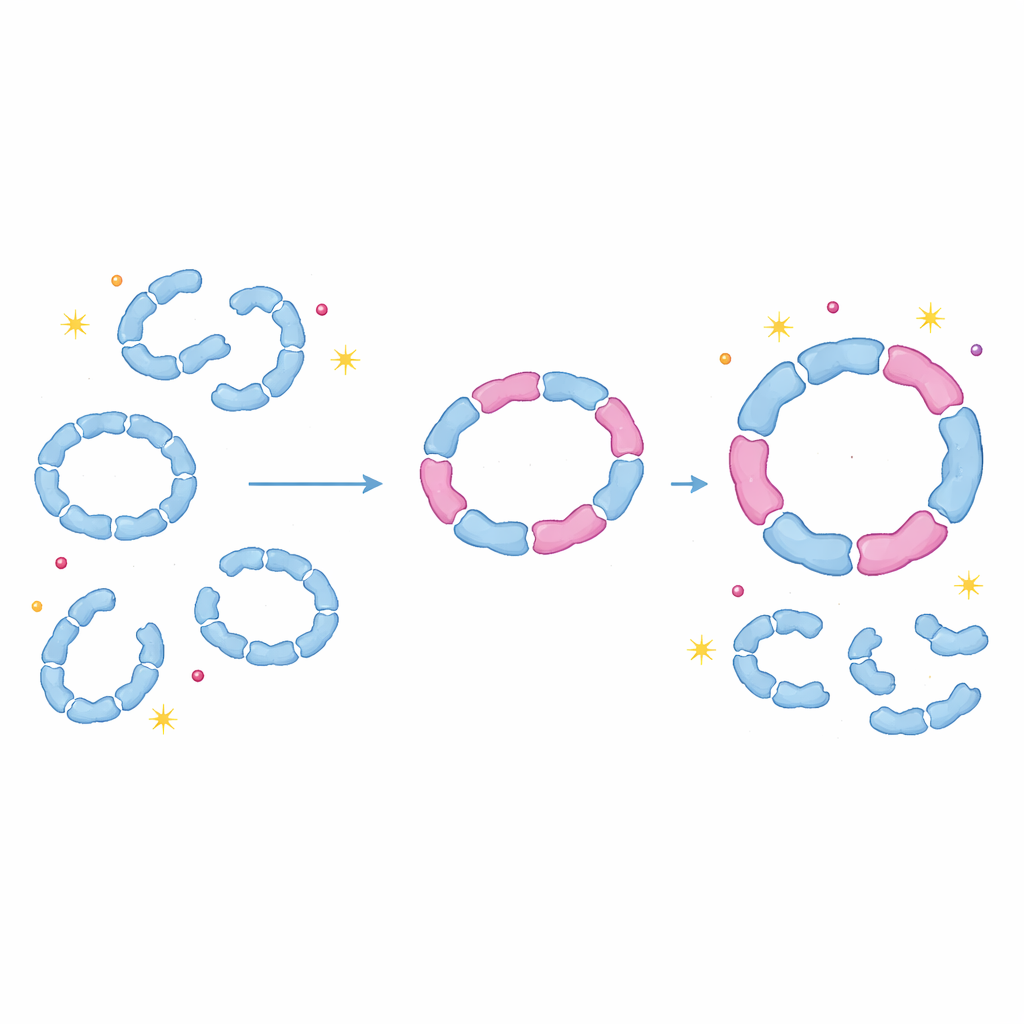
Proteínas como amortecedores ajustáveis
Ao mostrar que peroxiredoxinas rotineiramente constroem anéis e dímeros mistos, este trabalho desafia a suposição de longa data de que cada isoforma funciona apenas como um complexo puro. Em vez disso, as células parecem usar a hetero‑oligomerização como um meio flexível de ajustar quão estáveis esses anéis são, quão sensíveis ao dano e quando mudam entre funções de desintoxicação e de chaperona. Uma pequena alteração na expressão de uma isoforma, por exemplo durante estresse oxidativo, pode repercutir em todo o sistema ao remodelar muitos complexos mistos ao mesmo tempo. Para não especialistas, a mensagem-chave é que complexos proteicos se comportam menos como modelos rígidos de Lego e mais como amortecedores ajustáveis: ao trocar peças diferentes, porém compatíveis, as células podem sutilmente calibrar sua proteção contra o estresse oxidativo, com implicações para envelhecimento, câncer, infecções e outras condições em que o equilíbrio redox se altera.
Citação: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Palavras-chave: peroxiredoxina, estresse oxidativo, complexos proteicos, sinalização redox, adaptação celular