Clear Sky Science · es
La hetero-oligomerización impulsa la plasticidad estructural de las peroxiredoxinas eucariotas
Proteínas que se remodelan para proteger nuestras células
Dentro de cada célula se libra una batalla silenciosa contra moléculas reactivas de oxígeno que pueden dañar el ADN, las proteínas y los lípidos. Una familia de enzimas llamadas peroxiredoxinas actúa como defensa de primera línea, detoxificando estas especies reactivas y ayudando a las células a detectar cambios en los niveles de oxidación. Durante años, los científicos pensaron que cada peroxiredoxina trabajaba de forma aislada en ensamblajes uniformes formados por bloques idénticos. Este estudio pone esa visión patas arriba al mostrar que muchas peroxiredoxinas en realidad se mezclan con parientes estrechamente relacionados, formando ensamblajes híbridos que cambian de forma y estabilidad de modos que podrían afinar la manera en que las células afrontan el estrés.
Por qué importa el trabajo en equipo de las proteínas
Las peroxiredoxinas están entre las proteínas más abundantes en organismos que van desde la levadura hasta humanos y plantas. Eliminan peróxido de hidrógeno, un subproducto reactivo del metabolismo, y actúan además como chaperonas moleculares que ayudan a otras proteínas a mantener su conformación. La imagen clásica de los libros de texto muestra estas enzimas ensamblándose en pares (dímeros) o en anillos en forma de rosquilla de diez unidades (decámeros), pero siempre construidos a partir de una única isoforma. Sin embargo, muchas células contienen dos versiones casi idénticas de la misma peroxiredoxina en el mismo compartimento. Los autores plantearon una pregunta simple pero fundamental: ¿permanecen realmente separadas estas isoformas, o se ensamblan en complejos mixtos con propiedades nuevas?
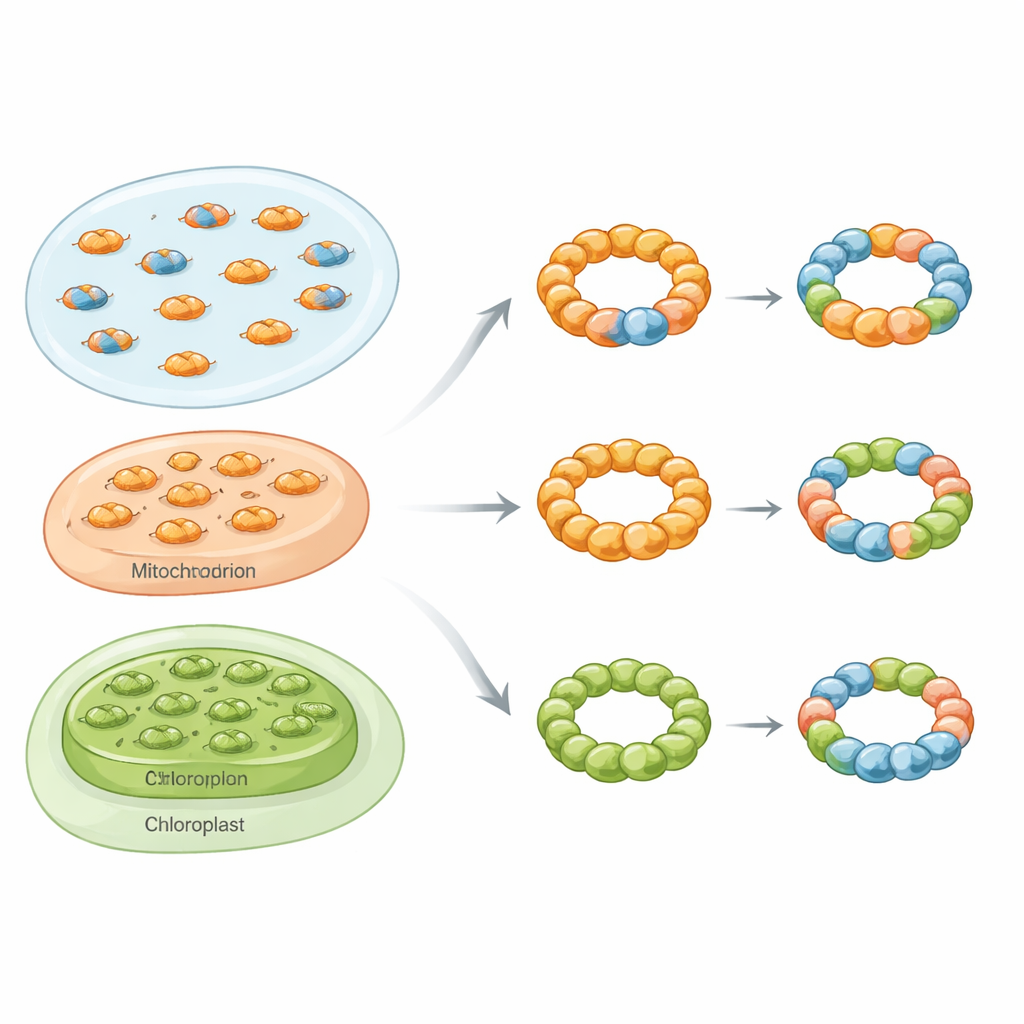
Anillos mixtos a través de los reinos de la vida
Empleando un conjunto de herramientas que incluyó purificación bioquímica, fotometría de masa nativa, microscopía electrónica y ensayos de fluorescencia en células vivas, los investigadores muestran que los complejos mixtos, u hetero-oligoméricos, de peroxiredoxinas no son rarezas. En la levadura de pan se centraron en dos isoformas citosólicas llamadas Tsa1 y Tsa2. Cuando ambas proteínas se produjeron juntas en bacterias, formaron tanto dímeros mixtos como decámeros mixtos con un espectro de proporciones de subunidades. Bajo el microscopio electrónico estos ensamblajes aparecían como partículas características en forma de anillo, confirmando que Tsa1 y Tsa2 pueden compartir el mismo andamiaje estructural en lugar de formar solo anillos separados.
Reconfiguración desencadenada por el estrés en células de levadura
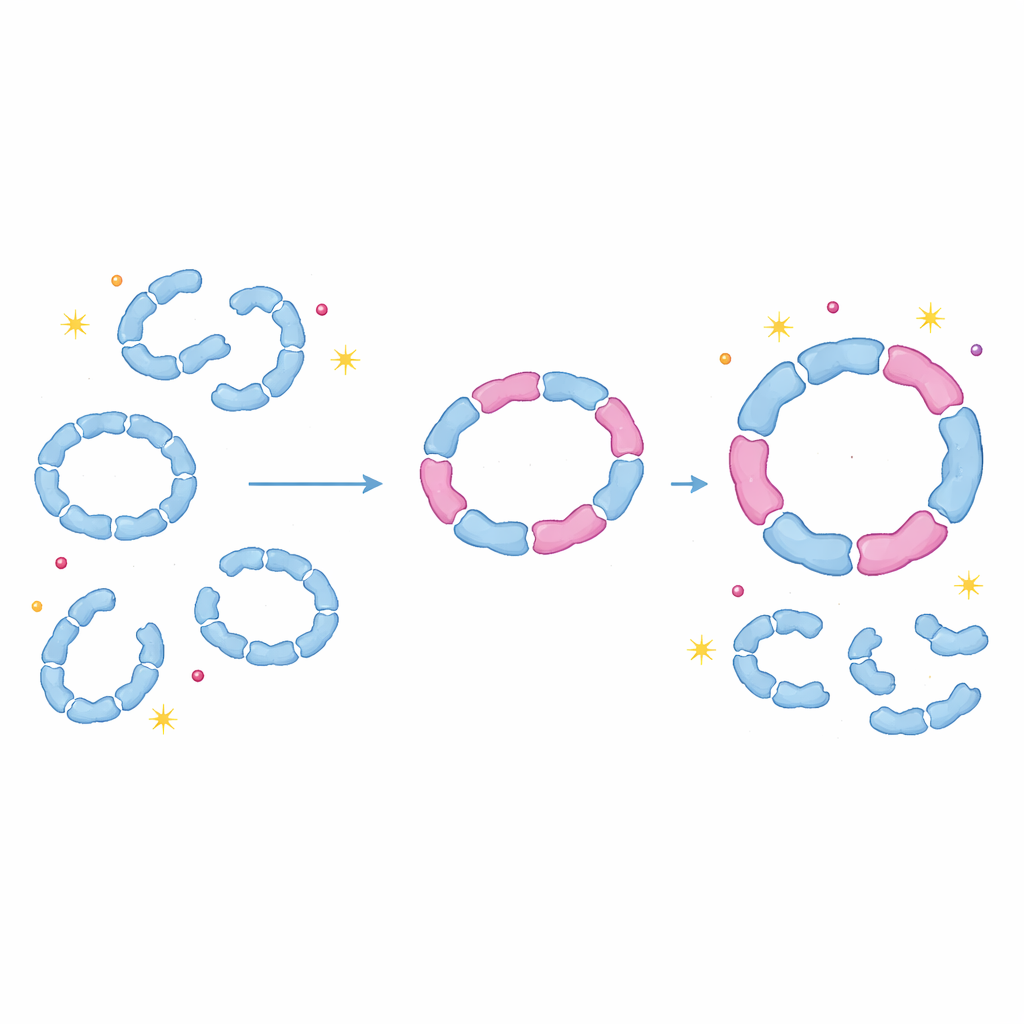
Para comprobar si esta mezcla importa dentro de células vivas, el equipo marcó Tsa1 y Tsa2 con un sensor fluorescente y siguió su comportamiento en levadura. Bajo condiciones normales de crecimiento, Tsa1 es abundante mientras que Tsa2 es escasa, y Tsa1 se encuentra mayoritariamente en formas más pequeñas. Cuando las células se expusieron a peróxido de hidrógeno, la producción de Tsa2 aumentó drásticamente y en geles nativos aparecieron bandas claras que correspondían a ensamblajes grandes en forma de anillo. Curiosamente, incluso la incorporación de solo una o dos subunidades Tsa2 en un anillo de Tsa1 fue suficiente para estabilizar la estructura de diez unidades frente a la desintegración al calentarse. Las cinéticas enzimáticas mostraron que estos anillos híbridos seguían siendo totalmente activos, con velocidades de reacción similares a las de las formas puras pero con menor tendencia a sobre-oxidarse y desactivarse.
Una estrategia generalizada para ajustar la función proteica
La historia no se detuvo en la levadura. En células humanas renales, los autores separaron dos peroxiredoxinas estrechamente relacionadas, PRDX1 y PRDX2, mediante cromatografía de intercambio iónico. En células carentes de una isoforma, cada proteína restante eluía como una especie distinta. Sin embargo, en células normales ambas isoformas coeluyeron en un rango compartido, coherente con la presencia de complejos mixtos. Pruebas similares en levaduras diseñadas para producir peroxiredoxinas humanas, vegetales y de parásitos mostraron que parejas de todas estas especies podían formar híbridos funcionales. En enzimas de cloroplasto vegetal y en un parásito que causa leishmaniasis, introducir una isoforma más proclive al decámero pudo arrastrar a una pareja más dímerica hacia anillos más grandes, o, a la inversa, desestabilizar anillos dependiendo de qué subunidad dominara. Análisis bioinformáticos de más de 1.500 genomas eucariotas revelaron que más del 80% de las especies probablemente albergan múltiples peroxiredoxinas tipo Prx1 en el mismo compartimento, lo que sugiere que tal mezcla es la norma más que la excepción.
Proteínas como amortiguadores ajustables
Al mostrar que las peroxiredoxinas construyen rutinariamente anillos y dímeros mixtos, este trabajo desafía la suposición de larga data de que cada isoforma funciona solo como un ensamblaje puro. En cambio, las células parecen usar la hetero-oligomerización como una forma flexible de ajustar cuán estables son estos anillos, cuán sensibles son al daño y cuándo cambian entre funciones de desintoxicación y de chaperona. Un pequeño cambio en la expresión de una isoforma, por ejemplo durante el estrés oxidativo, puede propagarse por el sistema al remodelar muchos complejos mixtos a la vez. Para el público general, el mensaje clave es que los complejos proteicos se comportan menos como modelos rígidos de Lego y más como amortiguadores ajustables: al intercambiar piezas diferentes pero compatibles, las células pueden sutilmente afinar su protección frente al estrés oxidativo, con implicaciones para el envejecimiento, el cáncer, las infecciones y otras condiciones donde el equilibrio redox se altera.
Cita: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Palabras clave: peroxiredoxina, estrés oxidativo, complejos proteicos, señalización redox, adaptación celular