Clear Sky Science · tr
Eukaryotik peroksiredoksinlerin yapısal plastisitesini hetero-oligomerizasyon yönlendiriyor
Hücrelerimizi korumak için kendini yeniden şekillendiren proteinler
Her hücrenin içinde DNA, proteinler ve yağlara zarar verebilen reaktif oksijen moleküllerine karşı sessiz bir mücadele sürer. Peroksiredoksinler adı verilen bir enzim ailesi, bu reaktif türleri detoksifiye ederek ilk savunma hattını oluşturur ve hücrelerin oksidasyon düzeylerindeki değişimleri algılamasına yardımcı olur. Yıllarca bilim insanları her peroksiredoksinin tek tip, özdeş yapı taşlarından oluşan kümeler halinde çalıştığını düşündü. Bu çalışma bu görüşü tersine çeviriyor: birçok peroksiredoksinin gerçekte yakından ilişkili kardeşleriyle karışıp yeni özellikler taşıyan hibrit yapılar oluşturduğunu ve bunların şekil ile kararlılığı hücrelerin strese uyumunu ince ayarlayabileceğini gösteriyor.
Protein işbirliğinin önemi
Peroksiredoksinler maya, insan ve bitkiler gibi organizmalarda en bol bulunan proteinler arasında yer alır. Metabolizmanın reaktif bir yan ürünü olan hidrojen peroksidi uzaklaştırır ve ayrıca diğer proteinlerin yapısını korumasına yardımcı olan moleküler şaperonlar olarak görev yapar. Klasik ders kitabı resminde bu enzimlerin ya çiftler (dimerler) ya da on birimin oluşturduğu halka şeklinde halkalar (dekamerler) şeklinde bir araya geldiği, ancak her zaman tek bir izoformdan inşa edildiği gösterilir. Oysa birçok hücre aynı bölmede iki neredeyse ikiz peroksiredoksin versiyonunu taşır. Yazarlar basit ama temel bir soru sordular: bu izoformlar gerçekten ayrı mı kalıyor, yoksa yeni özellikler kazanan karışık kompleksler mi oluşturuyorlar?
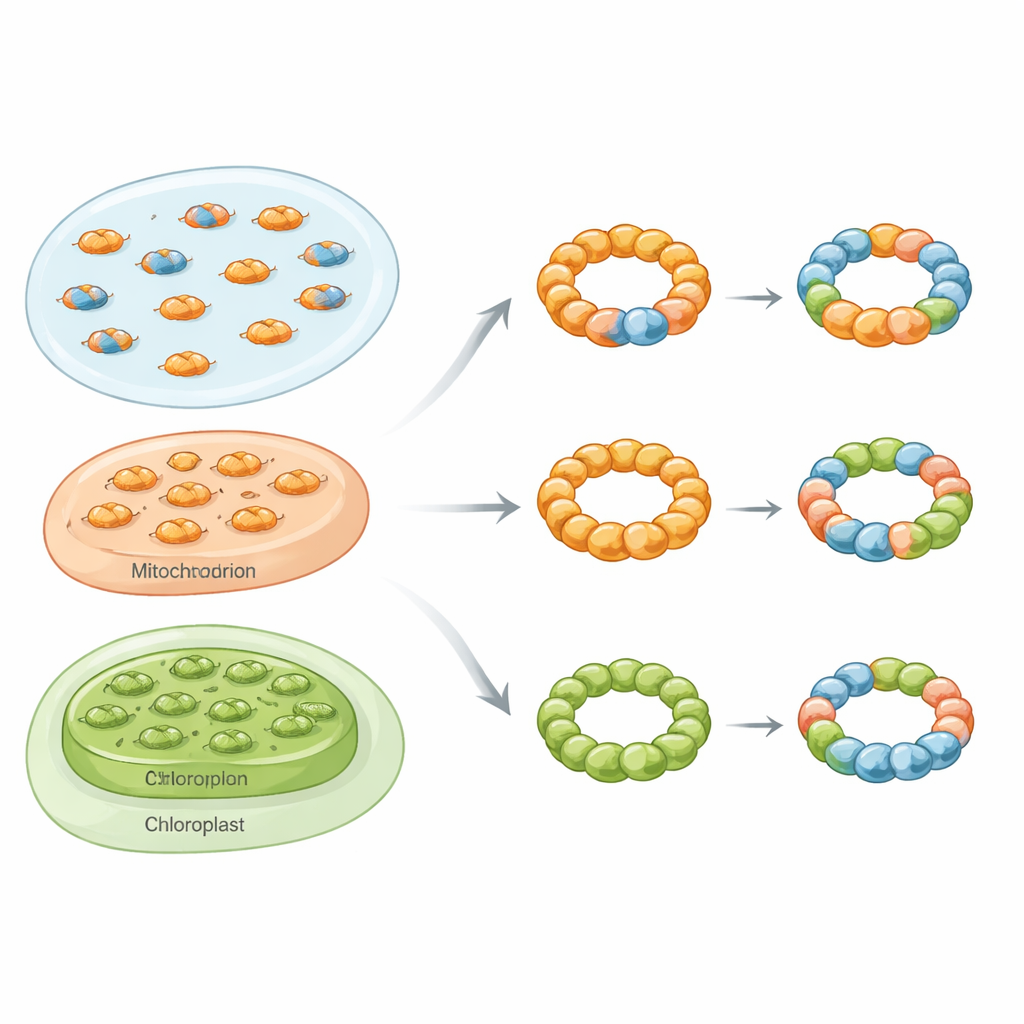
Yaşam krallıkları boyunca karışık halkalar
Biyokimyasal saflaştırma, natif kütle fotometresi, elektron mikroskobu ve canlı hücre floresans testlerini içeren bir araç seti kullanarak, araştırmacılar karışık ya da hetero-oligomerik peroksiredoksin komplekslerinin nadir meraklar olmadığını gösteriyor. Fırın mayasında çalışma, sitozolde bulunan Tsa1 ve Tsa2 adlı iki izoforma odaklandı. İki protein bakteride birlikte üretildiğinde hem karışık dimerler hem de altbirim oranları çeşitliliği gösteren karışık dekamerler oluşturdu. Elektron mikroskobunda bu yapılar karakteristik halka biçimli parçacıklar olarak görüldü ve Tsa1 ile Tsa2’nin yalnızca ayrı halkalar oluşturmak yerine aynı yapısal iskelesi paylaşabildiğini doğruladı.
Maya hücrelerinde strese bağlı yeniden şekillenme
Bu karışımın canlı hücrelerde önem taşıyıp taşımadığını test etmek için ekip Tsa1 ve Tsa2’yi bir floresan sensörle işaretledi ve mayadaki davranışlarını izledi. Normal büyüme koşullarında Tsa1 bolken Tsa2 kıttı ve Tsa1 çoğunlukla daha küçük formlarda bulunuyordu. Hücreler hidrojen perokside maruz kalınca Tsa2 üretimi hızla arttı ve natif jel üstünde daha büyük halka biçimli yapılara karşılık gelen belirgin bantlar ortaya çıktı. İlginç şekilde, bir Tsa1 halkasına sadece bir ya da iki Tsa2 altbiriminin katılması bile on birimli yapıyı ısı etkisiyle parçalanmaya karşı stabilize etmeye yetiyordu. Enzim kinetiği, bu hibrit halkaların reaksiyon hızlarının saf formlarla benzer olduğunu ancak aşırı oksitlenip inaktive olma eğilimlerinin azaldığını gösterdi.
Protein işlevini ayarlamak için yaygın bir strateji
Hikâye mayayla sınırlı kalmadı. İnsan böbrek hücrelerinde yazarlar iyon-değişim kromatografisi ile PRDX1 ve PRDX2 adlı iki yakın peroksiredoksini ayırdı. Bir izoform eksik olan hücrelerde geride kalan protein her seferinde ayrı bir tür olarak elüe oldu. Ancak normal hücrelerde her iki izoform ortak bir aralıkta birlikte elüe oldu; bu durum karışık komplekslerin varlığıyla uyumluydu. İnsan, bitki ve parazit peroksiredoksinleri üretecek şekilde mühendislik yapılan mayada benzer testler, tüm bu organizmalardan çiftlerin fonksiyonel hibritler oluşturabildiğini gösterdi. Bitki kloroplast enzimlerinde ve Leishmania’ya neden olan bir parazitte, daha “dekamer-sever” bir izoformun tanıtılması daha dimerik bir partneri daha büyük halkalara çekebilir ya da hangi altbirimin baskın olduğuna bağlı olarak halkaları tersine kararsızlaştırabilirdi. 1.500’den fazla ökaryotik genomun biyoinformatik analizi, türlerin %80’inden fazlasının muhtemelen aynı bölmede birden fazla Prx1-tipi peroksiredoksin barındırdığını ortaya koydu; bu da böyle bir karışımın istisna değil kural olduğunu düşündürüyor.
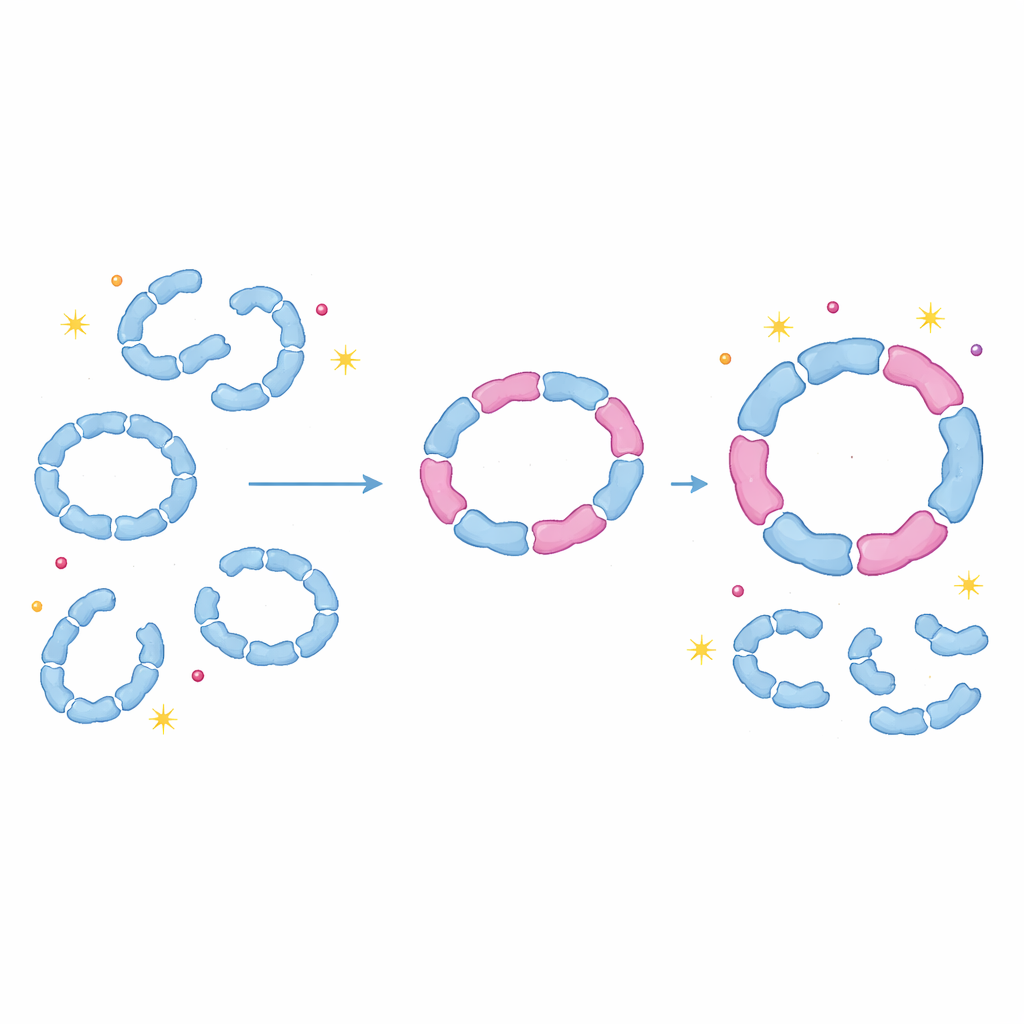
Ayarlanabilir darbe emici olarak proteinler
Peroksiredoksinlerin rutin olarak karışık halkalar ve dimerler inşa ettiğini göstererek, bu çalışma her izoformun yalnızca saf bir yapı olarak işlev gördüğü uzun süreli varsayımı sorguluyor. Bunun yerine hücreler, bu halkaların ne kadar kararlı olduğu, hasara ne kadar duyarlı olduğu ve detoksifikasyon ile şaperon rolleri arasında ne zaman geçiş yapacakları konusunda ayar yapmanın esnek bir yolu olarak hetero-oligomerizasyonu kullanıyor gibi görünüyor. Bir izoformun ifadesindeki küçük bir değişiklik —örneğin oksidatif stres sırasında— sistemde birden çok karışık kompleksi aynı anda yeniden şekillendirerek etkisini gösterebilir. Uzman olmayanlar için ana mesaj şudur: protein kompleksleri katı Lego modelleri gibi değil, ayarlanabilir darbe emicileri andırır; farklı ama uyumlu parçalar takarak hücreler oksidatif strese karşı korumalarını ince biçimde ayarlayabilir ve bu durum yaşlanma, kanser, enfeksiyon ve redoks dengesinin bozulduğu diğer durumlar açısından önemli sonuçlar doğurabilir.
Atıf: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Anahtar kelimeler: peroksiredoksin, oksidatif stres, protein kompleksleri, redoks sinyalleşmesi, hücresel uyum