Clear Sky Science · sv
Hetero-oligomerisering driver strukturell plasticitet hos eukaryota peroxiredoxiner
Proteiner som omformar sig för att skydda våra celler
Inuti varje cell pågår en tyst kamp mot reaktiva syreföreningar som kan skada DNA, proteiner och lipider. En familj enzymer kallade peroxiredoxiner fungerar som en frontlinjedefenskapare, avgiftar dessa reaktiva arter och hjälper celler att känna av när oxidationsnivåerna förändras. I åratal trodde forskare att varje peroxiredoxin arbetade ensam i enhetliga kluster byggda av identiska byggstenar. Denna studie kullkastar den bilden genom att visa att många peroxiredoxiner faktiskt blandar sig med nära släktingar och bildar hybridassembléer som ändrar form och stabilitet på sätt som kan finjustera hur celler hanterar stress.
Varför proteinlagarbete spelar roll
Peroxiredoxiner hör till de mest rikliga proteinerna i organismer från jäst till människor och växter. De avlägsnar väteperoxid, en reaktiv biprodukt av ämnesomsättningen, och fungerar också som molekylära chaperoner som hjälper andra proteiner att behålla sin struktur. Den klassiska bilden i läroböcker visar att dessa enzymer monterar sig i par (dimerer) eller donutformade ringar av tio enheter (dekamerer), men alltid byggda av en isoform åt gången. Ändå bär många celler två nästan tvillinglika versioner av samma peroxiredoxin i samma cellkompartment. Författarna ställde en enkel men grundläggande fråga: håller dessa isoformer verkligen isär, eller monterar de sig i blandade komplex med nya egenskaper?
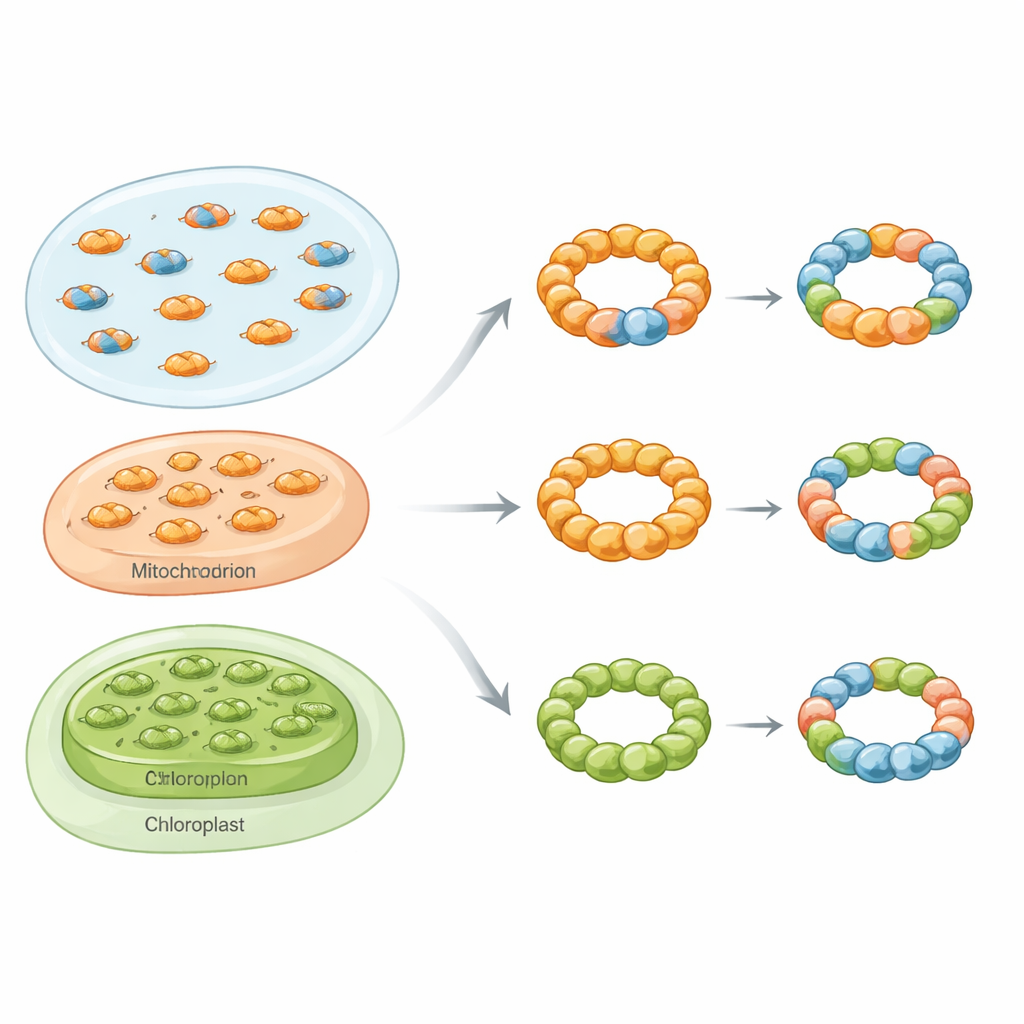
Blandade ringar över livets domäner
Med en verktygslåda som innehöll biokemisk rening, natívt massfotometri, elektronmikroskopi och fluorescensmätningar i levande celler visar forskarna att blandade, eller hetero‑oligomeriska, peroxiredoxinkomplex inte är sällsynta kuriositeter. I bakjäst fokuserade de på två cytosoliska isoformer kallade Tsa1 och Tsa2. När de två proteinerna producerades tillsammans i bakterier bildade de både blandade dimerer och blandade dekamerer med ett spektrum av subenhetskvoter. Under elektronmikroskopet framträdde dessa assembléer som karakteristiska ringformade partiklar, vilket bekräftar att Tsa1 och Tsa2 kan dela samma strukturella stomme istället för att endast bilda separata ringar.
Stressutlöst omformning i jästceller
För att testa om denna blandning betyder något i levande celler märkte teamet Tsa1 och Tsa2 med en fluorescerande sensor och följde deras beteende i jäst. Under normala tillväxtförhållanden är Tsa1 rikligt förekommande medan Tsa2 är sällsynt, och Tsa1 finns till största delen i mindre former. När cellerna exponerades för väteperoxid ökade produktionen av Tsa2 kraftigt, och tydliga band motsvarande större ringformade assembléer framträdde på natíva geler. Intressant nog var redan införandet av en eller två Tsa2‑enheter i en Tsa1‑ring nog för att stabilisera den tiodelade strukturen mot att falla isär vid uppvärmning. Enzymkinetiska mätningar visade att dessa hybrida ringar förblev fullt aktiva, med reaktionshastigheter liknande de rena formerna men med minskad benägenhet att bli överoxiderade och inaktiverade.
En utbredd strategi för att finjustera proteinfunktion
Berättelsen slutade inte med jäst. I humana njurceller separerade författarna två närbesläktade peroxiredoxiner, PRDX1 och PRDX2, med jonbyteskromatografi. I celler som saknade en isoform eluerade varje kvarvarande protein som en distinkt art. I normala celler eluerade dock båda isoformerna över ett gemensamt intervall, i linje med närvaron av blandade komplex. Liknande tester i jäst som modifierats för att producera mänskliga, växt- och parasitperoxiredoxiner visade att par från alla dessa organismer kunde bilda funktionella hybrider. I växtkloroplastenzymer och i en parasit som orsakar leishmaniasis kunde införandet av en mer “dekamer‑gynnande” isoform dra en mer dimerisk partner in i större ringar, eller tvärtom destabilisera ringar beroende på vilken subenhet som dominerade. Bioinformatiska analyser av mer än 1 500 eukaryota genom visade att över 80 % av arterna sannolikt har flera Prx1‑typperoxiredoxiner i samma kompartment, vilket tyder på att sådan blandning är regeln snarare än undantaget.
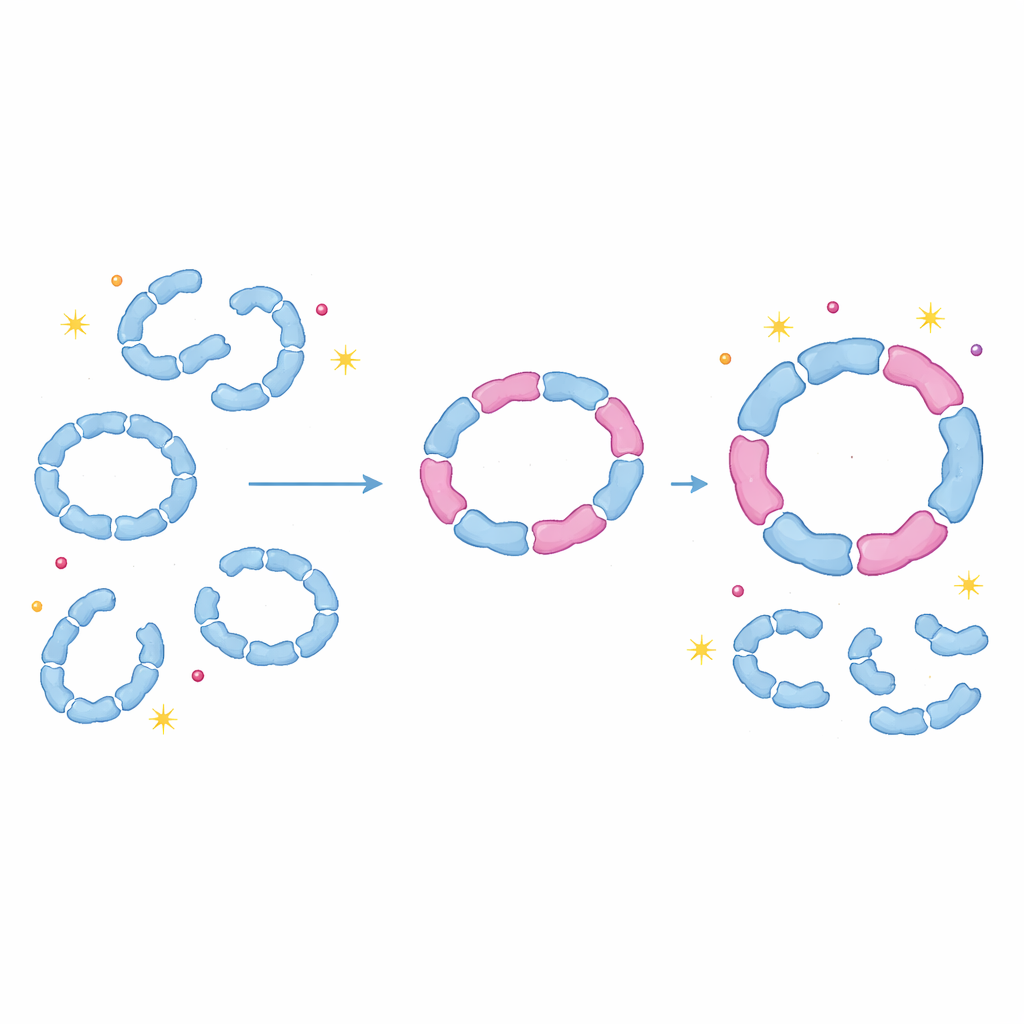
Proteiner som justerbara stötdämpare
Genom att visa att peroxiredoxiner rutinmässigt bygger blandade ringar och dimerer utmanar detta arbete den länge rådande antagandet att varje isoform fungerar endast som en ren assemblé. Istället verkar celler använda hetero‑oligomerisering som ett flexibelt sätt att reglera hur stabila dessa ringar är, hur känsliga de är för skador och när de växlar mellan avgiftande och chaperonroller. En liten förändring i uttrycket av en isoform, till exempel under oxidativ stress, kan ge ringar på vattnet genom systemet genom att omforma många blandade komplex samtidigt. För icke‑specialister är huvudbudskapet att proteinkomplex beter sig mindre som styva Lego‑modeller och mer som justerbara stötdämpare: genom att byta in olika men kompatibla delar kan celler subtilt stämma sin skyddsförmåga mot oxidativ stress, med konsekvenser för åldrande, cancer, infektion och andra tillstånd där redoxbalansen rubbas.
Citering: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Nyckelord: peroxiredoxin, oxidativ stress, proteinkomplex, redoxsignalering, cellanpassning