Clear Sky Science · pl
Hetero-oligomeryzacja napędza plastyczność strukturalną eukariotycznych peroksyredoksyn
Białka, które przekształcają się, by chronić nasze komórki
W każdej komórce toczy się cicha walka z reaktywnymi cząsteczkami tlenu, które mogą uszkadzać DNA, białka i lipidy. Rodzina enzymów zwanych peroksyredoksynami pełni rolę pierwszej linii obrony: oczyszczają te reaktywne związki i pomagają komórkom wyczuwać zmiany poziomu utlenienia. Przez lata naukowcy przypuszczali, że każda peroksyredoksyna działała samotnie w jednorodnych skupieniach zbudowanych z identycznych elementów. To badanie obala ten pogląd, pokazując, że wiele peroksyredoksyn miesza się z blisko spokrewnionymi wariantami, tworząc hybrydowe zespoły, które zmieniają kształt i stabilność w sposób mogący precyzyjnie regulować reakcję komórek na stres.
Dlaczego współpraca białek ma znaczenie
Peroksyredoksyny należą do najobficiej występujących białek u organizmów od drożdży po ludzi i rośliny. Usuwają nadtlenek wodoru, reaktywny produkt uboczny metabolizmu, i pełnią rolę molekularnych czaperonów, pomagając innym białkom zachować prawidłową strukturę. Klasyczny obraz z podręczników pokazuje te enzymy składające się albo w pary (dimery), albo w pierścienie przypominające pączki z dziesięciu jednostek (dekamery), zawsze jednak zbudowane z jednej izoformy. Tymczasem w wielu komórkach obecne są dwie niemal bliźniacze wersje tej samej peroksyredoksyny w tym samym przedziale komórkowym. Autorzy postawili proste, ale zasadnicze pytanie: czy te izoformy naprawdę pozostają oddzielne, czy też tworzą mieszane kompleksy o nowych właściwościach?
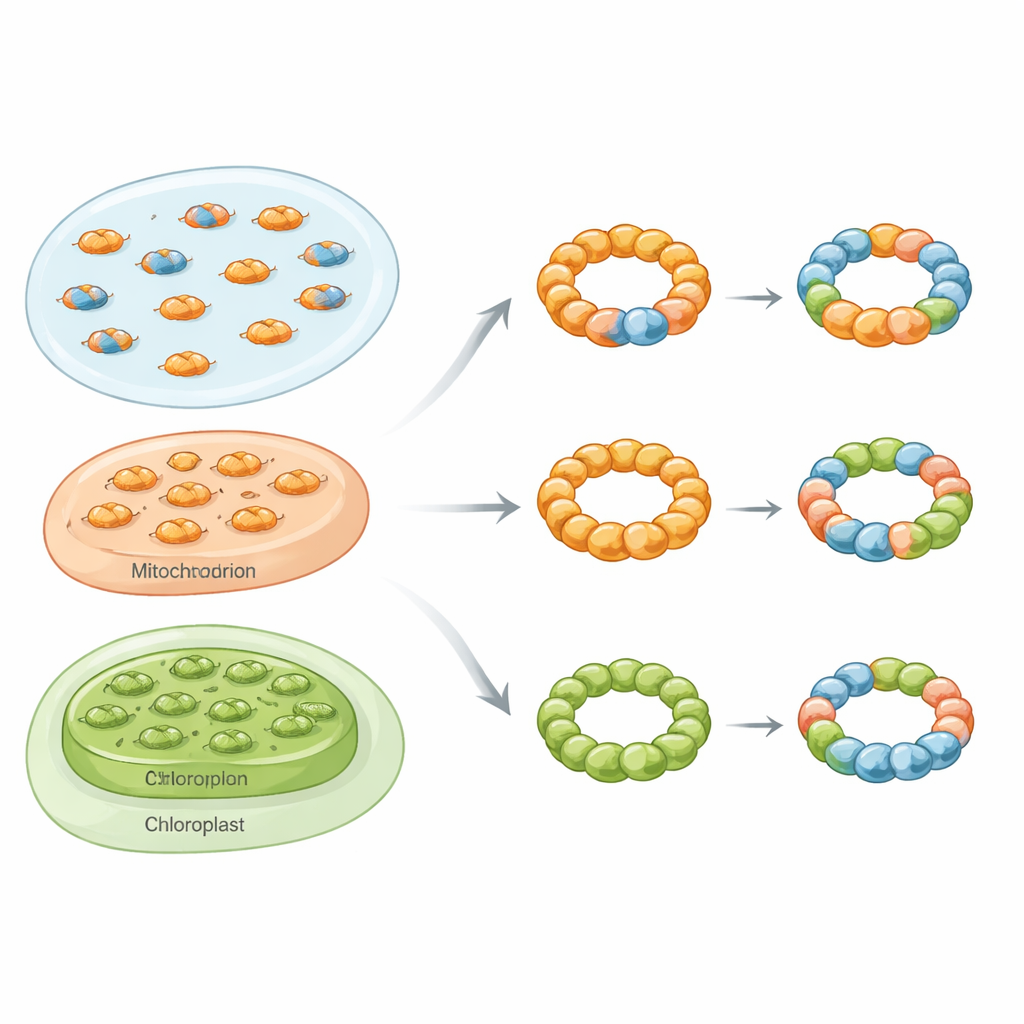
Mieszane pierścienie w różnych królestwach życia
Wykorzystując zestaw technik obejmujący oczyszczanie biochemiczne, natywną fotometrię mas, mikroskopię elektronową i testy fluorescencyjne w żywych komórkach, badacze pokazali, że mieszane, czyli hetero‑oligomeryczne kompleksy peroksyredoksyn nie są rzadkimi ciekawostkami. W drożdżach piekarskich skupili się na dwóch izoformach cytosolowych zwanych Tsa1 i Tsa2. Gdy oba białka były współwytwarzane w bakteriach, tworzyły zarówno mieszane dimery, jak i mieszane dekamery o zróżnicowanym stosunku podjednostek. W mikroskopie elektronowym te struktury przypominały charakterystyczne pierścieniowe cząstki, co potwierdza, że Tsa1 i Tsa2 mogą dzielić ten sam szkielet strukturalny zamiast tworzyć wyłącznie oddzielne pierścienie.
Przegrupowanie wywołane stresem w komórkach drożdży
Aby sprawdzić, czy to mieszanie ma znaczenie w żywych komórkach, zespół znakował Tsa1 i Tsa2 czujnikiem fluorescencyjnym i obserwował ich zachowanie w drożdżach. W normalnych warunkach wzrostu Tsa1 jest obfity, podczas gdy Tsa2 występuje w niewielkich ilościach, a Tsa1 występuje głównie w mniejszych formach. Po wystawieniu komórek na działanie nadtlenku wodoru produkcja Tsa2 gwałtownie wzrosła, a w żelach native pojawiły się wyraźne pasma odpowiadające większym pierścieniowym zespołom. Co ciekawe, nawet włączenie zaledwie jednego lub dwóch podjednostek Tsa2 do pierścienia Tsa1 wystarczało, by ustabilizować strukturę dziesięciounitową przed rozpadem podczas ogrzewania. Kinetyka enzymatyczna wykazała, że te hybrydowe pierścienie pozostawały w pełni aktywne, z szybkościami reakcji podobnymi do form czystych, ale o mniejszej skłonności do nadutlenienia i inaktywacji.
Rozpowszechniona strategia strojenia funkcji białek
Historia nie skończyła się na drożdżach. W ludzkich komórkach nerkowych autorzy rozdzielili dwie blisko spokrewnione peroksyredoksyny, PRDX1 i PRDX2, za pomocą chromatografii jonowymiennej. W komórkach pozbawionych jednej izoformy każda pozostała forma eluotowała jako odrębny gatunek. W komórkach normalnych jednak obie izoformy współeluotowały w wspólnym zakresie, co jest zgodne z obecnością mieszanych kompleksów. Podobne testy w drożdżach zmodyfikowanych do produkcji peroksyredoksyn ludzkich, roślinnych i pasożytniczych wykazały, że pary z wszystkich tych organizmów mogą tworzyć funkcjonalne hybrydy. W enzymach chloroplastów roślinnych i u pasożyta powodującego leiszmaniozę wprowadzenie izoformy bardziej „lubiącej dekamery” mogło przeciągnąć partnera mającego skłonność do dimerów do większych pierścieni, albo odwrotnie — destabilizować pierścienie w zależności od tego, która podjednostka dominowała. Analizy bioinformatyczne ponad 1 500 genomów eukariotycznych wykazały, że w ponad 80% gatunków prawdopodobnie występuje wiele peroksyredoksyn typu Prx1 w tym samym przedziale komórkowym, co sugeruje, że takie mieszanie jest regułą, a nie wyjątkiem.
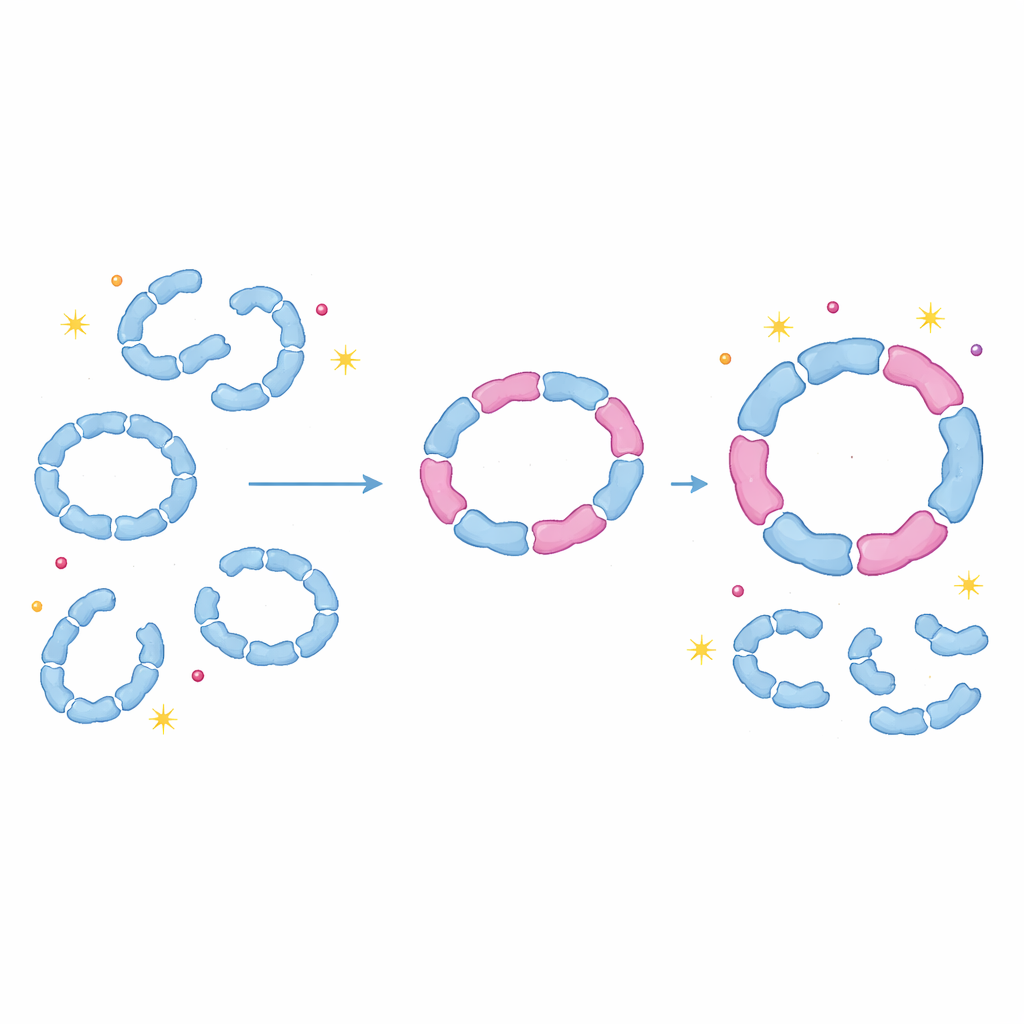
Białka jako regulowane amortyzatory uderzeń
Pokazując, że peroksyredoksyny rutynowo budują mieszane pierścienie i dimery, praca ta kwestionuje długotrwałe założenie, że każda izoforma funkcjonuje wyłącznie jako czyste zespoły. Zamiast tego komórki najwyraźniej wykorzystują hetero‑oligomeryzację jako elastyczny sposób regulacji stabilności tych pierścieni, ich wrażliwości na uszkodzenia oraz momentu przełączania między rolami detoksykacyjnymi i czaperonowymi. Niewielka zmiana ekspresji jednej izoformy, na przykład w trakcie stresu oksydacyjnego, może rozlać się po systemie, przebudowując wiele mieszanych kompleksów naraz. Dla osób niebędących specjalistami kluczowy wniosek jest taki, że kompleksy białkowe zachowują się mniej jak sztywne modele Lego, a bardziej jak regulowane amortyzatory: poprzez wymianę różnych, ale kompatybilnych części komórki mogą subtelnie dostrajać ochronę przed stresem oksydacyjnym, co ma znaczenie dla starzenia, raka, zakażeń i innych stanów związanych z zaburzeniem równowagi redoks.
Cytowanie: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Słowa kluczowe: peroksyredoksyna, stres oksydacyjny, kompleksy białkowe, sygnalizacja redoks, adaptacja komórkowa