Clear Sky Science · nl
Hetero-oligomerisatie stuurt structurele plasticiteit van eukaryote peroxiredoxines
Proteïnen die zichzelf hervormen om onze cellen te beschermen
In elke cel woedt een stille strijd tegen reactieve zuurstofmoleculen die DNA, eiwitten en vetten kunnen beschadigen. Een familie enzymen, peroxiredoxines genoemd, vormt de frontlinie van die verdediging: ze detoxificeren deze reactieve stoffen en helpen cellen te detecteren wanneer het oxidatieniveau verandert. Jarenlang dachten wetenschappers dat elk peroxiredoxine zelfstandig werkte in uniforme clusters van identieke bouwstenen. Deze studie keert dat beeld om door te laten zien dat veel peroxiredoxines feitelijk mengen met nauwe verwanten en hybride assemblages vormen die van vorm en stabiliteit veranderen op manieren die de stressrespons van cellen kunnen bijsturen.
Waarom teamwork tussen eiwitten ertoe doet
Peroxiredoxines behoren tot de meest voorkomende eiwitten in organismen van gist tot mensen en planten. Ze verwijderen waterstofperoxide, een reactief bijproduct van de stofwisseling, en fungeren ook als moleculaire chaperonnes die andere eiwitten helpen hun vorm te behouden. De klassieke leerboekvoorstelling toont deze enzymen als paren (dimeren) of als donutvormige ringen van tien eenheden (dekameer), maar altijd opgebouwd uit één isoform tegelijk. Toch dragen veel cellen twee bijna identieke versies van hetzelfde peroxiredoxine in hetzelfde compartiment. De auteurs stelden een simpele maar fundamentele vraag: blijven deze isoformen echt gescheiden, of assembleren ze zich tot gemengde complexen met nieuwe eigenschappen?
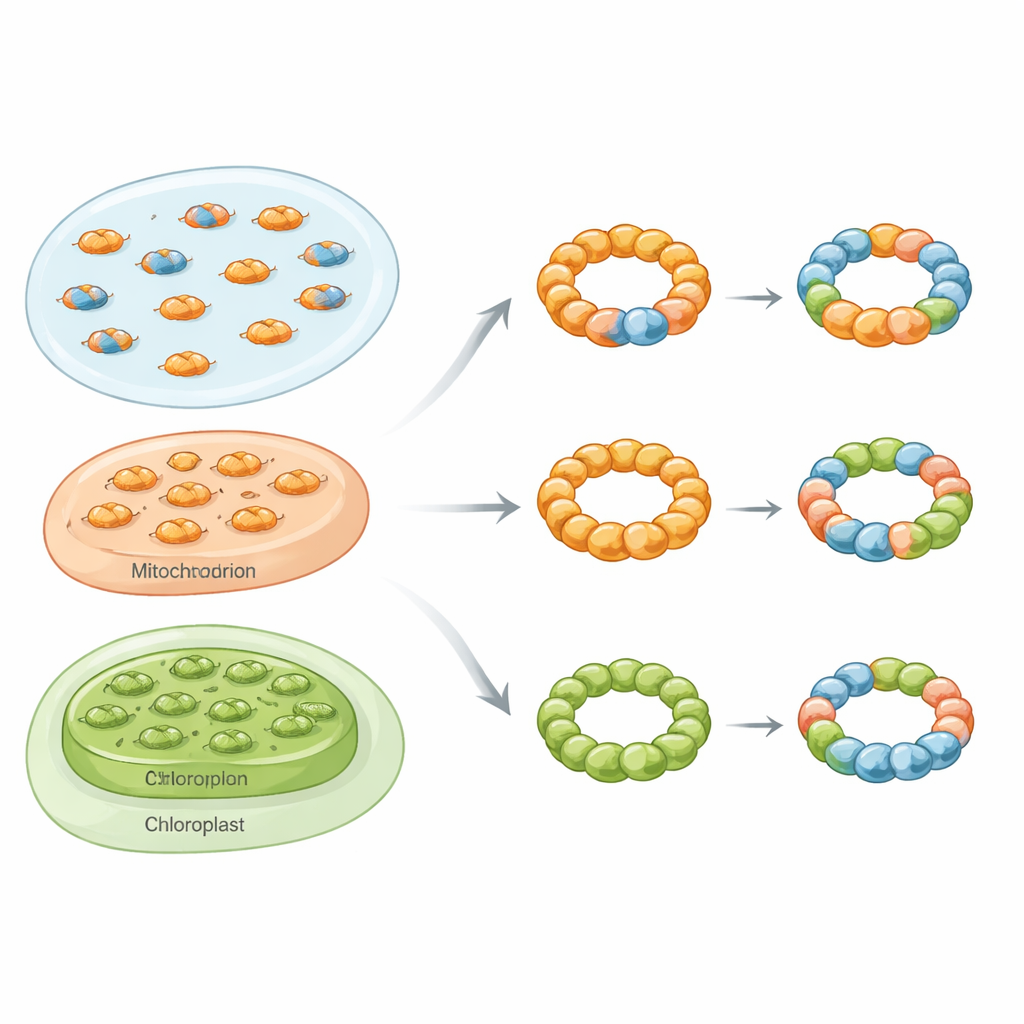
Gemengde ringen door vorstendommen van het leven heen
Met een gereedschapskist die biochemische zuivering, native massaphotometrie, elektronenmicroscopie en live-cel fluorescentie-assays omvatte, tonen de onderzoekers aan dat gemengde, oftewel hetero-oligomere, peroxiredoxinecomplexen geen zeldzame curiositeiten zijn. Bij bakergist richtten ze zich op twee cytosolische isoformen, Tsa1 en Tsa2. Wanneer de twee eiwitten samen in bacteriën werden geproduceerd, vormden ze zowel gemengde dimeren als gemengde dekameerstructuren met een spectrum aan subeenheidsverhoudingen. Onder de elektronenmicroscoop leken deze assemblages op karakteristieke ringvormige deeltjes, wat bevestigt dat Tsa1 en Tsa2 hetzelfde structurele geraamte kunnen delen in plaats van uitsluitend aparte ringen te vormen.
Stress‑geïnduceerde hervorming in gistcellen
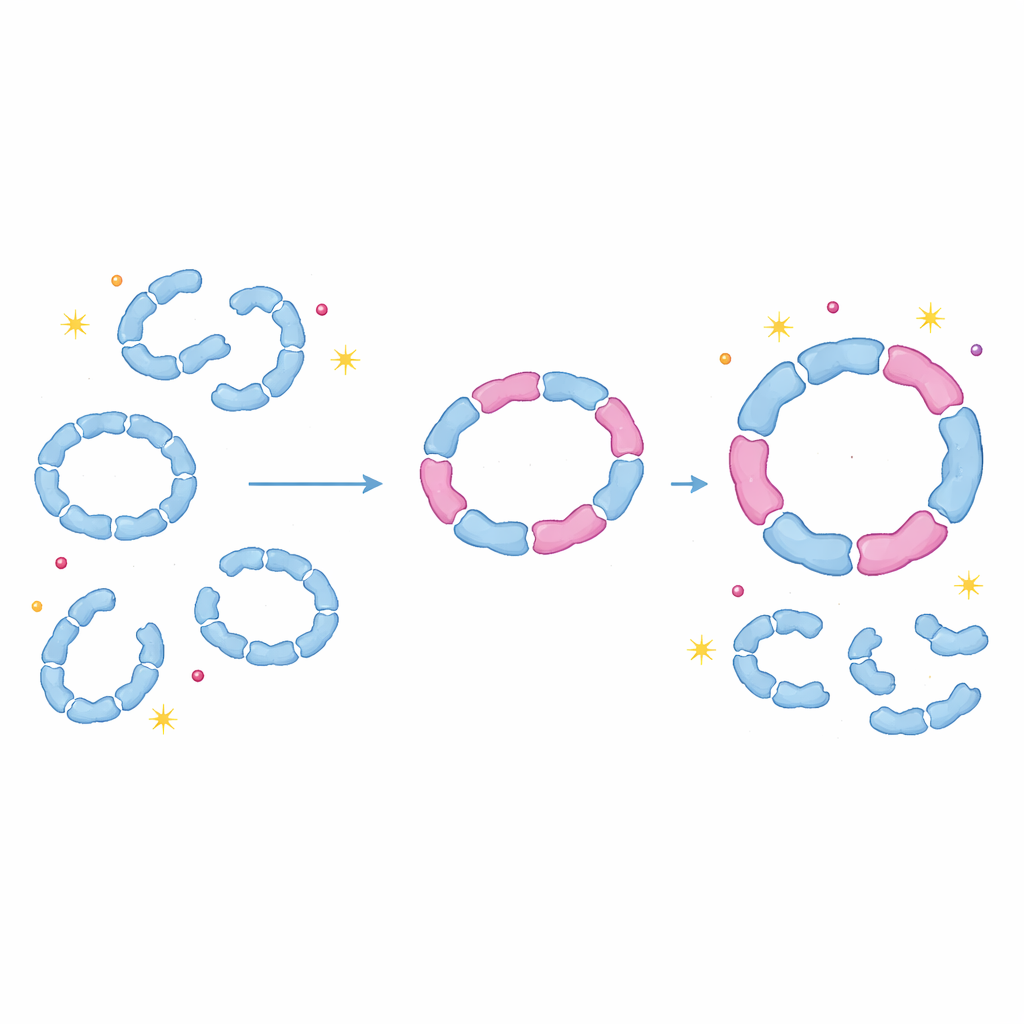
Om te testen of dit mengen binnen levende cellen van belang is, tagde het team Tsa1 en Tsa2 met een fluorescentiesensor en volgde hun gedrag in gist. Onder normale groeicondities is Tsa1 overvloedig terwijl Tsa2 schaars is, en bevindt Tsa1 zich voornamelijk in kleinere vormen. Wanneer de cellen aan waterstofperoxide werden blootgesteld, schoot de productie van Tsa2 omhoog en verschenen duidelijke banden die overeenkomen met grotere ringvormige assemblages op native gels. Intrigerend was dat zelfs de opname van slechts één of twee Tsa2-eenheden in een Tsa1-ring voldoende was om de tien-eenheidsstructuur te stabiliseren tegen het uit elkaar vallen bij verwarming. Enzymkinetiek toonde aan dat deze hybride ringen volledig actief bleven, met reactiesnelheden vergelijkbaar met die van de zuivere vormen maar met een verminderde neiging tot over-oxidatie en inactivatie.
Een wijdverbreide strategie om eiwitfunctie te tunen
Het verhaal hield niet op bij gist. In humane niercellen scheidden de auteurs twee nauwe peroxiredoxines, PRDX1 en PRDX2, door ionenwisselchromatografie. In cellen die één isoform misten, eluëerde elk overgebleven eiwit als een afzonderlijke soort. In normale cellen eluëerden de twee isoformen echter over een gedeeld bereik, in overeenstemming met de aanwezigheid van gemengde complexen. Vergelijkbare experimenten in gist die waren aangepast om menselijke, plantaardige en parasitaire peroxiredoxines te produceren, toonden dat paren uit al deze organismen functionele hybriden konden vormen. In chloroplastenzymen van planten en in een parasiet die leishmaniasis veroorzaakt, kon het introduceren van een meer 'dekameer‑minnende' isoform een meer dimerische partner in grotere ringen trekken, of omgekeerd ringen destabiliseren afhankelijk van welke subunit domineerde. Bioinformatica-analyse van meer dan 1.500 eukaryote genomen wees uit dat in meer dan 80% van de soorten waarschijnlijk meerdere Prx1‑type peroxiredoxines in hetzelfde compartiment voorkomen, wat suggereert dat mengen eerder de regel dan de uitzondering is.
Proteïnen als instelbare schokdempers
Door aan te tonen dat peroxiredoxines routinematig gemengde ringen en dimeren bouwen, daagt dit werk de lang bestaande veronderstelling uit dat elk isoform alleen als zuivere assemblage functioneert. In plaats daarvan lijken cellen hetero-oligomerisatie te gebruiken als een flexibele manier om de stabiliteit van deze ringen aan te passen, hoe gevoelig ze zijn voor schade en wanneer ze schakelen tussen ontgiftings- en chaperonnefuncties. Een kleine verandering in expressie van één isoform, bijvoorbeeld tijdens oxiderende stress, kan als een rimpeling door het systeem werken door vele gemengde complexen tegelijk te hervormen. Voor niet‑specialisten is de kernboodschap dat eiwitcomplexen zich minder gedragen als rigide Lego‑modellen en meer als instelbare schokdempers: door verschillende maar compatibele onderdelen in te wisselen kunnen cellen hun bescherming tegen oxiderende stress subtiel afstemmen, met implicaties voor veroudering, kanker, infectie en andere aandoeningen waarin de redoxbalans verstoord raakt.
Bronvermelding: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Trefwoorden: peroxiredoxine, oxiderende stress, proteïnecomplexen, redoxsignaalgeving, cellulaire aanpassing