Clear Sky Science · de
Hetero‑Oligomerisierung treibt die strukturelle Plastizität eukaryotischer Peroxiredoxine an
Proteine, die sich umformen, um unsere Zellen zu schützen
In jeder Zelle tobt ein stiller Kampf gegen reaktive Sauerstoffmoleküle, die DNA, Proteine und Lipide schädigen können. Eine Enzymfamilie namens Peroxiredoxine fungiert als erste Verteidigungslinie, detoxifiziert diese reaktiven Spezies und hilft den Zellen zu erkennen, wenn sich das Oxidationsniveau ändert. Jahrelang gingen Wissenschaftler davon aus, dass jedes Peroxiredoxin allein in gleichförmigen Clustern aus identischen Bausteinen arbeitet. Diese Studie widerruft diese Ansicht, indem sie zeigt, dass viele Peroxiredoxine tatsächlich mit nahe verwandten Geschwistern mischen und hybride Verbände bilden, die Form und Stabilität so verändern, dass sie die Fähigkeit der Zellen zur Stressbewältigung feinjustieren könnten.
Warum Teamarbeit von Proteinen wichtig ist
Peroxiredoxine gehören zu den am häufigsten vorkommenden Proteinen in Organismen von der Hefe bis zu Mensch und Pflanze. Sie entfernen Wasserstoffperoxid, ein reaktives Nebenprodukt des Stoffwechsels, und fungieren außerdem als molekulare Chaperone, die anderen Proteinen helfen, ihre Struktur zu erhalten. Das klassische Lehrbuchbild zeigt diese Enzyme entweder als Paare (Dimere) oder als ringförmige Zehner‑Ringe (Dekamere), jedoch immer aufgebaut aus einer Isoform zur Zeit. Dennoch tragen viele Zellen zwei fast identische Versionen desselben Peroxiredoxins im gleichen Kompartiment. Die Autoren stellten eine einfache, aber grundlegende Frage: Bleiben diese Isoformen wirklich getrennt, oder setzen sie sich zu gemischten Komplexen mit neuen Eigenschaften zusammen?
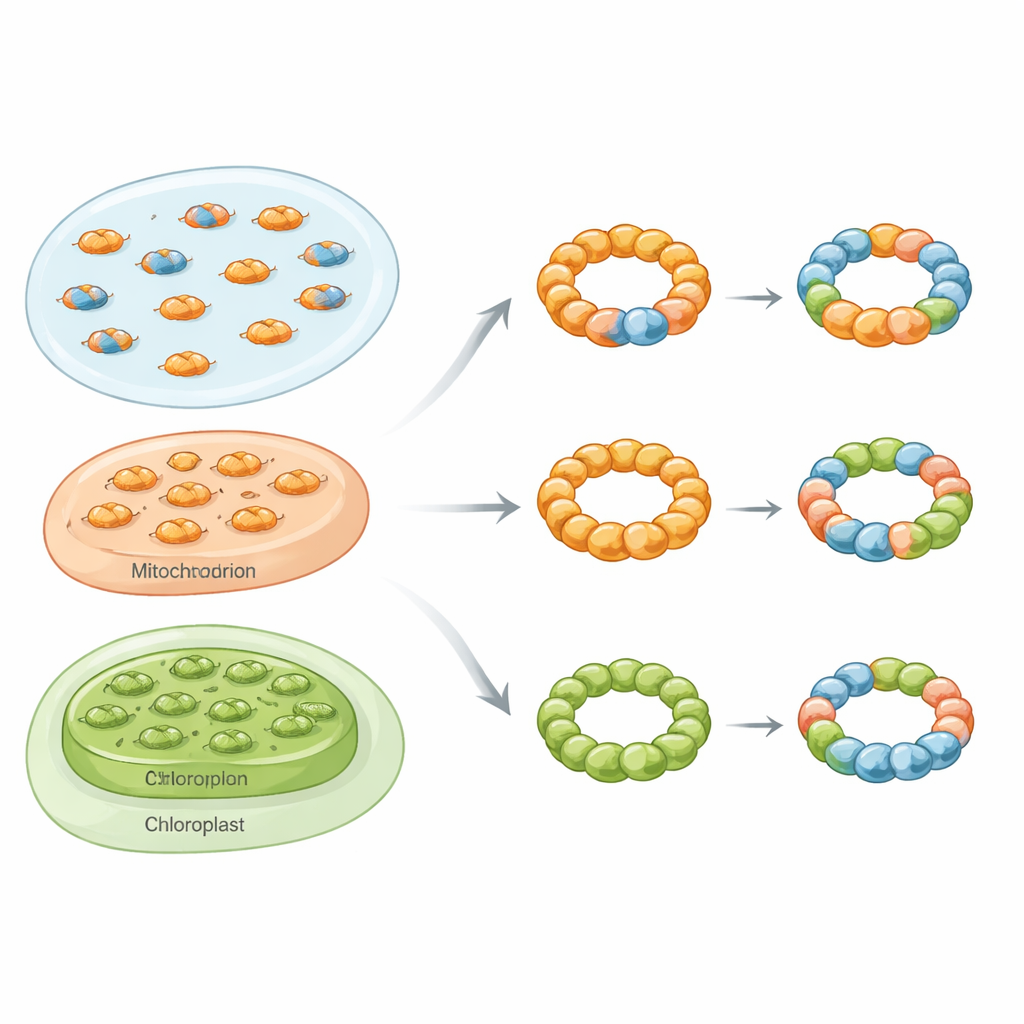
Gemischte Ringe in allen Lebensbereichen
Mithilfe eines Werkzeugkastens, zu dem biochemische Aufreinigung, native Massenspektrometrie, Elektronenmikroskopie und Live‑Zell‑Fluoreszenzassays gehörten, zeigen die Forschenden, dass gemischte bzw. hetero‑oligomere Peroxiredoxin‑Komplexe keine seltenen Kuriositäten sind. Bei der Backhefe konzentrierten sie sich auf zwei zytosolische Isoformen namens Tsa1 und Tsa2. Wenn die beiden Proteine gemeinsam in Bakterien produziert wurden, bildeten sie sowohl gemischte Dimere als auch gemischte Dekamere mit einem Spektrum an Untereinheitsverhältnissen. Unter dem Elektronenmikroskop erschienen diese Verbände als charakteristische ringförmige Partikel, was bestätigt, dass Tsa1 und Tsa2 dieselbe strukturelle Gerüst teilen können, statt nur getrennte Ringe zu bilden.
Stressausgelöste Umformung in Hefezellen
Um zu prüfen, ob dieses Mischen in lebenden Zellen eine Rolle spielt, markierte das Team Tsa1 und Tsa2 mit einem fluoreszenten Sensor und verfolgte ihr Verhalten in Hefe. Unter normalen Wachstumsbedingungen ist Tsa1 reichlich vorhanden, während Tsa2 selten ist, und Tsa1 liegt überwiegend in kleineren Formen vor. Wurden die Zellen Wasserstoffperoxid ausgesetzt, stieg die Produktion von Tsa2 stark an, und auf nativen Gelen traten klare Banden auf, die größeren ringförmigen Assemblierungen entsprachen. Interessanterweise reichte schon die Einfügung einer oder zweier Tsa2‑Untereinheiten in einen Tsa1‑Ring aus, um die Zehner‑Struktur gegen Zerfall bei Erwärmung zu stabilisieren. Enzymkinetische Messungen zeigten, dass diese hybriden Ringe voll aktiv blieben, mit Reaktionsraten vergleichbar zu den reinen Formen, jedoch mit geringerer Neigung zur Überoxidation und Inaktivierung.
Eine weit verbreitete Strategie zur Feinabstimmung von Proteinfunktionen
Die Geschichte endete nicht bei der Hefe. In menschlichen Nierenzellen trennten die Autoren zwei eng verwandte Peroxiredoxine, PRDX1 und PRDX2, mittels Ionenaustauschchromatographie. In Zellen, denen eine Isoform fehlte, eluierten die jeweils verbleibenden Proteine als unterschiedliche Spezies. In normalen Zellen hingegen eluierten beide Isoformen überlappend in einem gemeinsamen Bereich, was mit dem Vorhandensein gemischter Komplexe vereinbar ist. Ähnliche Tests in Hefe, die so konstruiert wurde, dass sie menschliche, pflanzliche und parasitäre Peroxiredoxine produziert, zeigten, dass Paare aus all diesen Organismen funktionelle Hybride bilden können. In pflanzlichen Chloroplastenenzymen und in einem Parasiten, der Leishmaniose verursacht, konnte die Einführung einer eher „dekamerfreundlichen“ Isoform einen eher dimerischen Partner in größere Ringe ziehen oder umgekehrt Ringe destabilisieren, je nachdem welche Untereinheit dominierte. Bioinformatische Analysen von mehr als 1.500 eukaryotischen Genomen ergaben, dass über 80 % der Arten vermutlich mehrere Prx1‑Typ Peroxiredoxine im selben Kompartiment besitzen, was darauf hindeutet, dass solches Mischen die Regel und nicht die Ausnahme ist.
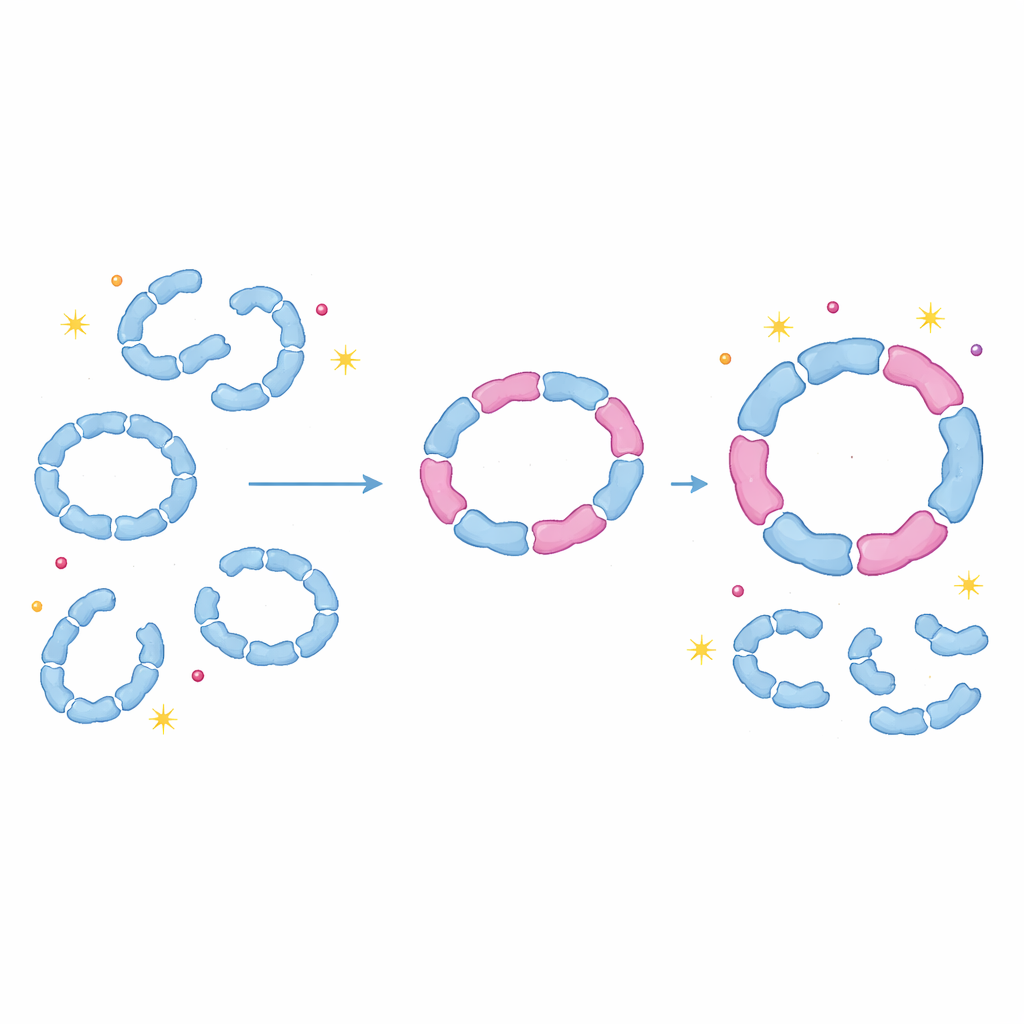
Proteine als einstellbare Stoßdämpfer
Indem gezeigt wird, dass Peroxiredoxine routinemäßig gemischte Ringe und Dimere bilden, stellt diese Arbeit die langjährige Annahme in Frage, dass jede Isoform nur als reine Assemblierung funktioniert. Stattdessen scheinen Zellen Hetero‑Oligomerisierung als flexibles Mittel zu nutzen, um die Stabilität dieser Ringe zu justieren, ihre Empfindlichkeit gegenüber Schäden zu steuern und den Zeitpunkt ihres Wechsels zwischen Entgiftungs‑ und Chaperon‑Rollen zu bestimmen. Eine kleine Veränderung in der Expression einer Isoform, etwa während oxidativen Stresses, kann das System durch die Umformung vieler gemischter Komplexe gleichzeitig beeinflussen. Für Nicht‑Spezialisten lautet die Kernbotschaft: Proteinkomplexe verhalten sich weniger wie starre Lego‑Modelle und mehr wie einstellbare Stoßdämpfer: Durch das Austauschen unterschiedlicher, aber kompatibler Teile können Zellen ihren Schutz gegen oxidativen Stress subtil abstimmen — mit Konsequenzen für Altern, Krebs, Infektionen und andere Zustände, in denen das Redoxgleichgewicht gestört ist.
Zitation: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Schlüsselwörter: Peroxiredoxin, oxidativer Stress, Proteinkomplexe, Redox‑Signaling, zelluläre Anpassung