Clear Sky Science · ru
Гетеро-олигомеризация обусловливает структурную пластичность перокси редоксинов эукариот
Белки, которые меняют форму, чтобы защищать наши клетки
Внутри каждой клетки ведётся тихая борьба с реактивными кислородными молекулами, способными повредить ДНК, белки и липиды. Семейство ферментов под названием пероксиредоксины выступает в роли передовой линии защиты, детоксифицируя эти реактивные виды и помогая клеткам чувствовать изменения степени окисления. Годы считалось, что каждый пероксиредоксин действует отдельно в однородных кластерах, составленных из идентичных звеньев. Это исследование опровергает такое представление, показывая, что многие пероксиредоксины на самом деле смешиваются с близкородственными собратьями, образуя гибридные сборки, которые меняют форму и стабильность и тем самым могут точно настраивать реакцию клетки на стресс.
Почему командная работа белков имеет значение
Пероксиредоксины — одни из самых многочисленных белков у организмов от дрожжей до человека и растений. Они удаляют перекись водорода, реактивный побочный продукт метаболизма, а также действуют как молекулярные шапероны, помогающие другим белкам сохранять правильную конформацию. Классический учебный образ показывает эти ферменты собирающимися либо в пары (димеры), либо в бубликоподобные кольца из десяти единиц (декамеры), но всегда построенные из одного изоформа. Однако во многих клетках в одном и том же компартменте присутствуют два почти тождественных варианта одного пероксиредоксина. Авторы задали простой, но фундаментальный вопрос: действительно ли эти изоформы остаются раздельными или они собираются в смешанные комплексы с новыми свойствами?
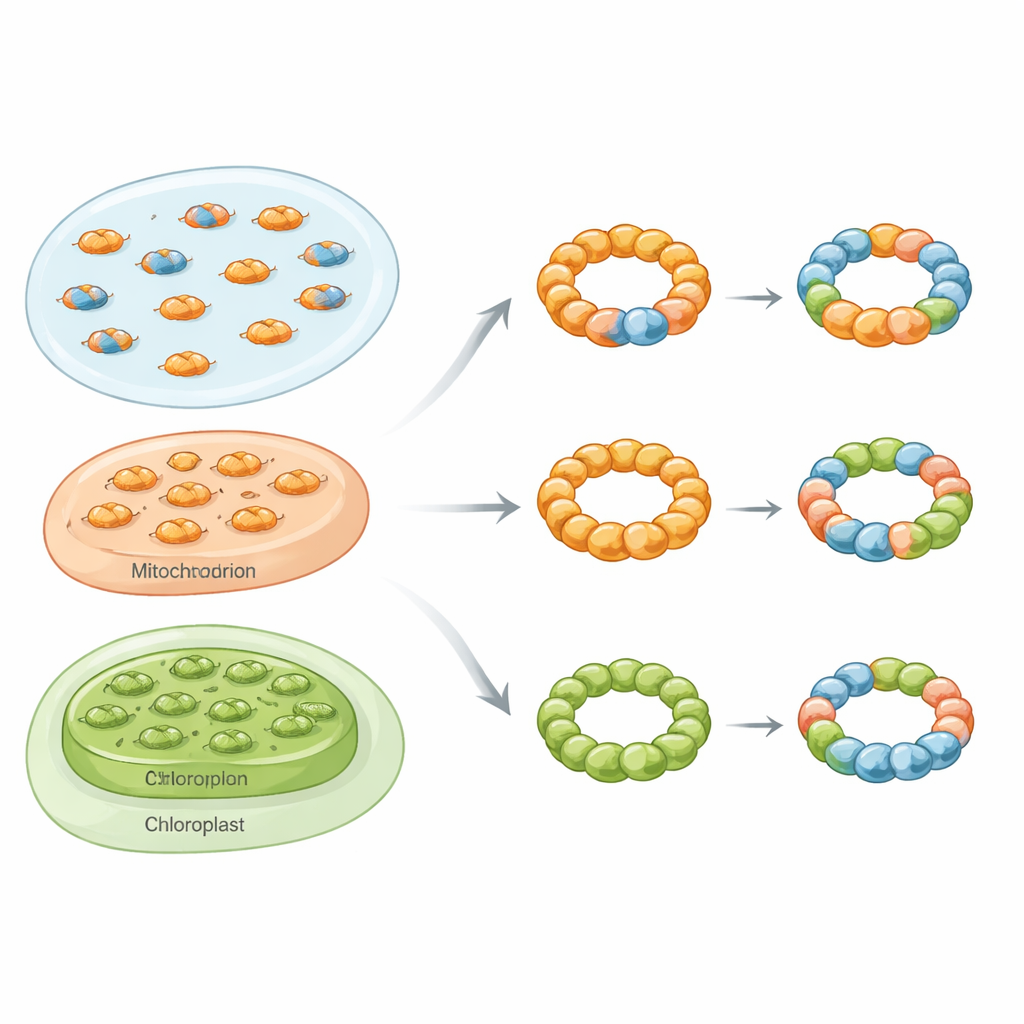
Смешанные кольца в разных царствах жизни
Используя набор методов, включавших биохимическую очистку, нативную массфотометрию, электронную микроскопию и флуоресцентные тесты в живых клетках, исследователи показали, что смешанные, или гетеро-олигомерные, комплексы пероксиредоксинов — не редкие исключения. У пекарских дрожжей они сосредоточили внимание на двух цитозольных изоформах, названных Tsa1 и Tsa2. Когда оба белка синтезировали вместе в бактериях, они образовывали как смешанные димеры, так и смешанные декамеры с распределением соотношений субъединиц. Под электронным микроскопом эти сборки выглядели как характерные кольцевые частицы, что подтверждало: Tsa1 и Tsa2 могут разделять одну и ту же структурную основу, а не формировать только отдельные кольца.
Перестройка под действием стресса в клетках дрожжей
Чтобы проверить, важно ли такое смешение в живых клетках, команда пометила Tsa1 и Tsa2 флуоресцентным датчиком и отслеживала их поведение в дрожжах. При нормальном росте Tsa1 присутствует в избытке, тогда как Tsa2 встречается редко, и Tsa1 в основном находится в более мелких формах. При обработке клеток перекисью водорода синтез Tsa2 резко возрастал, и на нативных гелях появлялись чёткие полосы, соответствующие крупным кольцеобразным сборкам. Любопытно, что даже включение всего одной-двух молекул Tsa2 в кольцо Tsa1 было достаточным, чтобы стабилизировать десятизвенную структуру и предотвратить её распад при нагревании. Кинетика фермента показала, что эти гибридные кольца остаются полностью активными, с скоростями реакции, сопоставимыми с чистыми формами, но с пониженной склонностью к переокислению и инактивации.
Распространённая стратегия настройки функции белков
История не ограничилась дрожжами. В клетках почки человека авторы разделили два близкородственных пероксиредоксина, PRDX1 и PRDX2, с помощью ионообменной хроматографии. В клетках, лишённых одного из изоформ, каждый остававшийся белок элюировался как отдельный вид. В нормальных же клетках оба изоформа ко-элюировались в общем диапазоне, что согласуется с наличием смешанных комплексов. Похожие тесты в дрожжах, генетически модифицированных для синтеза человеческих, растительных и паразитных пероксиредоксинов, показали, что пары из всех этих организмов способны образовывать функциональные гибриды. У ферментов хлоропластов растений и у паразита, вызывающего лейшманиоз, введение более «любит-декамеры» изоформа могло втянуть более димерный партнёр в большие кольца или, наоборот, дестабилизировать кольца в зависимости от доминирования того или иного субъединичного типа. Биоинформатический анализ более чем 1500 эукариотических геномов показал, что у свыше 80% видов, вероятно, присутствуют несколько пероксиредоксинов типа Prx1 в одном компартменте, что указывает на то, что подобное смешение скорее правило, чем исключение.
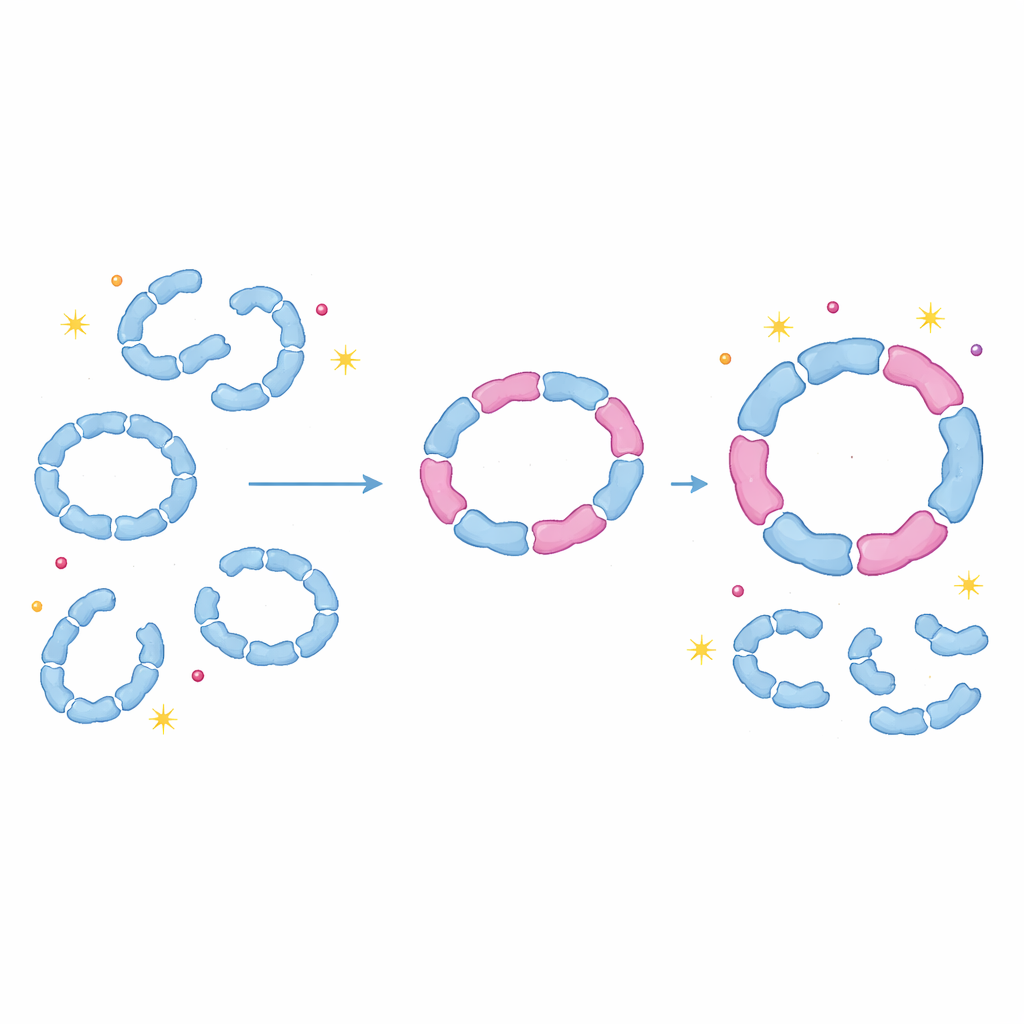
Белки как настраиваемые демпферы
Показав, что пероксиредоксины регулярно собирают смешанные кольца и димеры, эта работа ставит под сомнение давнее предположение, что каждый изоформ функционирует только в виде чистой сборки. Вместо этого клетки, по-видимому, используют гетеро-олигомеризацию как гибкий механизм регулирования стабильности колец, их чувствительности к повреждению и момента переключения между функциями детоксикации и шаперонной поддержкой. Небольшое изменение экспрессии одного изоформа, например во время окислительного стресса, может вызвать каскад изменений, перестроив множество смешанных комплексов одновременно. Для неспециалистов главный вывод таков: белковые комплексы ведут себя меньше как жёсткие модели Лего и больше как настраиваемые демпферы — за счёт замены на совместимые, но разные элементы клетки могут тонко регулировать защиту от окислительного стресса, что имеет значение для старения, рака, инфекций и других состояний, где нарушен редокс‑баланс.
Цитирование: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Ключевые слова: пероксиредоксин, окислительный стресс, белковые комплексы, редокс-сигналинг, клеточная адаптация