Clear Sky Science · fr
Hétéro‑oligomérisation conduit à la plasticité structurelle des peroxirédoxines eucaryotes
Des protéines qui se remodelent pour protéger nos cellules
À l’intérieur de chaque cellule se déroule une bataille discrète contre des molécules réactives de l’oxygène susceptibles d’endommager l’ADN, les protéines et les lipides. Une famille d’enzymes appelée peroxirédoxines joue le rôle de première ligne de défense, détoxifiant ces espèces réactives et aidant les cellules à détecter les variations du niveau d’oxydation. Pendant des années, les scientifiques ont pensé que chaque peroxirédoxine fonctionnait de façon indépendante dans des assemblages uniformes composés de blocs identiques. Cette étude renverse cette vision en montrant que de nombreuses peroxirédoxines se combinent en réalité avec des homologues proches, formant des assemblages hybrides qui modifient leur forme et leur stabilité d’une manière qui pourrait affiner la façon dont les cellules gèrent le stress.
Pourquoi le travail d’équipe des protéines compte
Les peroxirédoxines figurent parmi les protéines les plus abondantes chez des organismes allant de la levure aux humains et aux plantes. Elles éliminent le peroxyde d’hydrogène, un sous‑produit réactif du métabolisme, et agissent également comme chaperons moléculaires aidant d’autres protéines à conserver leur conformation. L’image classique montre ces enzymes s’assemblant soit en paires (dimères), soit en anneaux en forme de beigne de dix unités (décamères), mais toujours constitués d’une seule isoforme à la fois. Pourtant, de nombreuses cellules portent deux versions quasi identiques de la même peroxirédoxine dans le même compartiment. Les auteurs se sont posé une question simple mais fondamentale : ces isoformes restent‑elles vraiment séparées, ou s’assemblent‑elles en complexes mixtes dotés de nouvelles propriétés ?
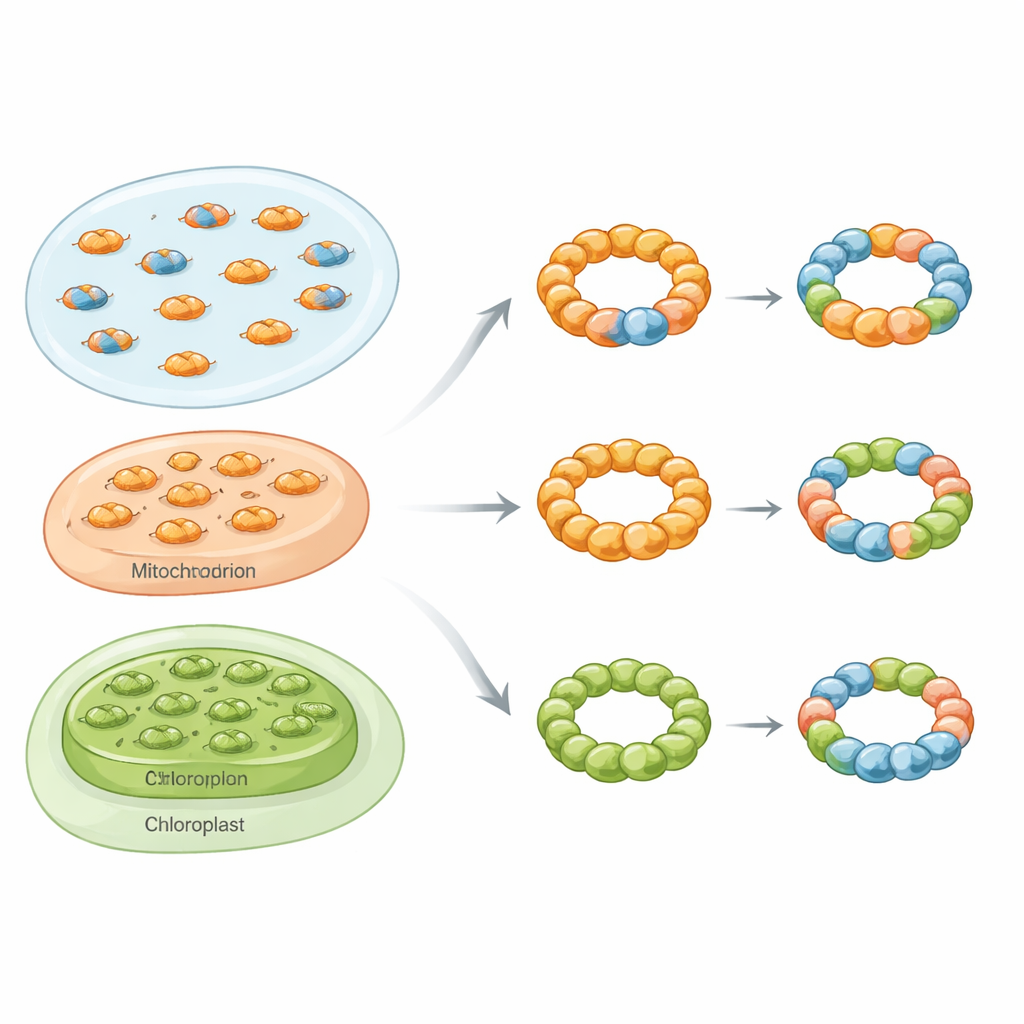
Anneaux mixtes à travers les règnes du vivant
En utilisant une boîte à outils comprenant purification biochimique, photométrie de masse native, microscopie électronique et essais de fluorescence en cellules vivantes, les chercheurs montrent que les complexes peroxirédoxine mixtes, ou hétéro‑oligomériques, ne sont pas des curiosités rares. Chez la levure de boulanger, ils se sont concentrés sur deux isoformes cytosoliques appelées Tsa1 et Tsa2. Lorsque les deux protéines ont été produites ensemble dans des bactéries, elles ont formé à la fois des dimères mixtes et des décamères mixtes avec un spectre de rapports de sous‑unités. Au microscope électronique, ces assemblages apparaissaient comme des particules en anneau caractéristiques, confirmant que Tsa1 et Tsa2 peuvent partager la même architecture structurelle au lieu de former uniquement des anneaux séparés.
Remodelage déclenché par le stress dans les cellules de levure
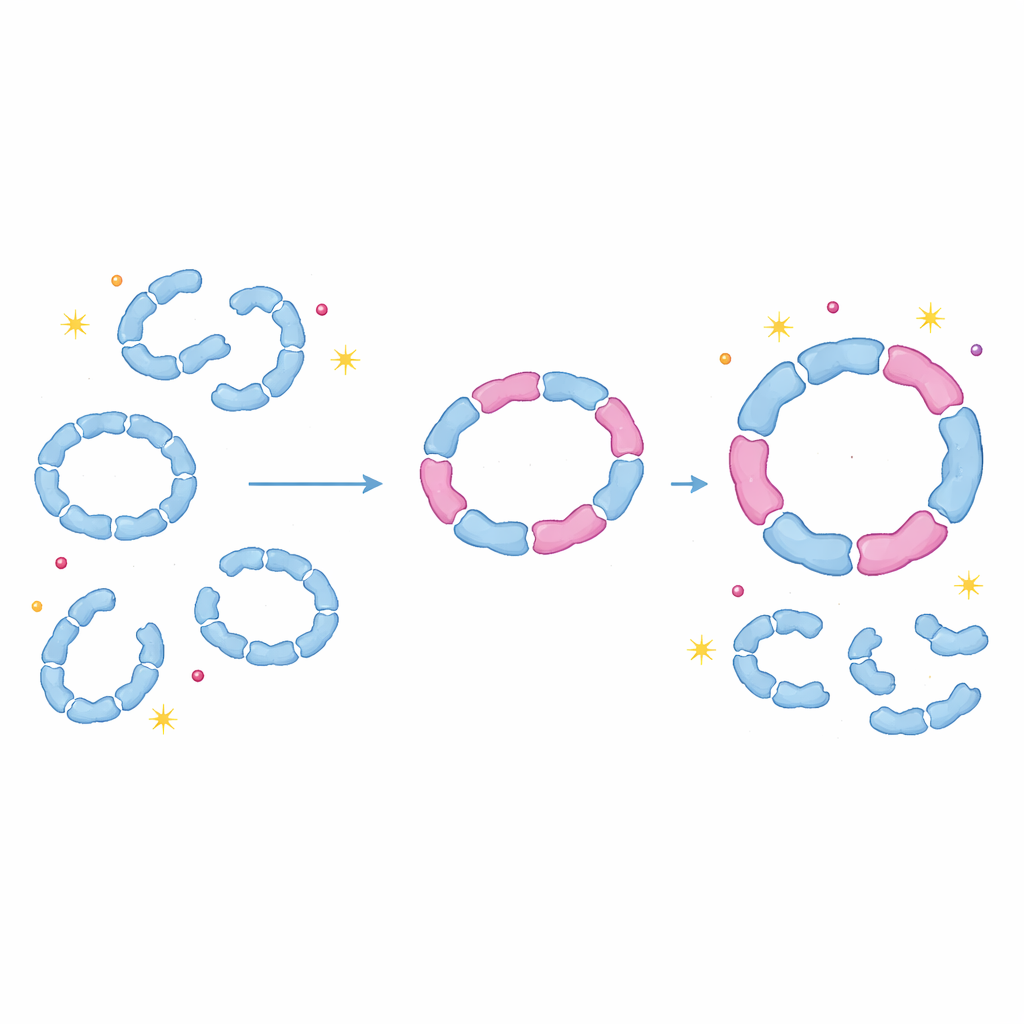
Pour vérifier si ce mélange a une importance dans les cellules vivantes, l’équipe a marqué Tsa1 et Tsa2 avec un capteur fluorescent et a suivi leur comportement dans la levure. En conditions de croissance normales, Tsa1 est abondante tandis que Tsa2 est rare, et Tsa1 se trouve principalement sous des formes plus petites. Lorsque les cellules ont été exposées au peroxyde d’hydrogène, la production de Tsa2 a fortement augmenté, et des bandes nettes correspondant à des assemblages plus grands en anneau sont apparues sur des gels natifs. Fait intrigant, l’incorporation d’une ou deux unités de Tsa2 seulement dans un anneau de Tsa1 suffisait à stabiliser la structure décamérique contre la désassemblage lors d’un réchauffement. La cinétique enzymatique a montré que ces anneaux hybrides restaient pleinement actifs, avec des vitesses de réaction similaires aux formes pures mais une tendance réduite à être sur‑oxydés et inactivés.
Une stratégie répandue pour ajuster la fonction des protéines
L’histoire ne s’est pas arrêtée à la levure. Dans des cellules rénales humaines, les auteurs ont séparé deux peroxirédoxines étroitement liées, PRDX1 et PRDX2, par chromatographie par échange d’ions. Dans des cellules dépourvues d’une isoforme, chaque protéine restante élait comme une espèce distincte. Dans des cellules normales, cependant, les deux isoformes co‑éluaient sur une plage commune, compatible avec la présence de complexes mixtes. Des essais similaires dans des levures génétiquement modifiées pour produire des peroxirédoxines humaines, végétales et de parasites ont montré que des paires de ces organismes pouvaient former des hybrides fonctionnels. Dans des enzymes de chloroplastes végétaux et chez un parasite responsable de la leishmaniose, l’introduction d’une isoforme plus « adepte du décamère » pouvait attirer un partenaire plus dimérique dans des anneaux plus grands, ou inversement déstabiliser les anneaux selon l’isoforme dominante. Des analyses bioinformatiques de plus de 1 500 génomes eucaryotes ont révélé que plus de 80 % des espèces hébergent probablement plusieurs peroxirédoxines de type Prx1 dans le même compartiment, suggérant que ce mélange est la règle plutôt que l’exception.
Des protéines comme amortisseurs réglables
En montrant que les peroxirédoxines construisent couramment des anneaux et des dimères mixtes, ce travail remet en cause l’hypothèse de longue date selon laquelle chaque isoforme fonctionnerait uniquement en assemblage pur. Au contraire, les cellules semblent utiliser l’hétéro‑oligomérisation comme un moyen flexible d’ajuster la stabilité de ces anneaux, leur sensibilité aux dommages et le moment où elles basculent entre rôles de détoxification et de chaperon. Un petit changement d’expression d’une isoforme, par exemple lors d’un stress oxydatif, peut se répercuter dans le système en remodelant simultanément de nombreux complexes mixtes. Pour le grand public, le message clé est que les complexes protéiques se comportent moins comme des modèles Lego rigides et plus comme des amortisseurs réglables : en échangeant des pièces différentes mais compatibles, les cellules peuvent ajuster finement leur protection contre le stress oxydatif, avec des implications pour le vieillissement, le cancer, les infections et d’autres conditions où l’équilibre redox est perturbé.
Citation: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Mots-clés: peroxirédoxine, stress oxydatif, complexes protéiques, signalisation redox, adaptation cellulaire