Clear Sky Science · ja
ヘテロオリゴマー化が真核生物ペロキシレドキシンの構造可塑性を促す
細胞を守るために自ら形を変えるタンパク質たち
細胞の内部では、DNA、タンパク質、脂質を損傷する活性酸素分子に対する静かな戦いが続いています。ペロキシレドキシンと呼ばれる酵素群は最前線の防御としてこれらの反応性種を解毒し、酸化状態の変化を細胞が感知するのを助けます。これまで研究者は各ペロキシレドキシンが同一の構成単位からなる均一なクラスターとして単独で働くと考えてきましたが、本研究は多くのペロキシレドキシンが実際には近縁のパートナーと混ざり合い、ハイブリッドな集合体を形成して形状や安定性を変えることで、細胞のストレス応答を微調整している可能性を示しています。
なぜタンパク質の協働が重要か
ペロキシレドキシンは酵母から人間、植物に至るまで幅広い生物で最も豊富に存在するタンパク質の一つです。代謝の副産物である過酸化水素を除去するだけでなく、他のタンパク質の折れ畳みを助ける分子シャペロンとしても機能します。教科書的な像では、これらの酵素は二量体(ダイマー)または十量体のドーナツ状リング(デカマー)として集合しますが、常に一つのアイソフォームだけで構成されるとされてきました。ところが多くの細胞は同じ区画にほぼ双子のような二つのペロキシレドキシンを持っています。著者らは単純だが根本的な疑問を投げかけました:これらのアイソフォームは本当に別々に存在し続けるのか、それとも新たな性質を持つ混合複合体を形成するのか?
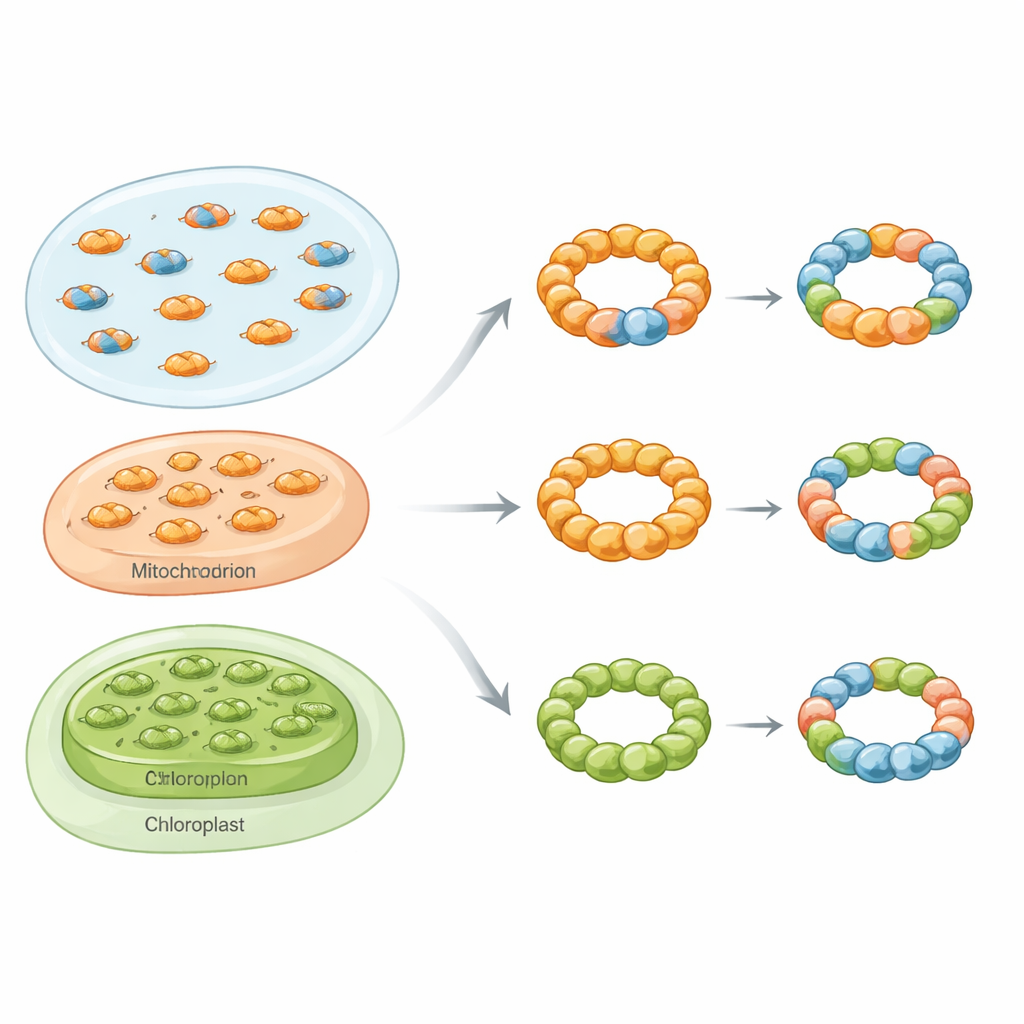
生物界を横断する混合リング
生化学的精製、ネイティブ質量光散乱(マスフォトメトリー)、電子顕微鏡、ライブセル蛍光アッセイなどを組み合わせた解析により、研究者らは混合、すなわちヘテロオリゴマー性のペロキシレドキシン複合体が稀な珍奇現象ではないことを示しました。パン酵母では、細胞質に存在するTsa1とTsa2という二つのアイソフォームに注目しました。両方のタンパク質を大腸菌で同時に発現させると、混合ダイマーと混合デカマーの両方が、様々なサブユニット比で形成されました。電子顕微鏡では、これらの集合体は特徴的なリング状粒子として観察され、Tsa1とTsa2が別々のリングを形成するだけでなく同じ構造的足場を共有できることを裏付けました。
酵母細胞でのストレス誘導による形状変化
この混合が生細胞内で意味を持つかを調べるため、研究チームはTsa1とTsa2に蛍光センサーをタグ付けし、酵母内での振る舞いを追跡しました。通常の増殖条件下ではTsa1が豊富でTsa2は稀であり、Tsa1は主に小さな形態で存在していました。細胞を過酸化水素にさらすと、Tsa2の産生が急増し、ネイティブゲル上で大きなリング状集合体に対応する明確なバンドが現れました。興味深いことに、Tsa1リングに1〜2個のTsa2サブユニットが組み込まれるだけで、加温時に十量体構造が崩れるのを防ぐのに十分な安定化効果がありました。酵素動力学の解析は、これらのハイブリッドリングが純粋な形と同様に完全に活性を保ちつつ、過酸化による不活性化を受けにくくなっていることを示しました。
タンパク質機能を調整する広範な戦略
この物語は酵母にとどまりません。ヒトの腎臓細胞では、著者らはイオン交換クロマトグラフィーで二つの近縁なペロキシレドキシン、PRDX1とPRDX2を分離しました。あるアイソフォームを欠く細胞では、残る各タンパク質は明確に異なるピークとして溶出しましたが、正常な細胞では両アイソフォームが共通の範囲で共溶出し、混合複合体の存在と一致しました。ヒト、植物、寄生虫のペロキシレドキシンを発現するよう改変した酵母での類似実験は、これらすべての生物の対が機能的なハイブリッドを形成できることを示しました。植物の葉緑体酵素やリーシュマニア症を起こす寄生虫においても、“デカマー志向”のアイソフォームを導入すると、よりダイマー寄りのパートナーを大きなリングへと引き込んだり、どのサブユニットが優勢かによっては逆にリングを不安定化させたりしました。1,500以上の真核生物ゲノムを用いたバイオインフォマティクス解析では、80%以上の種が同一区画内に複数のPrx1型ペロキシレドキシンを持つ可能性が高いことが示され、このような混合が例外ではなくむしろ規則であることが示唆されました。
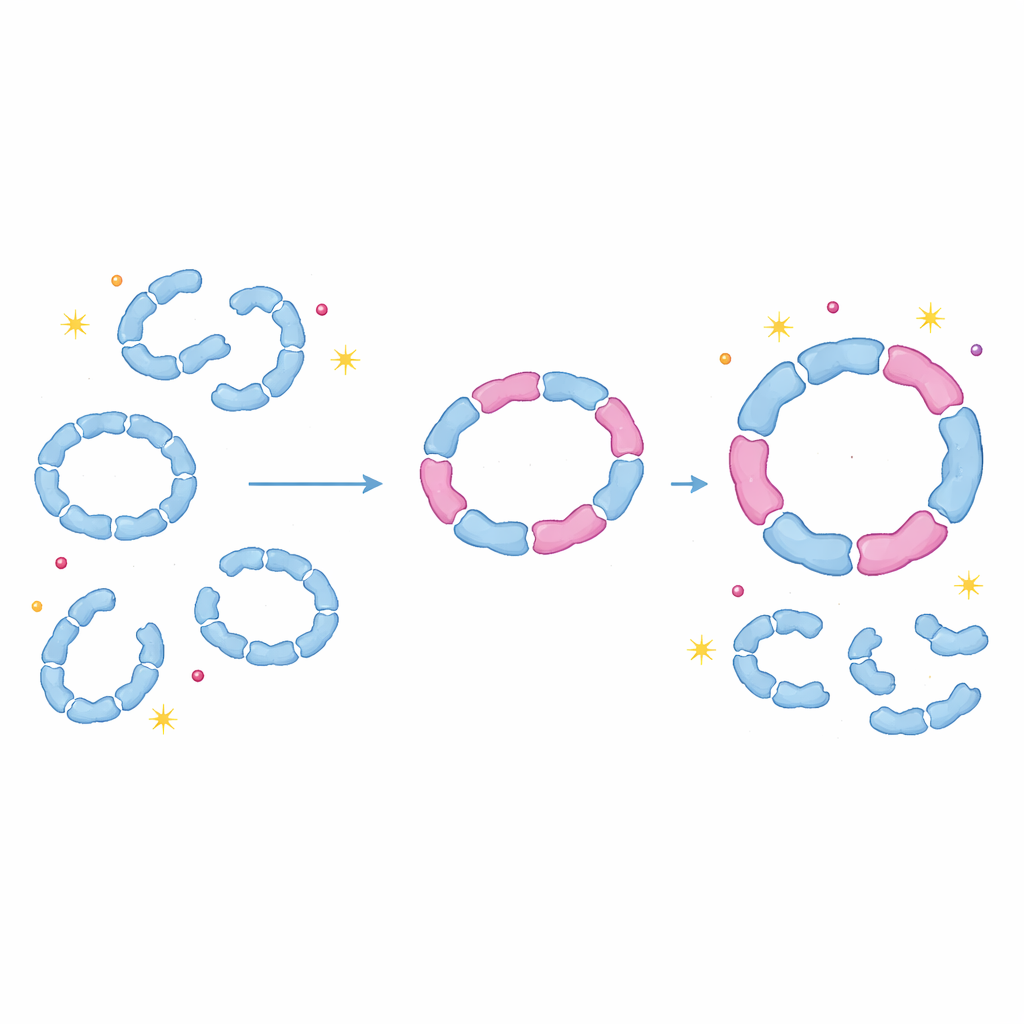
可変なショックアブソーバーとしてのタンパク質
ペロキシレドキシンが日常的に混合リングや混合ダイマーを構築することを示すことで、この研究は各アイソフォームが純粋な集合体としてのみ機能するという長年の前提に挑戦します。代わりに、細胞はヘテロオリゴマー化を用いてリングの安定性、損傷への感受性、解毒とシャペロン機能の切替えのタイミングを柔軟に調整しているように見えます。例えば酸化ストレス時の一方のアイソフォームの発現の小さな変化は、多くの混合複合体を同時に再形成することで系全体に波及効果をもたらします。専門外の方への要点は、タンパク質複合体は堅いレゴのモデルというよりも可変なショックアブソーバーに近く、互換性のある異なる部品を差し替えることで、細胞は酸化ストレスに対する防御を微妙に調整できるということです。これは加齢、がん、感染症など、レドックスバランスが乱れるさまざまな状況に影響を及ぼす可能性があります。
引用: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
キーワード: ペロキシレドキシン, 酸化ストレス, タンパク質複合体, レドックスシグナル伝達, 細胞の適応