Clear Sky Science · it
L’etero-oligomerizzazione guida la plasticità strutturale delle perossiredossine eucariotiche
Proteine che si rimodellano per proteggere le nostre cellule
All’interno di ogni cellula si svolge una lotta silenziosa contro molecole ossidanti reattive in grado di danneggiare DNA, proteine e lipidi. Una famiglia di enzimi chiamata perossiredossine funge da prima linea di difesa, detossificando queste specie reattive e aiutando le cellule a rilevare le variazioni dei livelli di ossidazione. Per anni gli scienziati hanno pensato che ciascuna perossiredossina lavorasse da sola in ammassi uniformi composti da blocchi identici. Questo studio rovescia quella visione mostrando che molte perossiredossine si combinano in realtà con membri strettamente correlati, formando assemblaggi ibridi che modificano forma e stabilità in modi che potrebbero regolare finemente la risposta cellulare allo stress.
Perché il lavoro di squadra delle proteine conta
Le perossiredossine sono tra le proteine più abbondanti in organismi che vanno dal lievito agli esseri umani e alle piante. Rimuovono il perossido di idrogeno, un sottoprodotto reattivo del metabolismo, e fungono anche da chaperoni molecolari che aiutano altre proteine a mantenere la loro conformazione. L’immagine classica sui testi mostra questi enzimi che si assemblano o in coppie (dimeri) o in anelli a ciambella di dieci unità (decameri), ma costruiti sempre da una sola isoforma alla volta. Eppure molte cellule ospitano due versioni quasi gemelle della stessa perossiredossina nello stesso compartimento. Gli autori si sono posti una domanda semplice ma fondamentale: queste isoforme restano davvero separate, oppure si assemblano in complessi misti con proprietà nuove?
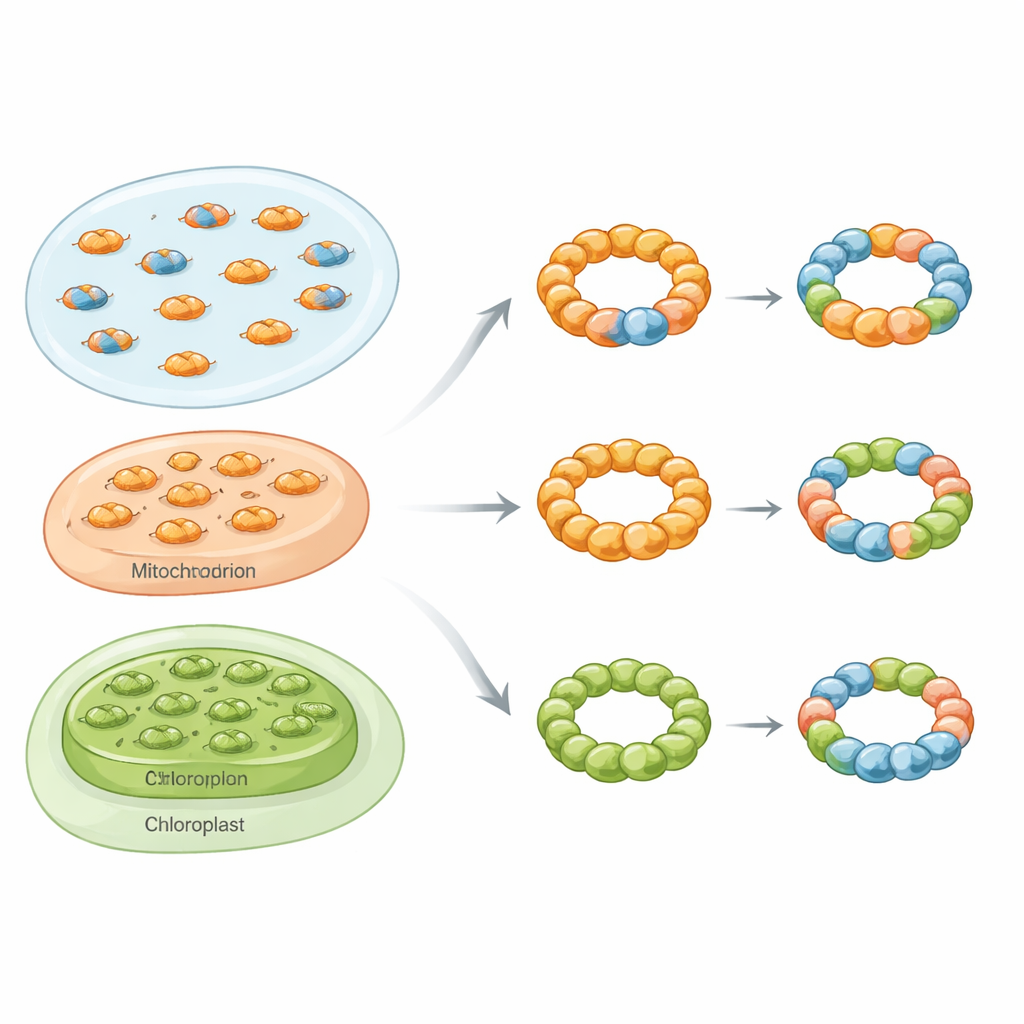
Anelli misti attraverso i regni della vita
Usando un insieme di tecniche che includevano purificazione biochimica, fotometria di massa nativa, microscopia elettronica e saggi di fluorescenza in cellule vive, i ricercatori mostrano che i complessi perossiredossina misti, o etero‑oligomerici, non sono rare curiosità. Nel lievito di birra si sono concentrati su due isoforme citosoliche chiamate Tsa1 e Tsa2. Quando le due proteine sono state prodotte insieme in batteri, hanno formato sia dimeri misti sia decameri misti con un ventaglio di rapporti tra le subunità. Al microscopio elettronico questi assemblaggi apparivano come particelle caratteristiche a forma di anello, confermando che Tsa1 e Tsa2 possono condividere lo stesso impalcatura strutturale invece di formare solo anelli separati.
Rimodellamento indotto dallo stress nelle cellule di lievito
Per verificare se questo mescolamento abbia rilevanza all’interno di cellule vive, il gruppo ha etichettato Tsa1 e Tsa2 con un sensore fluorescente e seguito il loro comportamento nel lievito. In condizioni di crescita normali, Tsa1 è abbondante mentre Tsa2 è scarsa, e Tsa1 è presente principalmente in forme più piccole. Quando le cellule sono state esposte a perossido di idrogeno, la produzione di Tsa2 è aumentata notevolmente e sulle gel native sono comparse bande corrispondenti ad assemblaggi più grandi a forma di anello. È interessante che anche l’incorporazione di una o due unità di Tsa2 in un anello di Tsa1 fosse sufficiente a stabilizzare la struttura a dieci unità contro lo smontaggio indotto dal riscaldamento. Le cinetiche enzimatiche hanno mostrato che questi anelli ibridi restano pienamente attivi, con velocità di reazione simili alle forme pure ma con minore tendenza a essere sovra‑ossidati e inattivati.
Una strategia diffusa per modulare la funzione proteica
La storia non si è fermata al lievito. In cellule renali umane, gli autori hanno separato due perossiredossine strettamente correlate, PRDX1 e PRDX2, mediante cromatografia a scambio ionico. In cellule che mancavano di una isoforma, ciascuna proteina rimanente eluteva come una specie distinta. Nelle cellule normali, tuttavia, entrambe le isoforme elutevano in una gamma condivisa, coerente con la presenza di complessi misti. Test analoghi in lieviti ingegnerizzati per produrre perossiredossine umane, vegetali e di parassiti hanno mostrato che coppie provenienti da tutti questi organismi potevano formare ibridi funzionali. Nelle perossiredossine dei cloroplasti vegetali e in un parassita che causa la leishmaniosi, l’introduzione di un’isoforma più «amante del decamero» poteva trainare un partner più dimerico verso anelli più grandi, o al contrario destabilizzare gli anelli a seconda di quale subunità prevaleva. Analisi bioinformatiche su più di 1.500 genomi eucariotici hanno rivelato che oltre l’80% delle specie probabilmente possiede più perossiredossine di tipo Prx1 nello stesso compartimento, suggerendo che tale mescolamento sia la regola piuttosto che l’eccezione.
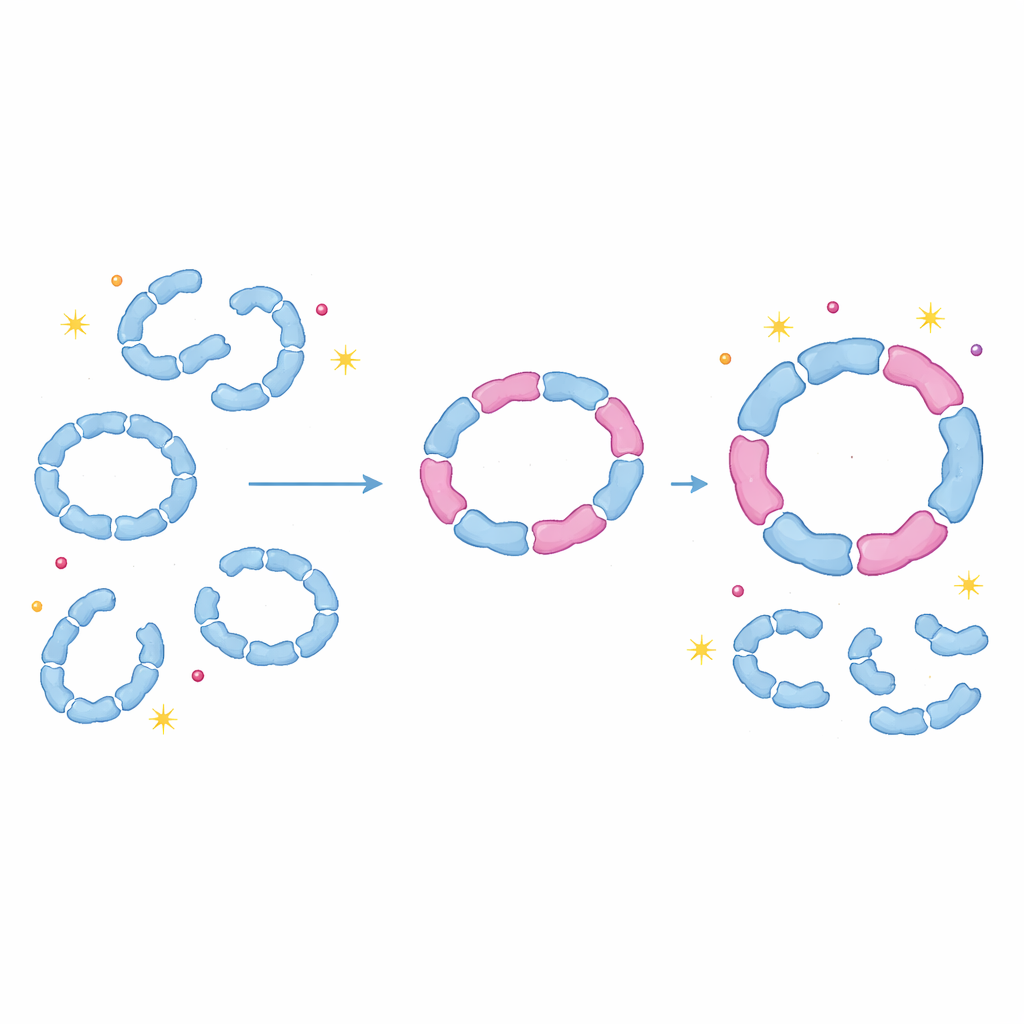
Proteine come ammortizzatori regolabili
Dimostrando che le perossiredossine costruiscono abitualmente anelli e dimeri misti, questo lavoro sfida l’assunzione di lunga data secondo cui ogni isoforma funziona soltanto come un assemblaggio puro. Al contrario, le cellule sembrano utilizzare l’etero‑oligomerizzazione come un modo flessibile per regolare quanto sono stabili questi anelli, quanto sono sensibili ai danni e quando passano tra ruoli di detossificazione e di chaperone. Una piccola variazione nell’espressione di un’isoforma, per esempio durante lo stress ossidativo, può riverberare nel sistema rimodellando molti complessi misti contemporaneamente. Per il lettore non specialista, il messaggio chiave è che i complessi proteici si comportano meno come modelli di Lego rigidi e più come ammortizzatori regolabili: sostituendo parti diverse ma compatibili, le cellule possono modulare sottilmente la loro protezione contro lo stress ossidativo, con implicazioni per l’invecchiamento, il cancro, le infezioni e altre condizioni in cui l’equilibrio redox viene compromesso.
Citazione: Zimmermann, J., Lang, L., Malo Pueyo, J. et al. Hetero-oligomerization drives structural plasticity of eukaryotic peroxiredoxins. Nat Chem Biol 22, 580–592 (2026). https://doi.org/10.1038/s41589-026-02157-6
Parole chiave: perossiredossina, stress ossidativo, complessi proteici, segnalazione redox, adattamento cellulare