Clear Sky Science · zh
成年人、衰老与阿尔茨海默病中的人类海马神经发生
为什么成人产生新脑细胞很重要
几十年来,科学家们一直围绕一个既简单又深刻的问题争论:成年人体内在大脑的记忆中心是否会生成新的神经细胞,如果会,这是否有助于保护我们免受记忆丧失和阿尔茨海默病的侵害?这项研究通过结合前沿的单细胞技术与尸检人脑组织,直接回应了这一争论,展示了在健康成年人、处于阿尔茨海默病进程中的人、患病患者以及少数记忆异常出色的高龄人群(称为超级老年人)中,海马中新生神经元的行为方式。
大脑的记忆“育苗室”
在大脑深处的海马体中,有一个称为齿状回的区域,类似记忆的“育苗室”,新的神经元可以由驻留的干细胞产生。研究者从38位已故捐赠者的大脑中切取了该区域,捐赠者年龄从年轻成年人到记忆表现和阿尔茨海默相关病变各异的老年人不等。通过多组学单细胞测序(同时读取基因活动与DNA包装紧密程度),他们分析了超过35万个单个细胞核。这使得他们能够可靠地区分神经干细胞、神经母细胞(早期新生细胞)和未成熟颗粒神经元,并映射这些细胞如何逐步成熟为加入记忆回路的完整神经元。他们的数据明确支持成人海马中新生神经元存在一个按步骤发展的轨迹。
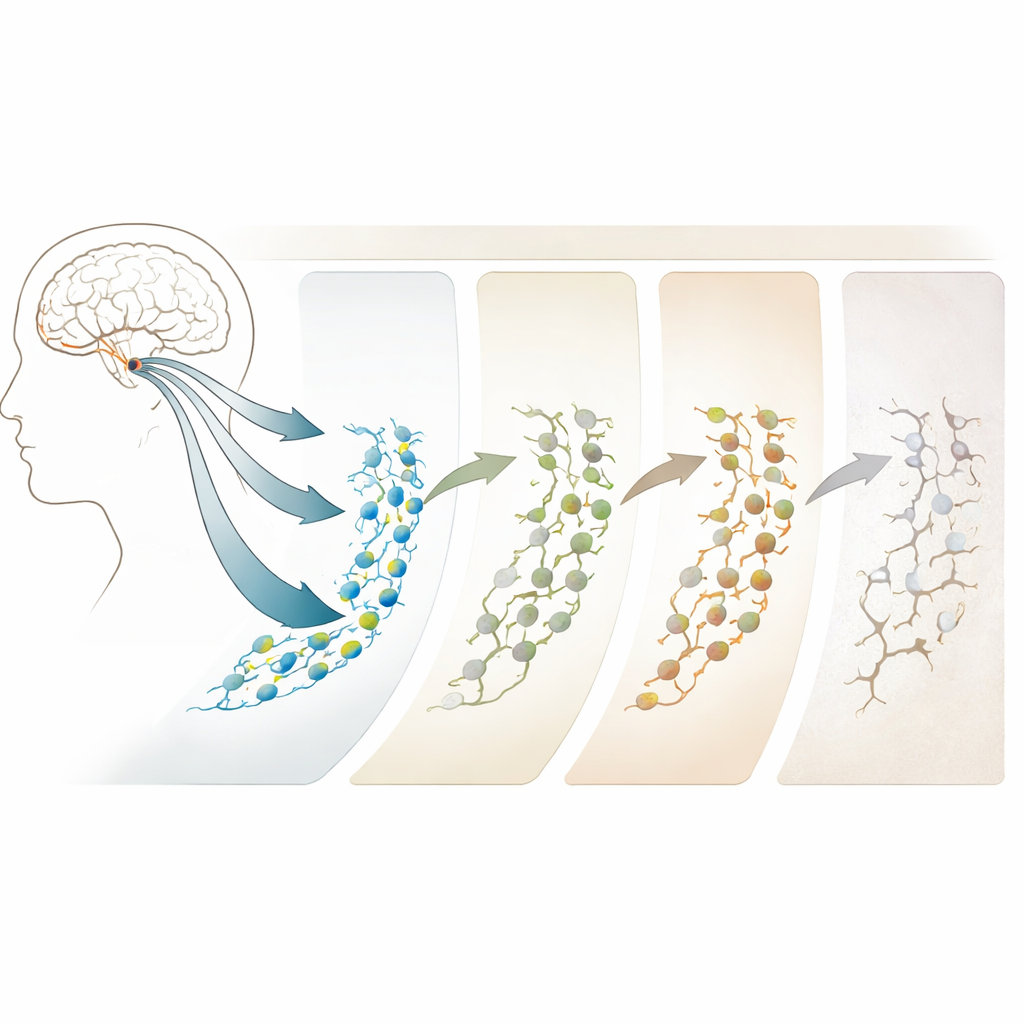
年龄与阿尔茨海默如何改变这一路径
将年轻成年人与老年组比较显示,衰老和阿尔茨海默并非简单地将神经发生打开或关闭,而是以更复杂的方式重塑这一过程。在处于临床前中度病理的人群——那些似乎从正常衰老向阿尔茨海默过渡的个体中,干细胞数量实际上增加了,但神经发生的后期阶段开始出现衰弱。在确诊阿尔茨海默患者中,神经母细胞和未成熟神经元明显减少,尽管类干细胞样细胞更为丰富。引人注目的是,最一致的变化并非出现在基因本身,而是在DNA的可及区域——这些区域像门一样打开或关闭,控制哪些基因可以被利用。这些表观遗传学的变化,尤其是在与突触和神经元结构相关的区域,早期出现并随病情加重,是潜在的早期预警标志和治疗靶点。
韧性的分子指纹
超级老年人——那些80多岁甚至更老却记忆力堪比年轻成年人的人——为研究认知韧性提供了重要窗口。他们的海马中神经母细胞和未成熟神经元显著多于阿尔茨海默患者,且常常多于典型的老年人。关键差异并非体现在干细胞的大幅变化上,而是在成千上万个在神经母细胞和未成熟神经元中更开放的DNA区域,这些开放区域支持强劲的生长和突触功能。研究团队定义了一个“韧性评分”,涵盖在年轻成年人、健康老年人和超级老年人中保持稳定但在阿尔茨海默中崩溃的基因和DNA区域。许多这些因子与维持神经连接和高效信息传递有关。超级老年人还显示出独特的调控网络模式——控制蛋白与DNA开关的组合在某些方面类似于年轻人,但也包含可能推动新生神经元进入特别强健、长久状态的独特激活子。
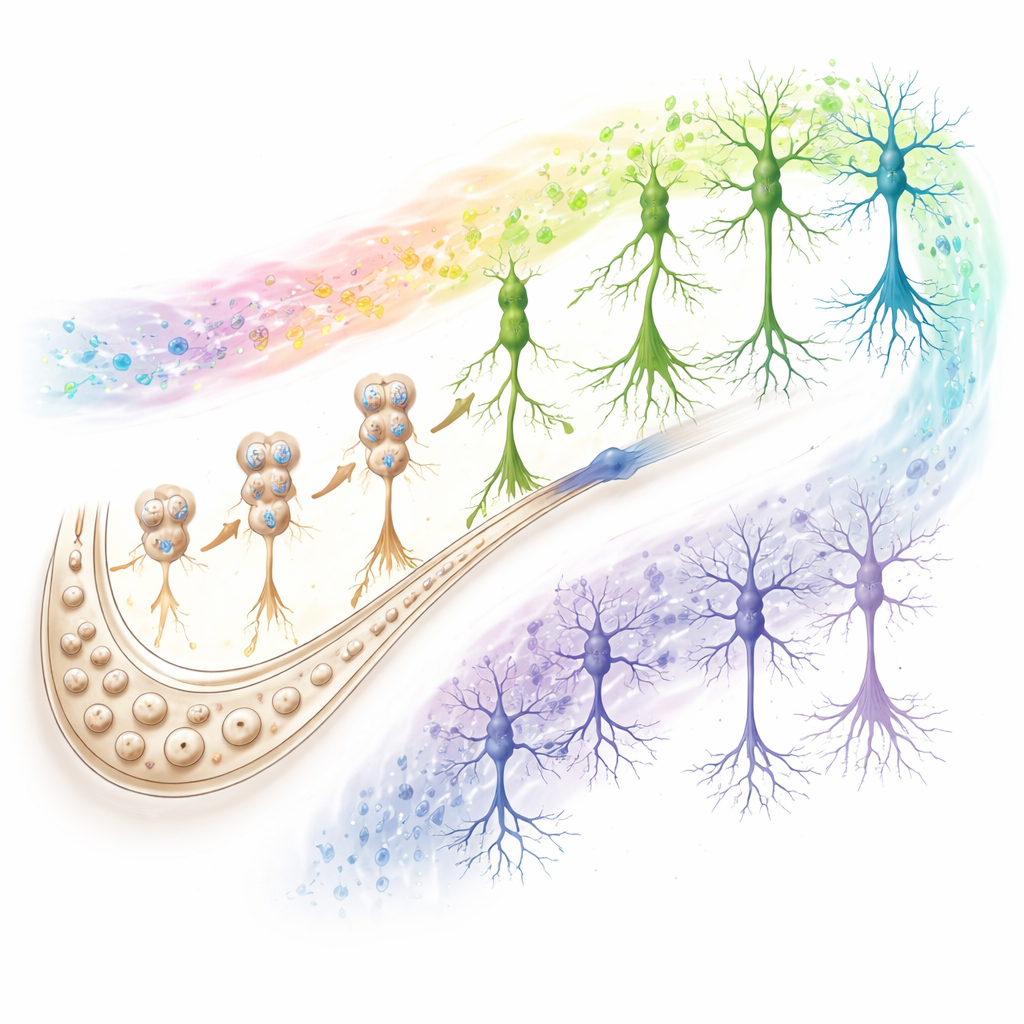
标志成功与失败衰老的回路
研究并未只停留在新生神经元层面。通过检查所有主要细胞类型,作者发现维持或破坏认知的信号集中在两个关键角色:CA1神经元(海马的核心输出站)和星形胶质细胞(管理化学环境并帮助调节突触的支持细胞)。在成功衰老者和超级老年人中,CA1神经元的基因支持强健的突触传递、能量生产和细胞清理通路,而星形胶质细胞显示出有利于保护性反应的染色质模式。在走向阿尔茨海默的人群中,这些相同通路朝相反方向变化。细胞间通信分析突出显示,CA1神经元、星形胶质细胞与神经发生细胞之间的黏附与基于谷氨酸的信号在临床前和阿尔茨海默组中减弱,提示兴奋性突触的崩溃是认知衰退的共同特征。
这对保护记忆意味着什么
综合起来,结果描绘了一幅清晰的图景:成年人确实持续生成新的海马神经元,但这一过程对年龄和疾病极为敏感。最早且最明显的变化发生在染色质可及性层面——即DNA的包装方式——远早于许多基因活动出现明显改变。在具有韧性的脑(如超级老年人)中,分子网络使神经发生和突触通信在高龄时仍维持“青年化”的模式。在易受损的脑中,这些网络发生转变,导致新生神经元发育停滞与海马回路的逐步崩解。通过揭示这些表观遗传和细胞学签名,研究指向了未来可能保护记忆的策略:不仅仅清除斑块,而是保持大脑的记忆育苗室开放、让DNA的“门”保持适当调节,并增强突触的韧性。
引用: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
关键词: 海马神经发生, 认知韧性, 超级老年人(SuperAgers), 表观遗传学, 阿尔茨海默病