Clear Sky Science · sv
Neurogeneration i människans hippocampus under vuxenlivet, åldrandet och Alzheimers sjukdom
Varför nya hjärnceller hos vuxna betyder något
I årtionden har forskare diskuterat en enkel men djup fråga: bildar vuxna människor nya hjärnceller i hjärnans minnescenter, och om så är fallet, hjälper detta oss att skydda minnets funktion och förebygga Alzheimers sjukdom? Denna studie tar itu med debatten direkt genom att kombinera ledande enkelcellsmetoder med postmortalt mänskligt hjärnvävnad för att visa hur nyfödda neuroner i hippocampus beter sig hos friska vuxna, hos personer på väg mot Alzheimers, hos patienter med sjukdomen och hos sällsynta äldre vuxna med exceptionellt minne, så kallade SuperAgers.
Hjärnans minnesuppfödning
Djupt i hippocampus finns dentate gyrus, en slags minnes"uppfödning" där nya neuroner kan uppstå från lokala stamceller. Författarna dissekerade denna region från hjärnor från 38 avlidna donatorer, från unga vuxna till äldre med varierande minnesprestanda och Alzheimersrelaterade förändringar. Med multiomisk enkelcellssekvensering—som läser både genaktivitet och hur tätt DNA är paketerat—analyserade de mer än 350 000 individuella cellkärnor. Detta gjorde det möjligt att tillförlitligt skilja neurala stamceller, neuroblaster (tidiga nyfödda celler) och omogna granule‑neuron, samt att kartlägga hur dessa utvecklas till fullt mogna neuroner som ingår i minneskretsar. Deras data stöder bestämt förekomsten av en stegvis utveckling av nya neuroner i den vuxna människans hippocampus.
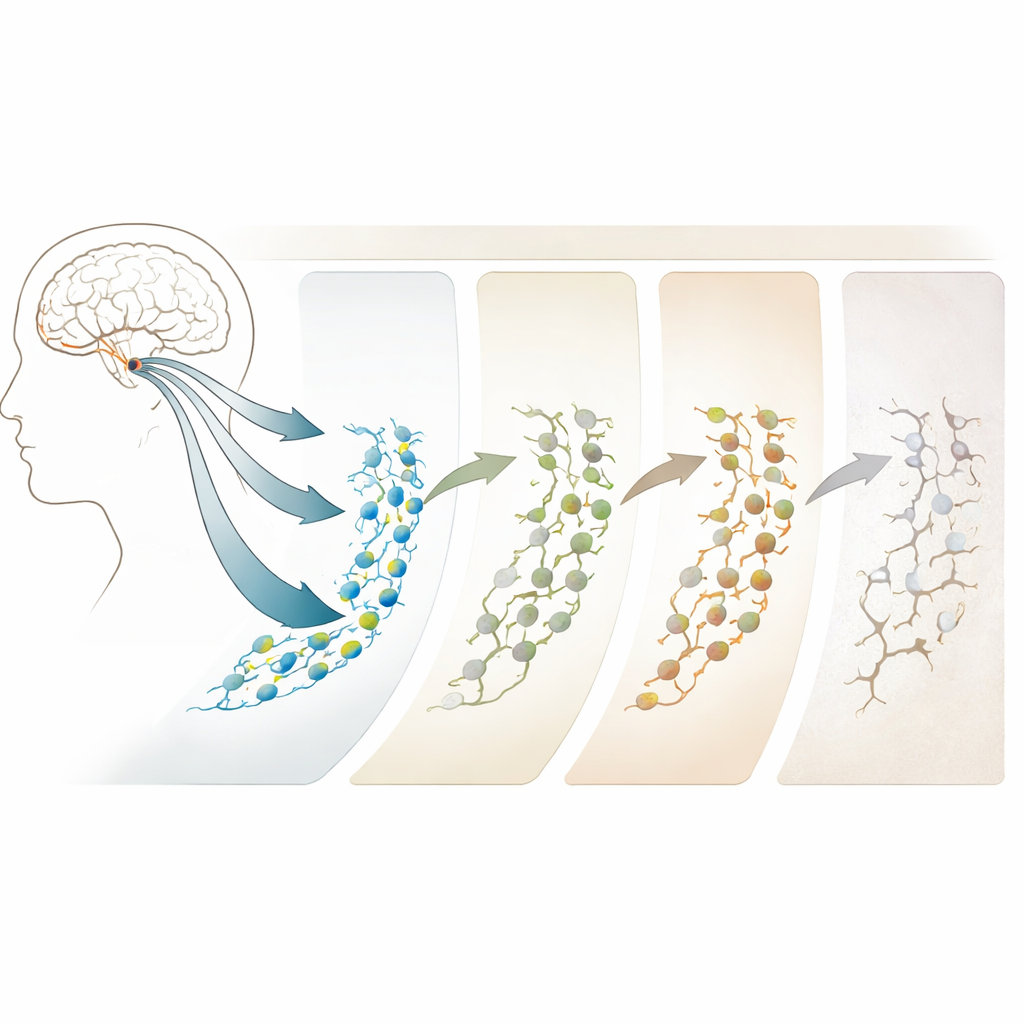
Hur ålder och Alzheimer förändrar förloppet
Jämförelser mellan unga vuxna och äldre grupper visade att åldrande och Alzheimer inte helt enkelt slår av eller på neurogenes; istället omformar de processen. Hos personer med preklinisk intermediär patologi—individer som verkar vara på väg från normalt åldrande mot Alzheimer—ökar antalet stamceller faktiskt, men de senare stadierna av neurogenes börjar svikta. Vid full sjukdom är neuroblaster och omogna neuroner markant minskade, även om stamcells‑lika celler är mer rikliga. Slående nog är de mest konsekventa förändringarna inte i generna själva, utan i DNA‑regioner som blir mer eller mindre åtkomliga, som grindar som öppnas eller stängs för att styra vilka gener som kan användas. Dessa epigenetiska skiften, särskilt i regioner kopplade till synapser och neuronstruktur, uppträder tidigt och intensifieras med sjukdomen, vilket gör dem till potentiella tidiga varningssignaler och terapeutiska mål.
De molekylära fingeravtrycken för resiliens
SuperAgers—personer i 80‑årsåldern och äldre som minns lika bra som betydligt yngre vuxna—gav en inblick i resiliens. Deras hippocampi innehöll betydligt fler neuroblaster och omogna neuroner än de hos Alzheimerspatienter, och ofta fler än hos typiska äldre vuxna. Istället för omfattande förändringar i stamceller låg nyckelskillnaderna i tusentals DNA‑regioner som var mer öppna i neuroblaster och omogna neuroner, vilket stöder robust tillväxt och synaptisk funktion. Teamet definierade en ”resilienspoäng” som fångar gener och DNA‑regioner som förblir stabila hos unga vuxna, friska åldrande och SuperAgers men kollapsar vid Alzheimers. Många av dessa är kopplade till att bevara neuronala förbindelser och effektiv kommunikation. SuperAgers visade också ett distinkt mönster av reglerande nätverk—kombinationer av kontrollproteiner och DNA‑brytare—som i vissa avseenden liknar unga vuxna men även innehåller unika aktivatorer som kan driva nyfödda neuroner mot ett särskilt robust och långvarigt tillstånd.
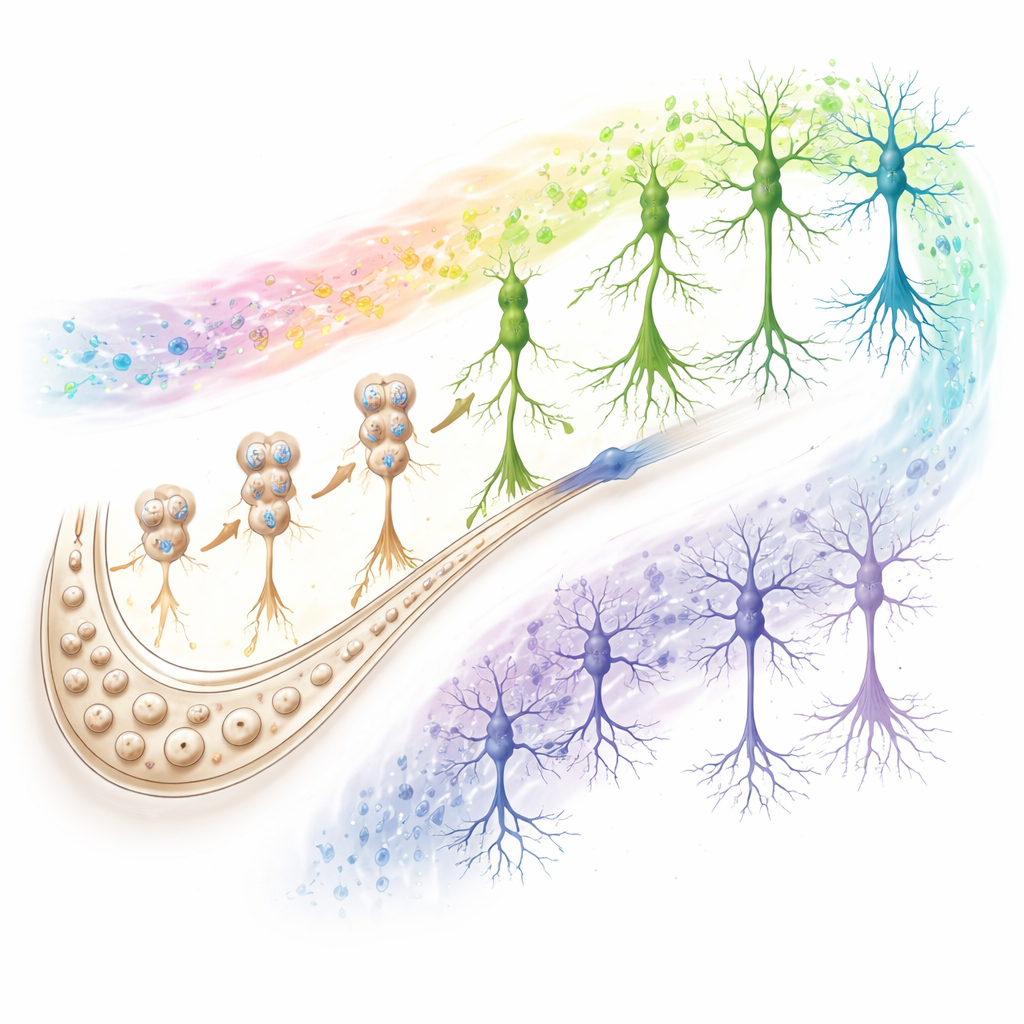
Kretsar som skiljer framgångsrikt från misslyckat åldrande
Studien stannade inte vid nyfödda neuroner. Genom att undersöka alla huvudtyper av celler fann författarna att signaler som bevarar eller urholkar kognition koncentreras till två nyckelaktörer: CA1‑neuroner (en central utgångsstation i hippocampus) och astrocyter (stödjeceller som hanterar den kemiska miljön och hjälper till att reglera synapser). Hos framgångsrika åldrande och SuperAgers stöder gener i CA1‑neuroner stark synaptisk transmission, energiproduktion och cellulära rengöringsvägar, medan astrocyter visar kromatinmönster som gynnar skyddande responser. Hos personer på väg mot Alzheimer driver dessa samma vägar i motsatt riktning. Analyser av cell‑till‑cell‑kommunikation lyfte fram försvagad adhesion och glutamatbaserad signalering mellan CA1‑neuroner, astrocyter och neurogena celler i prekliniska och Alzheimergrupper, vilket tyder på att nedbrytningen av excitatoriska synapser är ett gemensamt kännetecken för kognitiv försämring.
Vad detta betyder för att skydda minnet
Tillsammans målar resultaten upp en detaljerad bild: vuxna människor fortsätter att generera nya hippocampala neuroner, men denna process är extremt känslig för ålder och sjukdom. De tidigaste och mest robusta förändringarna sker på nivån av kromatinåtkomlighet—sättet DNA är paketerat—långt innan många gener visar synliga förändringar i sin aktivitet. I resilienta hjärnor, såsom hos SuperAgers, håller molekylära nätverk neurogenes och synaptisk kommunikation i ett "ungdomligt" läge trots hög ålder. I sårbara hjärnor skiftar dessa samma nätverk, vilket leder till att utvecklingen av nya neuroner stannar upp och hippocampala kretsar trådas upp. Genom att avslöja dessa epigenetiska och cellulära signaturer pekar studien mot strategier som en dag kan bevara minnet: terapier inriktade inte bara på att avlägsna plack, utan på att hålla hjärnans minnesuppfödning öppen, dess DNA‑grindar korrekt inställda och dess synapser resilient.
Citering: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Nyckelord: hippocampal neurogenes, kognitiv resiliens, SuperAgers, epigenetik, Alzheimers sjukdom