Clear Sky Science · pl
Neurogeneza hipokampa u dorosłych, w starzeniu się i w chorobie Alzheimera
Dlaczego nowe komórki mózgowe u dorosłych mają znaczenie
Przez dekady naukowcy spierali się o proste, lecz doniosłe pytanie: czy dorośli ludzie wytwarzają nowe komórki mózgowe w ośrodku pamięci, a jeśli tak — czy to chroni nas przed utratą pamięci i chorobą Alzheimera? To badanie mierzy się bezpośrednio z tą debatą, łącząc najnowocześniejsze narzędzia pojedynczych komórek z tkanką mózgową pobraną pośmiertnie, by pokazać, jak zachowują się nowo powstające neurony w hipokampie u zdrowych dorosłych, u osób na drodze do Alzheimera, u pacjentów z chorobą oraz u rzadkich starszych osób o wyjątkowej pamięci, zwanych SuperAgers.
Pielęgniarnia pamięci w mózgu
Głęboko w hipokampie znajduje się zakręt zębaty, coś w rodzaju „pielęgniarni” pamięci, gdzie nowe neurony mogą powstawać z lokalnych komórek macierzystych. Autorzy wyodrębnili ten rejon z mózgów 38 zmarłych dawców, od młodych dorosłych po starsze osoby o różnym poziomie wydajności pamięci i zmian związanych z Alzheimerem. Wykorzystując wieloomowe sekwencjonowanie pojedynczych komórek — które odczytuje zarówno aktywność genów, jak i stopień upakowania DNA — przeanalizowali ponad 350 000 pojedynczych jąder komórkowych. Pozwoliło to wiarygodnie rozróżnić komórki macierzyste nerwowe, neuroblasty (wczesne komórki nowo narodzone) i niedojrzałe neurony ziarniste oraz odtworzyć, jak przechodzą one w w pełni dojrzałe neurony włączające się w obwody pamięci. Dane jednoznacznie wspierają istnienie etapowej trajektorii rozwojowej nowych neuronów w dorosłym hipokampie człowieka.
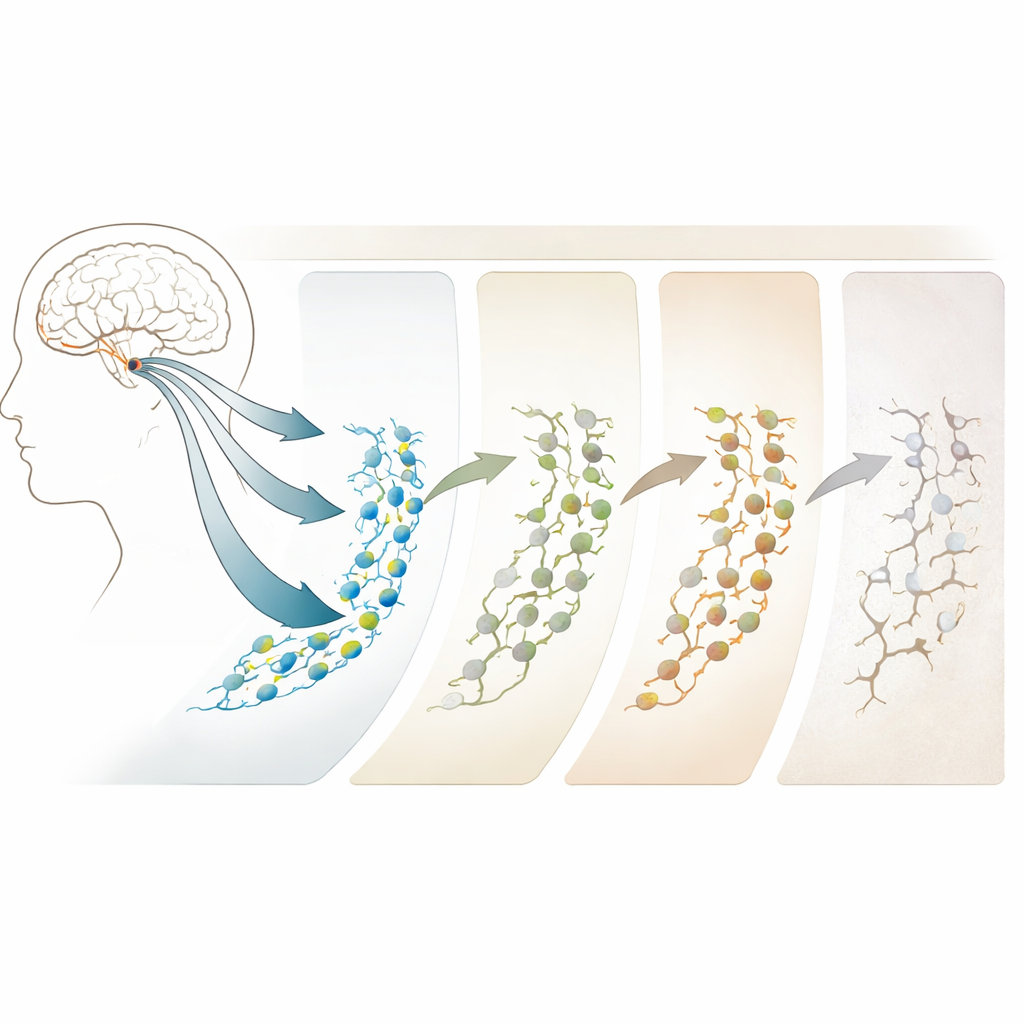
Jak wiek i Alzheimer zmieniają trajektorię
Porównanie młodych dorosłych z grupami starszymi wykazało, że starzenie się i Alzheimer nie włączają ani nie wyłączają neurogenezy jak przełącznika; raczej ją przekształcają. U osób z wczesną, pośrednią patologią — będących w przejściu od normalnego starzenia do Alzheimera — liczba komórek macierzystych faktycznie rośnie, ale późniejsze etapy neurogenezy zaczynają słabnąć. W pełnej chorobie Alzheimera liczba neuroblastów i niedojrzałych neuronów jest wyraźnie zredukowana, mimo że komórki o cechach komórek macierzystych są bardziej liczne. Uderzające jest to, że najbardziej spójne zmiany nie zachodzą w genach samych w sobie, lecz w regionach DNA, które stają się bardziej lub mniej dostępne — jak bramy, które się otwierają lub zamykają, kontrolując, które geny można aktywować. Te zmiany epigenetyczne, zwłaszcza w obszarach powiązanych z synapsami i strukturą neuronalną, pojawiają się wcześnie i nasilają w chorobie, co czyni je potencjalnymi wczesnymi sygnałami ostrzegawczymi i celami terapeutycznymi.
Molekularne odciski odporności
SuperAgers — osoby po osiemdziesiątce i starsze, które pamiętają równie dobrze jak dużo młodsi dorośli — dały wgląd w mechanizmy odporności. Ich hipokamp zawierał znacząco więcej neuroblastów i niedojrzałych neuronów niż u pacjentów z Alzheimerem, a często także więcej niż u typowych starszych dorosłych. Zamiast masywnych zmian w komórkach macierzystych, kluczowe różnice dotyczyły tysięcy regionów DNA, które były bardziej otwarte w neuroblastach i niedojrzałych neuronach, wspierając silny wzrost i funkcję synaptyczną. Zespół zdefiniował „wskaźnik odporności” obejmujący geny i regiony DNA stabilne u młodych dorosłych, zdrowych starzejących się i SuperAgers, ale załamujące się w chorobie Alzheimera. Wiele z tych elementów wiąże się z utrzymaniem połączeń neuronalnych i efektywnej komunikacji. SuperAgers wykazali również odmienny wzorzec sieci regulatorowych — kombinacji białek kontrolnych i przełączników DNA — który w pewnych aspektach przypomina młodych dorosłych, ale zawiera też unikalne aktywatory mogące kierować nowo powstałe neurony ku szczególnie odpornemu, długotrwałemu stanowi.
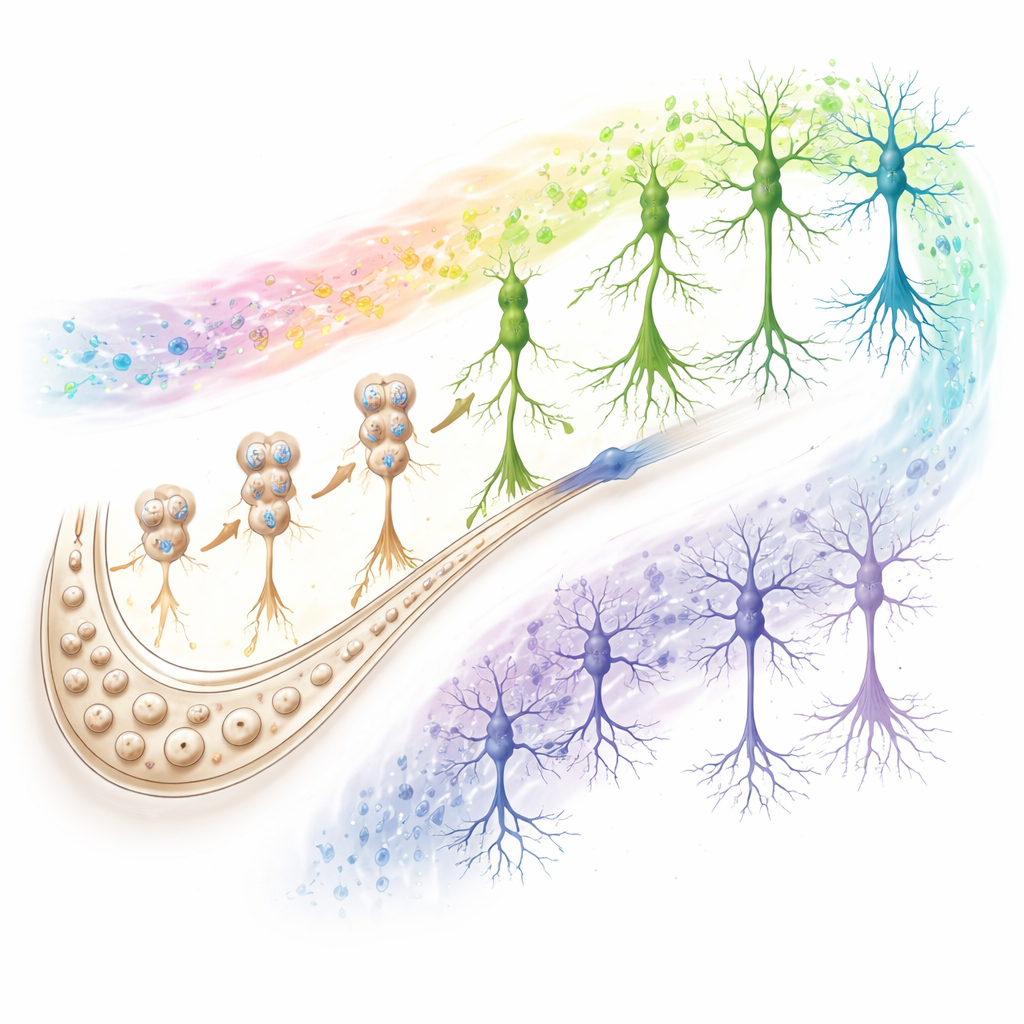
Obwody oznaczające udane versus zawodzące starzenie
Badanie nie zakończyło się na nowo narodzonych neuronach. Analizując wszystkie główne typy komórek, autorzy odkryli, że sygnały zachowujące lub erodujące poznanie koncentrują się w dwóch kluczowych aktorach: neuronach CA1 (głównej stacji wyjściowej hipokampa) oraz astrocytach (komórkach wspierających, które zarządzają środowiskiem chemicznym i pomagają regulować synapsy). U osób dobrze się starzejących i u SuperAgers geny w neuronach CA1 wspierają silne przewodnictwo synaptyczne, produkcję energii i szlaki oczyszczania komórkowego, podczas gdy astrocyty wykazują wzorce chromatyny sprzyjające reakcjom ochronnym. U osób na drodze do Alzheimera te same szlaki zmierzają w przeciwnym kierunku. Analizy komunikacji międzykomórkowej uwypukliły osłabienie adhezji i sygnalizacji glutaminergicznej między neuronami CA1, astrocytami i komórkami neurogennymi w grupach przedklinicznych i z Alzheimerem, sugerując, że rozpad synaps pobudzających jest wspólnym znakiem towarzyszącym spadkowi funkcji poznawczych.
Co to oznacza dla ochrony pamięci
W sumie wyniki tworzą szczegółowy obraz: dorośli ludzie nadal generują nowe neurony hipokampa, ale proces ten jest wyjątkowo wrażliwy na wiek i chorobę. Najwcześniejsze i najsilniejsze zmiany zachodzą na poziomie dostępności chromatyny — sposobu pakowania DNA — na długo przed tym, jak wiele genów wyraźnie zmienia swoją aktywność. W mózgach odpornych, takich jak u SuperAgers, sieci molekularne utrzymują neurogenezę i komunikację synaptyczną w „młodzieńczym” trybie pomimo zaawansowanego wieku. W mózgach wrażliwych te same sieci zmieniają się, prowadząc do zatrzymania rozwoju nowych neuronów i rozluźnienia obwodów hipokampa. Poprzez ujawnienie tych epigenetycznych i komórkowych sygnatur badanie wskazuje kierunki strategii, które mogą kiedyś chronić pamięć: terapie skierowane nie tylko na usuwanie blaszek, ale na utrzymanie otwartej „pielęgniarni pamięci”, właściwe wyregulowanie „bram” DNA i zachowanie odporności synaps.
Cytowanie: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Słowa kluczowe: neurogeneza hipokampa, odporność poznawcza, SuperAgers, epigenetyka, choroba Alzheimera