Clear Sky Science · ja
成人期、高齢化およびアルツハイマー病におけるヒト海馬の神経新生
なぜ成人の新しい脳細胞が重要なのか
何十年にもわたり、科学者たちは単純だが深遠な疑問を巡って議論してきました:成人の人間は記憶の中枢である海馬で新しい脳細胞を生み出すのか、そしてもしそうならそれは記憶喪失やアルツハイマー病から私たちを守るのに役立つのか?本研究は、最先端の単一細胞技術と死後のヒト脳組織を組み合わせることでこの議論に正面から取り組み、成人の海馬における新生ニューロンが健常者、アルツハイマーへの経路上にある人、患者、および「スーパーエイジャー」と呼ばれる記憶力に優れた稀な高齢者でどのように振る舞うかを示しています。
脳の記憶の苗床
海馬の深部には歯状回(デンテートジルス)と呼ばれる、常在する幹細胞から新しいニューロンが生まれる可能性のある「記憶の苗床」のような領域があります。著者らはこの領域を、若年成人から記憶機能やアルツハイマー関連変化の程度が異なる高齢者まで含む38人の献体の脳から解剖しました。遺伝子発現とDNAのパッケージ状態の両方を読み取るマルチオミクス単一細胞シーケンスを用いて、35万以上の個々の細胞核を解析しました。これにより、神経幹細胞、神経芽細胞(初期の新生細胞)、未熟な顆粒ニューロンを確実に区別し、これらがどのようにして記憶回路に加わる完全に成熟したニューロンへと進行するかをマップできました。データは、成人ヒト海馬における新生ニューロンの段階的な発達軌道の存在を明確に支持しています。
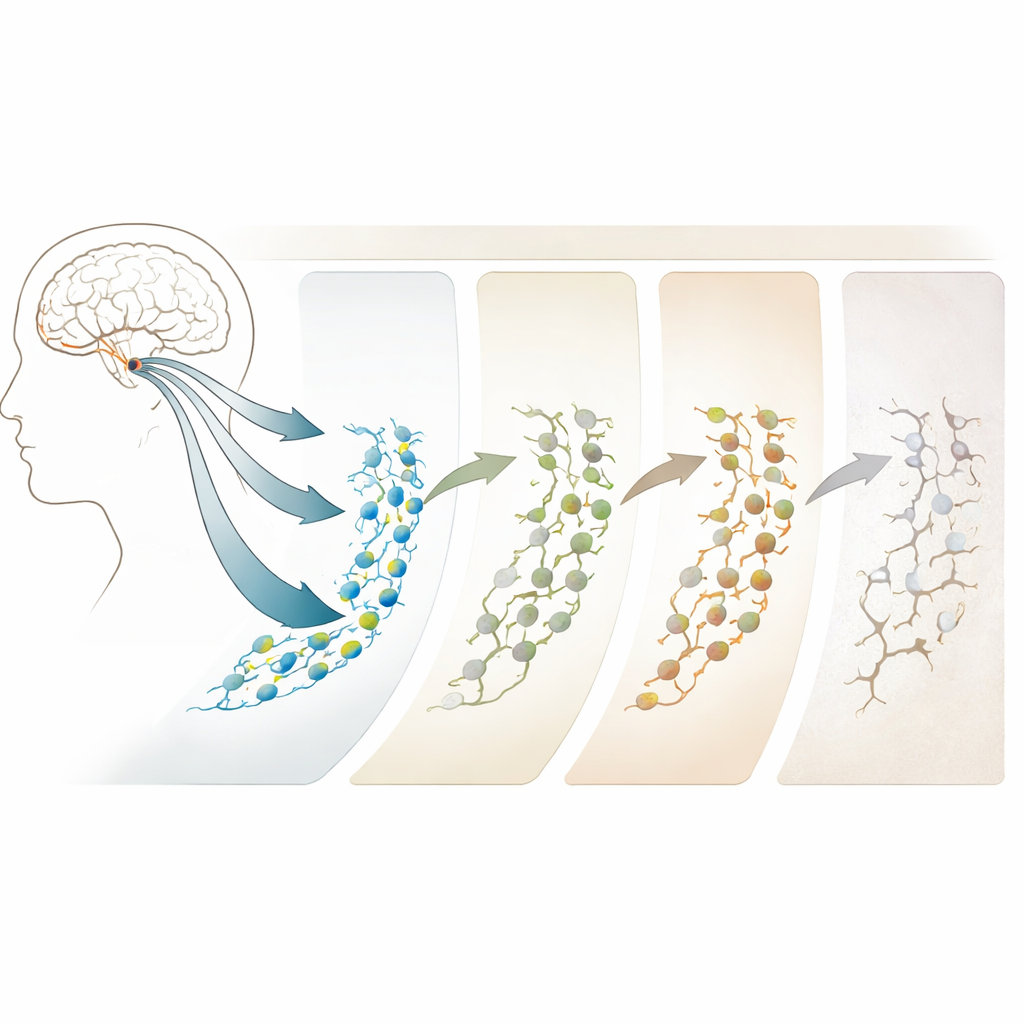
年齢とアルツハイマーが軌道を変える仕方
若年成人と高齢群を比較すると、加齢やアルツハイマーは単に神経新生をオン・オフするのではなく、その形を変えることが明らかになりました。前臨床の中間病理を示す人々—正常な加齢からアルツハイマーへ移行しているように見える個体—では、幹細胞の数は実際に増える一方で、神経新生の後期段階がつまずき始めます。完全なアルツハイマー病では、神経芽細胞や未熟なニューロンが著しく減少しているのに対し、幹細胞様の細胞はより多く存在しています。注目すべきは、最も一貫した変化は遺伝子そのものではなく、遺伝子の利用可能性を制御する門のように開閉するDNA領域の変化(クロマチンのアクセスビリティ)であることです。これらのエピジェネティックな変化は、特にシナプスやニューロンの構造に関連する領域で早期に現れ、病気とともに強まるため、初期の警告サインや治療標的として注目されます。
回復力の分子指紋
80代以上で若年成人と同等に記憶するスーパーエイジャーは、回復力を理解するための手がかりを与えてくれました。彼らの海馬には、アルツハイマー患者よりも、しばしば典型的な高齢者よりも多くの神経芽細胞や未熟なニューロンが含まれていました。幹細胞自体の大規模な変化よりも、鍵となる差異は神経芽細胞や未熟ニューロンでより開かれている何千ものDNA領域にあり、これが旺盛な成長とシナプス機能を支えていました。研究チームは「回復力スコア」を定義し、若年成人、健康な高齢者、スーパーエイジャーでは安定しているがアルツハイマーでは崩れる遺伝子やDNA領域を捉えました。多くはニューロンの結合と効率的な情報伝達の維持に結び付いています。スーパーエイジャーはまた、規制ネットワークの独特なパターンを示し—制御タンパク質とDNAスイッチの組み合わせ—一部は若年成人に似る一方で、新生ニューロンを特に強靭で長持ちする状態へと導く可能性のある独自の活性化因子も含んでいました。
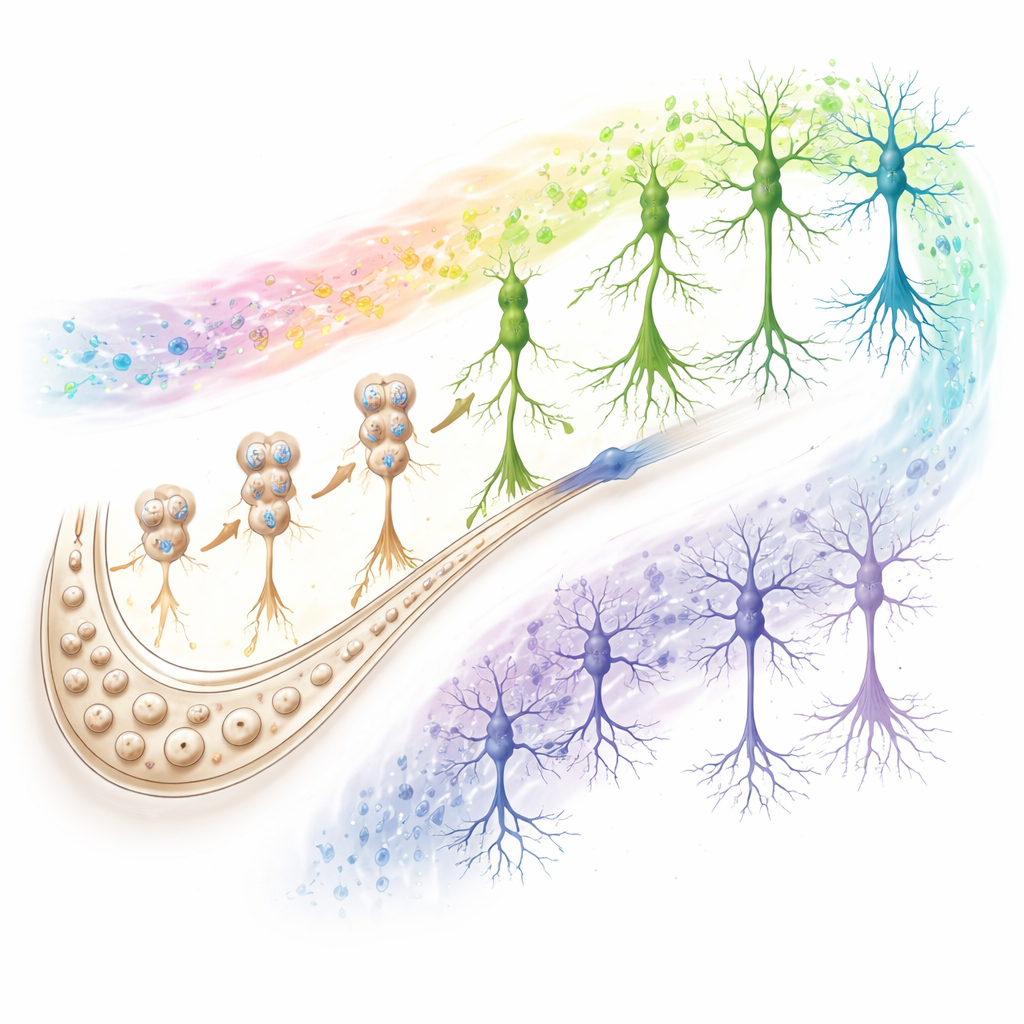
成功する加齢と失敗する加齢を示す回路
研究は新生ニューロンだけに留まりませんでした。すべての主要な細胞型を調べたところ、認知を守るか蝕むかに関わるシグナルは2つの主要なプレイヤーに集中していることがわかりました:海馬の主要な出力ステーションであるCA1ニューロンと、化学環境を管理しシナプスを助ける支持細胞であるアストロサイトです。成功する加齢者やスーパーエイジャーでは、CA1ニューロンの遺伝子は強いシナプス伝達、エネルギー産生、細胞のクリアランス経路を支持し、アストロサイトは保護的な反応を促すクロマチンパターンを示しました。アルツハイマーへの道をたどる人々では、これら同じ経路が逆方向へと傾きます。細胞間コミュニケーションの解析は、前臨床群やアルツハイマー群においてCA1ニューロン、アストロサイト、神経新生細胞間の接着やグルタミン酸を介したシグナル伝達が弱まっていることを強調しており、興奮性シナプスの崩壊が認知低下の共通の特徴であることを示唆しています。
記憶を守るための意味
総合すると、結果は詳細な図を描きます:成人のヒトは海馬で新しいニューロンを作り続けているが、このプロセスは年齢と病気に非常に敏感です。最も早期かつ顕著な変化はクロマチンのアクセスビリティ、すなわちDNAのパッケージ方法のレベルで起こり、多くの遺伝子の活性が目に見えて変わるよりずっと前に現れます。スーパーエイジャーのような回復力のある脳では、分子ネットワークが神経新生とシナプス通信を高度な年齢にもかかわらず「若々しい」モードで維持します。脆弱な脳では同じネットワークが変化し、新生ニューロンの発達が停滞し海馬回路がほつれていきます。これらのエピジェネティックおよび細胞の署名を明らかにすることで、本研究は記憶を保つための戦略を示唆します:プラークの除去だけでなく、記憶の苗床を開いたままにし、DNAのゲートを適切に調整し、シナプスを強靭に保つことを目指す治療法です。
引用: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
キーワード: 海馬の神経新生, 認知的回復力, スーパーエイジャー, エピジェネティクス, アルツハイマー病