Clear Sky Science · fr
Neurogénèse hippocampique humaine à l’âge adulte, au vieillissement et dans la maladie d’Alzheimer
Pourquoi les nouvelles cellules cérébrales chez l’adulte comptent
Pendant des décennies, les scientifiques ont débattu d’une question simple mais profonde : les humains adultes produisent‑ils de nouvelles cellules cérébrales dans le centre de la mémoire du cerveau, et si oui, cela aide‑t‑il à nous protéger de la perte de mémoire et de la maladie d’Alzheimer ? Cette étude aborde ce débat de front en combinant des outils unicellulaires de pointe et du tissu cérébral humain post‑mortem pour montrer comment les neurones nouvellement nés dans l’hippocampe se comportent chez des adultes en bonne santé, chez des personnes en voie de développer la maladie d’Alzheimer, chez des patients atteints, et chez de rares personnes âgées dotées d’une mémoire exceptionnelle appelées SuperAgers.
La pépinière de la mémoire
Au cœur de l’hippocampe se trouve le gyrus denté, une sorte de « pépinière » de la mémoire où de nouveaux neurones peuvent émerger à partir de cellules souches résidentes. Les auteurs ont disséqué cette région dans les cerveaux de 38 donneurs décédés, allant de jeunes adultes à des personnes âgées présentant différents niveaux de performances mnésiques et d’altérations liées à la maladie d’Alzheimer. En utilisant le séquençage multi‑omique unicellulaire — qui lit à la fois l’activité des gènes et la compaction de l’ADN — ils ont analysé plus de 350 000 noyaux cellulaires individuels. Cela leur a permis de distinguer de manière fiable les cellules souches neurales, les neuroblastes (cellules nouvellement nées précoces) et les neurones granulaires immatures, et de cartographier leur progression vers des neurones pleinement matures intégrés aux circuits de la mémoire. Leurs données soutiennent fermement l’existence d’une trajectoire développementale en étapes des nouveaux neurones dans l’hippocampe humain adulte.
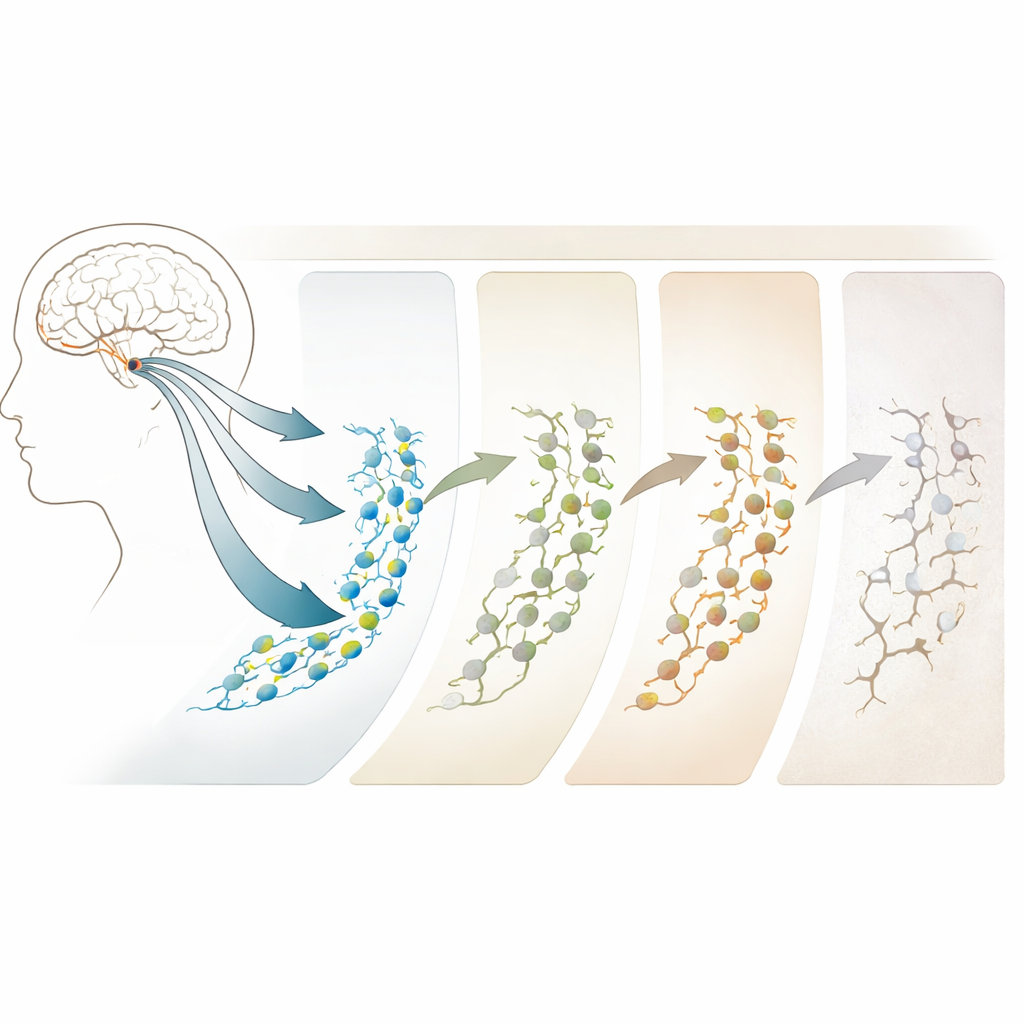
Comment l’âge et la maladie d’Alzheimer modulent la trajectoire
La comparaison entre jeunes adultes et groupes plus âgés a révélé que le vieillissement et la maladie d’Alzheimer ne se contentent pas d’activer ou d’éteindre la neurogenèse ; ils la remodèlent. Chez les personnes présentant une pathologie intermédiaire préclinique — celles qui semblent passer d’un vieillissement normal vers la maladie d’Alzheimer — le nombre de cellules souches augmente en réalité, mais les stades ultérieurs de la neurogenèse commencent à faiblir. Dans la maladie d’Alzheimer avancée, les neuroblastes et les neurones immatures sont nettement réduits, alors même que des cellules de type souches sont plus abondantes. De manière frappante, les changements les plus constants ne se situent pas tant dans les gènes eux‑mêmes que dans des régions d’ADN qui deviennent plus ou moins accessibles, comme des portes qui s’ouvrent ou se ferment pour contrôler l’utilisation des gènes. Ces changements épigénétiques, notamment dans des régions liées aux synapses et à la structure neuronale, apparaissent tôt et s’intensifient avec la maladie, faisant d’eux des signaux d’alerte précoces et des cibles thérapeutiques potentielles.
Les empreintes moléculaires de la résilience
Les SuperAgers — personnes dans les années 80 et plus qui se souviennent aussi bien que des adultes beaucoup plus jeunes — offrent une fenêtre sur la résilience. Leurs hippocampes contenaient significativement plus de neuroblastes et de neurones immatures que ceux des patients Alzheimer, et souvent plus que ceux d’adultes âgés typiques. Plutôt que des changements massifs au niveau des cellules souches, les différences clés résidaient dans des milliers de régions d’ADN plus ouvertes dans les neuroblastes et les neurones immatures, soutenant une croissance robuste et une fonction synaptique performante. L’équipe a défini un « score de résilience » regroupant gènes et régions d’ADN qui restent stables chez les jeunes adultes, les vieillissants en bonne santé et les SuperAgers mais s’effondrent dans la maladie d’Alzheimer. Nombre d’entre eux sont liés au maintien des connexions neuronales et à une communication efficace. Les SuperAgers présentaient aussi un profil distinct de réseaux régulateurs — combinaisons de protéines de contrôle et d’interrupteurs d’ADN — qui ressemble en partie à celui des jeunes adultes mais inclut aussi des activateurs uniques susceptibles de pousser les neurones nouvellement nés vers un état particulièrement robuste et durable.
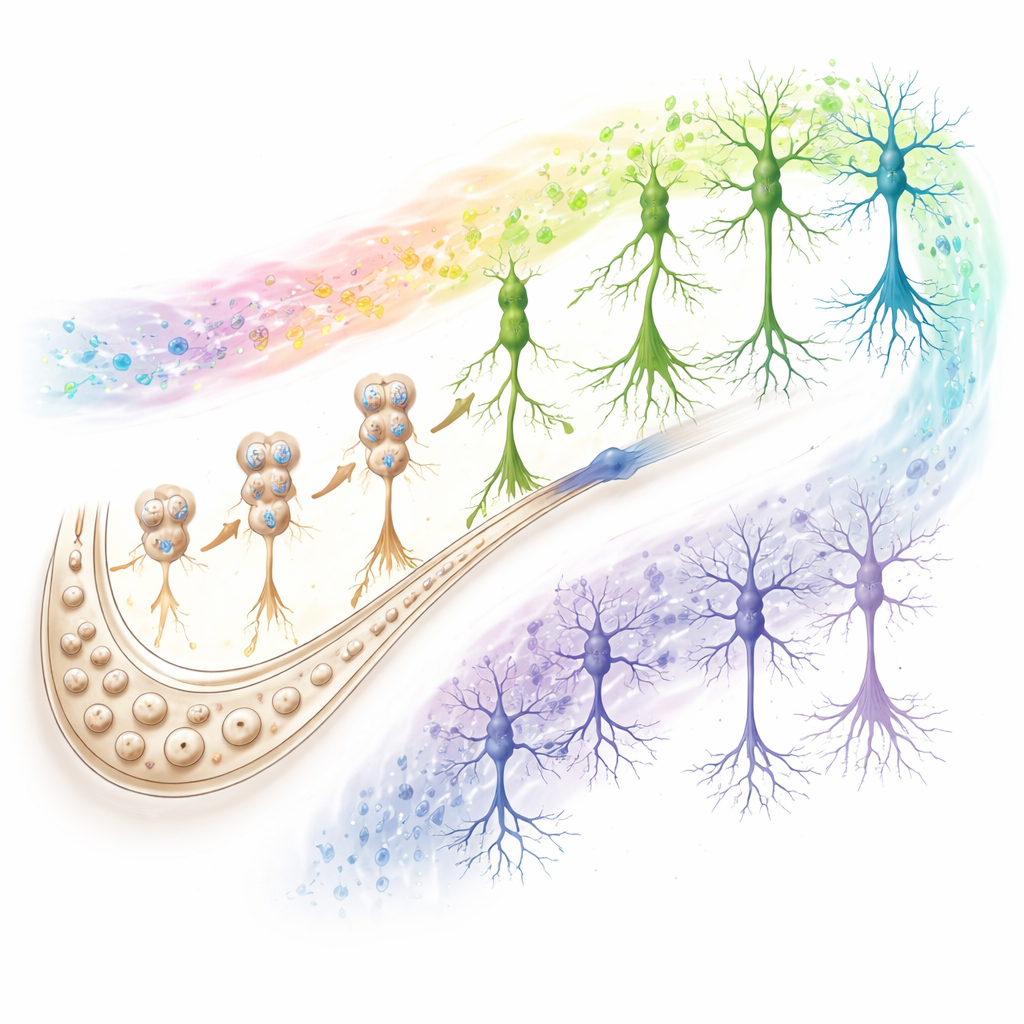
Les circuits qui distinguent un vieillissement réussi d’un vieillissement défaillant
L’étude ne s’est pas arrêtée aux neurones nouvellement nés. En examinant tous les types cellulaires majeurs, les auteurs ont observé que les signaux qui préservent ou érodent la cognition se concentrent sur deux acteurs clés : les neurones CA1 (une station de sortie centrale de l’hippocampe) et les astrocytes (cellules de soutien qui gèrent le milieu chimique et aident à réguler les synapses). Chez les vieillissants réussis et les SuperAgers, les gènes des neurones CA1 soutiennent une transmission synaptique forte, la production d’énergie et les voies de nettoyage cellulaire, tandis que les astrocytes présentent des motifs de chromatine favorisant des réponses protectrices. Chez les personnes en voie d’Alzheimer, ces mêmes voies dérivent en sens inverse. Les analyses de communication intercellulaire ont mis en évidence une adhésion affaiblie et une signalisation à base de glutamate réduite entre les neurones CA1, les astrocytes et les cellules neurogéniques dans les groupes précliniques et Alzheimer, suggérant que la rupture des synapses excitatrices est une caractéristique commune du déclin cognitif.
Ce que cela signifie pour la protection de la mémoire
Ensemble, les résultats dessinent un tableau détaillé : les humains adultes continuent bien de générer de nouveaux neurones hippocampiques, mais ce processus est extrêmement sensible à l’âge et à la maladie. Les changements les plus précoces et les plus marqués se produisent au niveau de l’accessibilité de la chromatine — la façon dont l’ADN est emballé — bien avant que de nombreux gènes ne modifient visiblement leur activité. Dans les cerveaux résilients, comme ceux des SuperAgers, des réseaux moléculaires maintiennent la neurogenèse et la communication synaptique dans un mode « juvénile » malgré l’âge avancé. Dans les cerveaux vulnérables, ces mêmes réseaux se décalent, entraînant un arrêt du développement des nouveaux neurones et l’effilochage des circuits hippocampiques. En révélant ces signatures épigénétiques et cellulaires, l’étude oriente vers des stratégies qui pourraient un jour préserver la mémoire : des thérapies visant non seulement à éliminer les plaques, mais aussi à maintenir la pépinière mnésique du cerveau ouverte, à régler correctement les « portes » de l’ADN et à préserver la résilience des synapses.
Citation: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Mots-clés: neurogénèse hippocampique, résilience cognitive, SuperAgers, épi-génétique, maladie d’Alzheimer